Abstract
Sudden cardiac death (SCD) is a major healthcare problem worldwide. The left ventricular ejection fraction is the most important predictor of SCD in patients with ischaemic and nonischaemic cardiomyopathy. Implantable cardioverter defibrillator (ICD) therapy prevents SCD in specific patient populations and various studies have analysed the efficacy of the ICD to prevent SCD. The purpose of this article is to describe the evidence supporting the use of ICD therapy and to discuss, whether all patients with an ejection fraction ≤ 35% should receive an ICD.
Zusammenfassung
Der plötzliche Herztod gehört zu den häufigsten Todesursachen in den industrialisierten Ländern. Die linksventrikuläre Auswurffraktion ist der wichtigste unabhängige Prädiktor für die Gesamtmortalität und den plötzlichen Herztod bei Patienten mit ischämischer und nicht-ischämischer Kardiomyopathie. Seit der Einführung des ICD (implantable cardioverter defibrillator) wurden mehrere Studien durchgeführt, um die Effektivität des ICD im Hinblick auf die Prävention des plötzlichen Herztodes zu untersuchen. Für den Kardiologen ist es nun wichtig, dass mittels dieser Studien Prädiktoren erarbeitet werden, die ihm helfen, das individuelle Risiko eines einzelnen Patienten abzuschätzen, damit die Indikation zur ICD-Implantation möglichst effektiv gestellt werden kann. Diese Übersichtsarbeit diskutiert, ob alle Patienten mit einer LV-EF unter 35% einen ICD brauchen.
Einleitung
Der plötzliche Herztod gehört zu den häufigsten Todesursachen in den industrialisierten Ländern und ist definiert als natürlicher Tod kardialer Ursache, der bedingt ist durch einenplötzlichen Herzstillstand innerhalb einer Stunde nach Beginn der akuten Symptomatik [1,2]. In den USA beträgt die Inzidenz für einen plötzlichen Herztod in der Population von über 35jährigen 0,1–0,2% pro Jahr. Eine vorbestehende Herzerkrankung kann zum Zeitpunkt des plötzlichen Herztodes erkannt worden sein, wobei die koronare Herzkrankheit die häufigste Ursache des plötzlichen Herztodes darstellt [2]. Die linksventrikuläre Auswurffraktion (LV-EF) ist der wichtigste unabhängige Prädiktor sowohl für die Gesamtmortalität als auch für den plötzlichen Herztod bei Patienten mit ischämischer und nichtischämischer Kardiomyopathie [3]. Seit den 1970er Jahren hat die Mortalität wegen Pumpversagen bei Herzinsuffizienz (bessere Behandlungsmethoden mit ACE-Hemmer, Betablocker usw.) deutlich abgenommen, hingegen ist die Mortalitätsabnahme an plötzlichem Herztod in der gleichen Zeitperiode deutlich weniger ausgeprägt [4]. Mehrere Studien haben gezeigt, dass Betablocker die Mortalität (auch des plötzlichen Herztodes) bei Patienten mit Herzinsuffizienz deutlich reduzieren [5,6,7]. Seit der Einführung der ICD (implantable cardioverter defibrillator)-Therapie wurden mehrere Studien durchgeführt, um die Effektivität des ICD im Hinblick auf die Prävention des plötzlichen Herztodes zu untersuchen. Dabei muss unterschieden werden zwischen Primär- (kein arrhythmisches Ereignis) und Sekundärpräventionsstudien (Patienten nach einem arrhythmischen Ereignis) sowie Studien bei ischämischer bzw. nicht-ischämischer Kardiomyopathie. Für den Kardiologen ist es nun wichtig, dass mittels dieser Studien Prädiktoren erarbeitet werden, die ihm helfen, das individuelle Risiko eines einzelnen Patienten abzuschätzen, damit die Indikation zur ICD-Implantation möglichst effektiv gestellt werden kann. Auf der anderen Seite ist es wünschenswert, einen möglichst einfachen Parameter zu haben, der die Indikation zur ICD-Implantation definiert, wobei ein einzelner Parameter (wie die LV-EF) eine gewisse Gefahr der Ungenauigkeit und mässigen Reproduzierbarkeit in sich birgt. Aufgrund der aktuellen Studienlage stellt sich zum aktuellen Zeitpunkt die Frage, ob alle Patienten mit einer LV-EF unter 35% einen ICD brauchen.
Sekundärprophylaxe des Plötzlichen Herztodes Mittels ICD
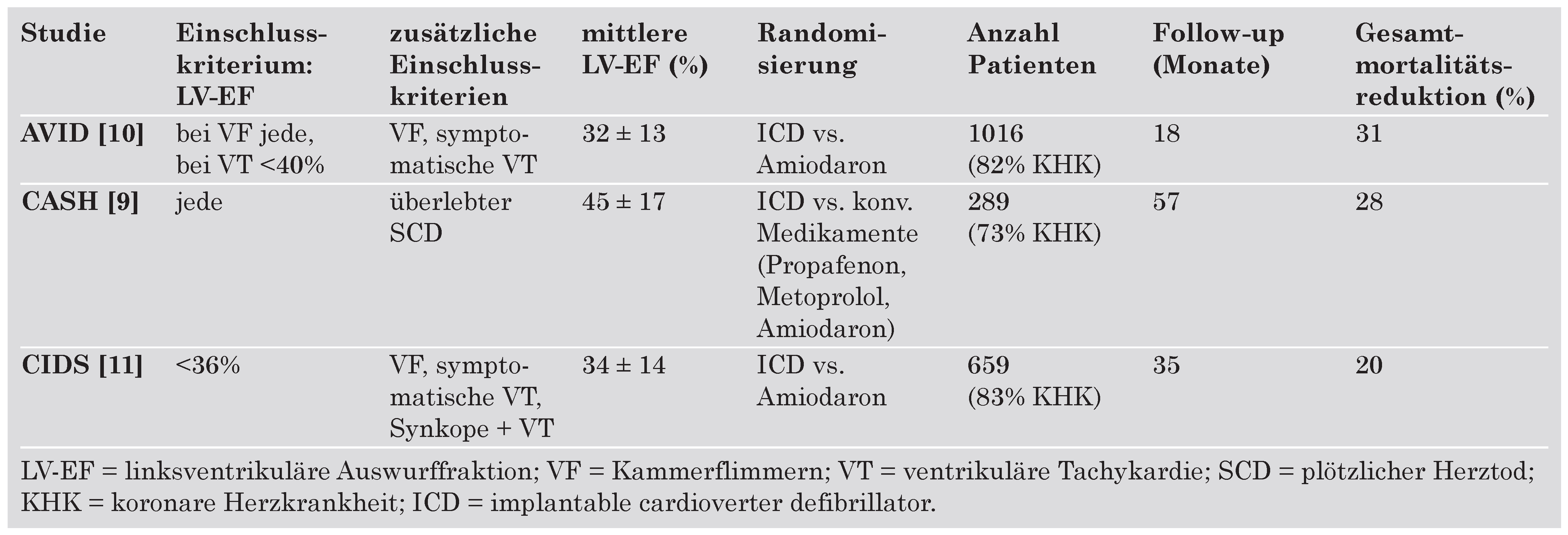
Die ersten ICD-Studien wurden an Patienten nach überlebtem Herzstillstand (infolge Kammerflimmern) und bei Patienten mit hämodynamisch instabilen Kammertachykardien durchgeführt (Table 1) [8,9,10,11]. In der Metaanalyse der drei Sekundärpräventionsstudien, bei der die gepoolten Daten von ca. 900 Patienten ausgewertet wurden, zeigte sich eine 27prozentige Reduktion der Gesamtmortalität durch die ICD-Therapie, unabhängig von der zugrunde liegenden Herzerkrankung oder Arrhythmie [12]. Eine Subanalyse zeigte, dass Patienten mit einer LV-EF unter 35% vom ICD bezüglich Mortalität profitierten und Patienten mit einer Auswurffraktion über 35% kein zusätzliches Benefiz von einer ICD-Therapie hatten [8].

Table 1.
ICD-Sekundärpräventionsstudien.
Bei etwa 10% der wegen Kammerflimmern reanimierten jungen Patienten kann keine zugrunde liegende Ursache trotz ausgedehnten Untersuchungen gefunden werden. Die Prognose bei diesen Patienten ist unsicher, weshalb heute auch bei Patienten mit normaler EF nach einem dokumentierten Kammerflimmern ohne reversible Ursache eine ICDImplantation empfohlen wird.
Primärprophylaxe des Plötzlichen Herztodes Mittels ICD
- Ischämische Herzkrankheit
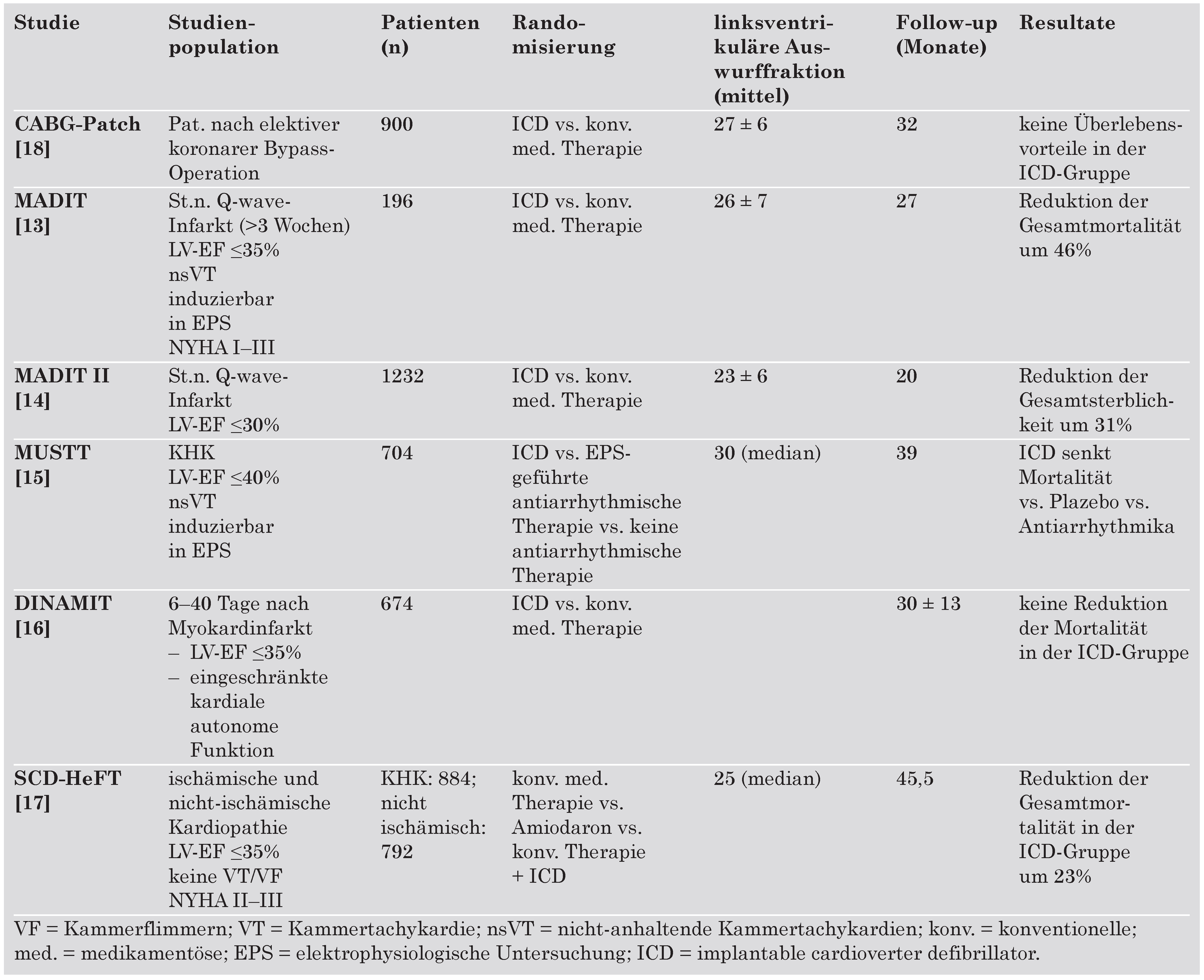
Verschiedene Studien haben die Wirksamkeit des ICD in der Primärprophylaxe des plötzlichen Herztodes bei Patienten mit koronarer Herzkrankheit untersucht (Table 2) [13,14,15,16,17].

Table 2.
ICD-Primärpräventionsstudien bei koronarer Herzkrankheit.
- Patienten mit koronarer Herzkrankheit mit St. n. Myokardinfarkt und eingeschränkter linksventrikulärer Auswurffraktion
MADIT (Multicenter Automatic Defibrillator Implantation Trial; n = 196) und MADIT II (Multicenter Automatic Defibrillator Implantation Trial II; n = 1232), zwei prospektive, randomisierte Studien, verglichen den Gebrauch eines ICD im Vergleich zur konventionellen medikamentösen Behandlung [13,14]. Beide Studien untersuchten Patienten mit koronarer Herzkrankheit nach Myokardinfarkt mit eingeschränkter LV-EF. Die Unterschiede in der Patientenselektion sind in Tabelle 3 aufgeführt. Beide Studien zeigten eine signifikante Reduktion der Gesamtmortalität unter ICD-Behandlung. In MADIT mussten 4,6 Patienten mit einem ICD behandelt werden, um einen plötzlichen Herztod zu verhindern (= number-needed-to-treat [NNT]; mittleres Follow-up 27 Monate). In MADIT II war die NNT 17,9 (mittleres Follow-up 20 Monate; absolute Risikoreduktion von 5,6%). Insgesamt liefern diese beiden Studien Evidenz, dass Patienten mit koronarer Herzkrankheit, St. n. Myokardinfarkt (älter als 1 Monat) und eingeschränkter LV-EF, die die Einschlusskriterien einer der beiden Studien erfüllen, eine signifikant verminderte Mortalität aufweisen, wenn zusätzlich zur optimalen medikamentösen Therapie ein ICD implantiert wurde. Neben der Einschränkung der LV-EF scheint bei der ischämischen Kardiomyopathie die Induzierbarkeit von ventrikulären Tachykardien in der elektrophysiologischen Untersuchung ein relativ guter Parameter zur Risikostratifizierung zu sein. So konnte bei ischämischer Kardiomyopathie bei MADIT im Vergleich zu MADIT II (Table 3) mittels Bestimmung der Induzierbarkeit die NNT reduziert werden [13,14].

Table 3.
Unterschiede zwischen MADIT und MADIT II in der Patientenselektion.

Table 4.
ICD-Primärpräventionsstudien bei nicht-ischämischer Kardiomyopathie.
Die zwei randomisierten Studien MUSTT (Multicenter Unsustained Tachycardia Trial) und CABG Patch (Coronary Artery Bypass Graft Patch Trial) schlossen Patienten mit koronarer Herzkrankheit ein, jedoch war ein früherer Myokardinfarkt als Einschlusskriterium nicht zwingend notwendig [15,18]. Effektiv aber hatte die Mehrheit einen früheren Myokardinfarkt, so dass diese Resultate auf diese Patientenpopulation angewendet werden können. MUSTT schloss 704 Patienten ein, davon hatten 94% einen früheren Myokardinfarkt (der Einschluss erfolgte frühesten 4 Tage nach Myokardinfarkt), CABG-Patch schloss 900 Patienten ein, 83% hatten einen früheren Myokardinfarkt.
MUSTT schloss Patienten mit koronarer Herzkrankheit, eingeschränkter linksventrikulärer Auswurffraktion und spontanen nicht anhaltenden ventrikulären Tachykardien ein. Die Patienten mussten zudem induzierbare ventrikuläre Tachykardien in der elektrophysiologischen Untersuchung haben. Die Patienten wurden in zwei Gruppen randomisiert: medikamentöse antiarrhythmische Therapie vs. Plazebo. Nicht induzierbare Patienten wurden in einem Register geführt. Bei Patienten der Antiarrhythmika-Gruppe konnte bei Versagen mindestens eines Antiarrhythmikums ein ICD implantiert werden. 46% dieser Patienten erhielten einen ICD. Der Endpunkt, Herzstillstand oder Tod durch Arrhythmie, war verglichen mit keiner antiarrhythmischen Therapie in der EPS-geführten Therapie-Gruppe nach 5 Jahren signifikant tiefer (relative Risikoreduktion von 27%). Die NNT betrug in der EPS-geführten Therapie-Gruppe 14,3 Patienten, um einen Patienten über 5 Jahre vor einem Herzstillstand oder einem Tod durch Arrhythmie zu bewahren. Der deutlichere Vorteil der ICD-Therapie bei dieser Studie liegt an einer Selektion von Patienten mit erhöhtem Mortalitätsrisiko (Mortalität der Kontrollgruppe vs. Madit II).
Der CABG-Patch-Trial schloss Patienten ein, die einer Bypass-Operation unterzogen wurden, eine LV-EF ≤35% und ein pathologisches signalgemitteltes EKG hatten. Die Patienten wurden randomisiert in eine Gruppe mit ICD und eine Gruppe ohne ICD. In der Nachbeobachtungszeit von 32 Monaten zeigte sich kein Vorteil durch den ICD bezüglich der Gesamtmortalität.
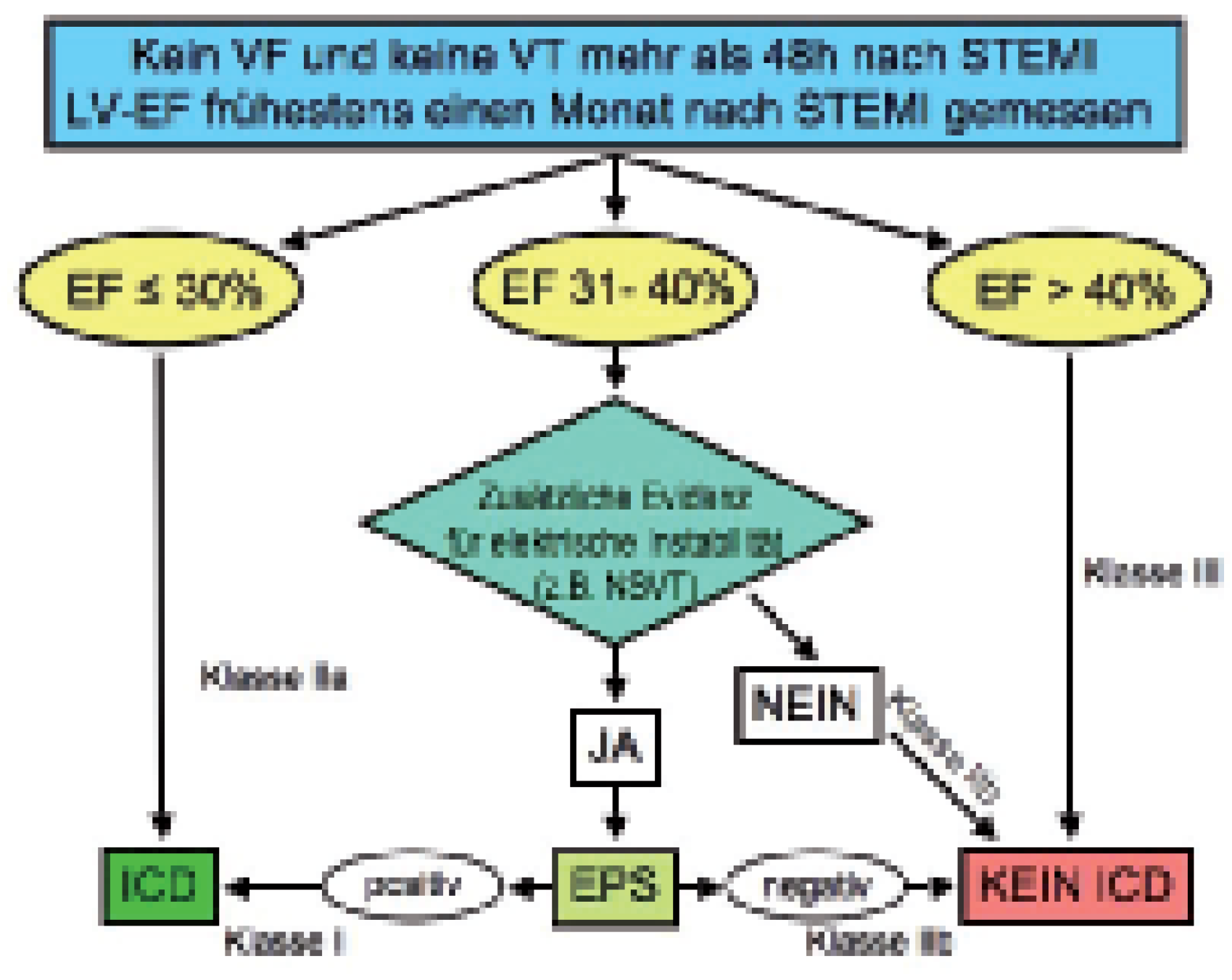
In der SCD-HeFT-Studie (Sudden Cardiac Death in Heart Failure Trial) wurden 1310 Patienten mit ischämischer (52%) und 1211 mit nicht-ischämischer (48%) Kardiopathie mit einer EF ≤35% eingeschlossen [17]. Die ischämische Kardiopathie wurde folgendermassen definiert: linksventrikuläre systolische Dysfunktion, die von mindestens einer signifikanten (<75%) Stenose einer der 3 Koronararterien begleitet war oder dokumentierter früherer Myokardinfarkt. Eine nicht-ischämische Kardiopathie war definiert als systolische Dysfunktion ohne signifikante Koronarstenosen. Die mediane LV-EF betrug 25%. Die Patienten wurden in 3 Gruppen randomisiert: Amiodaron, Plazebo oder ICD. Insgesamt zeigte sich unter Amiodaron keine Reduktion der Mortalität im Vergleich zu Plazebo, jedoch kam es in der ICD-Gruppe zu einer signifikanten relativen Mortalitätsreduktion um 23% bei einem medianen Follow-up von 45,5 Monaten (absolute Risikoreduktion 6,8%, NNT = 13,9). Die Studie zeigte zwar insgesamt einen Vorteil für die ICD-Gruppe, die Subgruppenanalyse konnte aber sowohl für die Patienten mit ischämischer Kardiopathie (p = 0,05, aber CI >1) als auch für die Patienten ohne ischämische Kardiopathie (p = 0,06, CI >1) keinen signifikanten Benefit zeigen. Es profitierten Patienten mit deutlich eingeschränkter LV-EF (<30%), bei Patienten mit einer EF über 30% konnte kein Nutzen gezeigt werden. Zudem konnte in der Subgruppenanalyse für folgende Subgruppen ein Vorteil durch die ICD-Therapie gezeigt werden: NYHA-Klasse II, Alter <65 Jahre und QRS-Dauer über 120 ms. Deshalb stellt sich die Frage, ob die Grenze für die ICD Indikation ähnlich wie bei MADIT II bei einer LV-EF von 30% festgesetzt werden sollte. Auch in den ACC/AHA-Guidelines wurden Patienten nach Myokardinfarkt mit einer LV-EF zwischen 30 und 40% als Grenzbereich deklariert. Figure 1 zeigt einen evidenzbasierten Algorithmus für die Primärprävention des plötzlichen Herztodes bei Postinfarktpatienten ohne spontanes Kammerflimmern oder anhaltende Kammertachykardien mindestens einen Monat nach Myokardinfarkt [19].
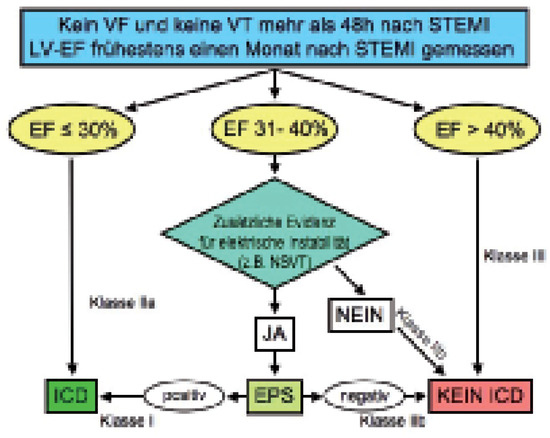
Figure 1.
Evidenz-basierter Algorithmus für die Primärprävention des plötzlichen Herztodes bei Postinfarktpatienten ohne spontanes Kammer-flimmern (VF) oder anhaltende Kammertachykardien (VT,) mindestens ein Monat nach ST-Hebungs-Myokardinfarkt (STEMI). NSVT = nicht-anhaltende Kammertachykardien; EF = Ejektionsfraktion; EPS = elektrophysiologische Untersuchung; ICD = implantable cardioverter defibrillator. Adaptiert nach [19].
- Patienten mit koronarer Herzkrankheit mit akutem Herzinfarkt und eingeschränkter linksventrikulärer Auswurffraktion
Die DINAMIT-Studie untersuchte Patienten, bei denen 6–40 Tage nach akutem Myokardinfarkt eine eingeschränkte LV-EF (≤35%) und eine pathologisch verminderte Herzfrequenzvariabilität bzw. erhöhte Herzfrequenz festgestellt wurde [16]. Die 674 Patienten wurden randomisiert in eine ICD-Gruppe und eine Gruppe, der kein ICD implantiert wurde. Die prophylaktische ICD-Implantation nach akutem Myokardinfarkt zeigte keine Reduktion der Gesamtmortalität bei diesen Hochrisiko-Patienten.
Somit kann eine routinemässige ICD-Implantation nicht für alle Patienten mit eingeschränkter LV-EF nach akutem oder kürzlichem Myokardinfarkt empfohlen werden.
- Nicht-ischämische Herzkrankheit
Verschiedene Primärpräventionsstudien haben Patienten mit nicht-ischämischer Kardiopathie untersucht.
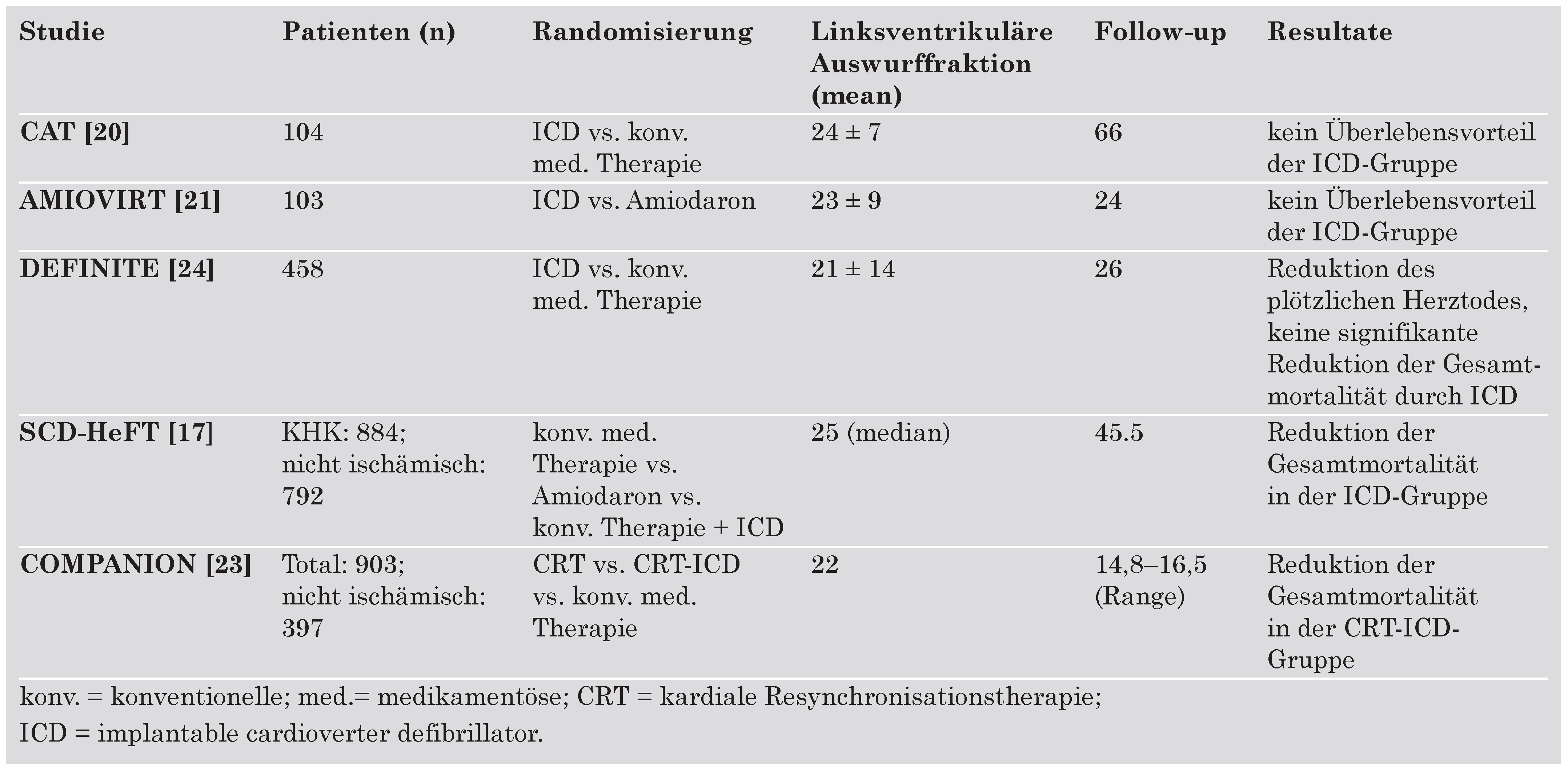
In der CAT-Studie (Cardiomyopathie Arrhythmia Trial) wurden Patienten mit dilatativer Kardiomyopathie (LV-EF ≤30%) seit 9 oder weniger Monaten mit NYHA II oder III eingeschlossen [20]. Sie wurden in 2 Gruppen randomisiert (ICD vs. konventionelle Therapie). Der Einschluss von Patienten wurde nach 104 Patienten beendet, da die Gesamtmortalität nach einem Jahr, die erwarteten 30% in der Kontrollgruppe, nicht erreicht wurde. Nach 2, 4 und 6 Jahren wurden keine Mortalitätsunterschiede zwischen den beiden Gruppen gefunden. Somit ergab diese Studie keine Evidenz für eine prophylaktische ICD-Implantation bei Patienten mit neu aufgetretener dilatativer Kardiomyopathie und eingeschränkter linksventrikulärer Auswurffraktion.
In der AMIOVIRT-Studie wurden 200 Patienten mit dilatativer Kardiomyopathie, nichtanhaltenden Kammertachykardien und linksventrikulärer Auswurffraktion ≤35% eingeschlossen [21]. Es zeigten sich keine Mortalitätsunterschiede zwischen ICD-Patienten und solchen, die mit Amiodaron behandelt wurden. Das fehlende Benefiz der ICD-Gruppe ist möglicherweise der relativ kleinen Patientenzahl zuzuschreiben.
In der DEFINITE-Studie wurden 458 Patienten mit dilatativer Kardiomyopathie und einer LV-EF ≤35%, symptomatischer Herzinsuffizienz und komplexen ventrikulären Extrasystolien (>10 ventrikuläre Extrasystolen pro Stunde oder nicht anhaltende ventrikuläre Tachykardien) eingeschlossen. Die Patienten wurden in eine ICD-Gruppe und eine Kontrollgruppe randomisiert. Die Mehrheit der Patienten (kein Unterschied zwischen den Gruppen) wurde mit ACE-Hemmern (85,6%), Diuretika (86,7%) und mit Betablockern (84,9%) behandelt. In der ICD-Gruppe zeigte sich eine signifikante Reduktion des plötzlichen Herztodes durch Arrhythmie (sekundärer Endpunkt), jedoch nicht bei der Reduktion der Gesamtmortalität (primärer Endpunkt, p = 0,08; Follow-up 29 Monate, Hazard Ratio für Mortalität 0,65 (0,4–1,06), absolutes Mortalitätsbenefiz 5,3%, NNT = 18,9).
In SCD-HeFT wurden neben KHK-Patienten auch solche mit dilatativer Kardiomyopathie eingeschlossen [17]. Die Studie zeigte eine 27prozentige relative Mortalitätsreduktion bei Patienten mit nicht-ischämischer Kardiomyopathie (absolute Risikoreduktion 6,5%, NNT = 15,4) [22].
Die Resultate von DEFINITE (NNT = 18,9) und SCD-HeFT (NNT = 15,4) sind weitgehend konsistent und weisen darauf hin, dass die Implantation eines ICD die Überlebensraten bei Patienten mit nicht-ischämischer Kardiomyopathie und schwerer linksventrikulärer Dysfunktion verbessert.
Desai et al. haben diese fünf Studien [17,20,21,23,24] in einer Metaanlyse analysiert [25]. Die Metaanalyse von 1854 Patienten mit nicht-ischämischer Kardiomyopathie zeigte eine signifikante 31prozentige Reduktion der Gesamtmortalität bei Patienten mit ICD im Vergleich zu Patienten unter rein medikamentöser Therapie. In einer Sensitivitätsanalyse schlossen die Autoren die COMPANION-Studie aus, da diese Studie eine Population mit fortgeschrittener Herzinsuffizienz unter biventrikulärem Pacing eingeschlossen hatte. Der signifikante Unterschied der Metaanalyse blieb auch nach Ausschluss der COMPANION-Studie bestehen.
Die obengenannten Studien schlossen zum grössten Teil Patienten mit nicht-ischämischer dilatativer Kardiomyopathie ein. Deshalb sollte man die übrigen Kardiomyopathien gesondert betrachten:
Wichter et al. haben den Nutzen des ICD bei der arrhythmogenen rechts-ventrikulären Kardiomyopathie (ARVC) untersucht [26]. Nur 32% der 60 in die Studie eingeschlossenen Patienten wiesen eine linksventrikuläre Beteiligung auf, die mittlere LV-EF betrug 66%. Die Studie zeigte eine signifikante Verbesserung der Langzeitprognose bei Patienten mit ARVC, jedoch erhielten nur 7% der Patienten den ICD zur Primärprävention. Somit muss bei Patienten mit ARVC die Indikation zur ICD-Implantation im Sinne einer Primärprophylaxe weiterhin nach individueller Risikostratifizierung und dem Ermessen des behandelnden Arztes und den Präferenzen des Patienten gestellt werden [27,28]. Gleich wie bei den Patienten mit ARVC darf auch bei Patienten mit hypertropher Kardiomyopathie die Indikation für einen ICD nicht von der LV-EF abhängig gemacht werden. Die Sekundärprävention mittels ICD hat sich bei Patienten mit hypertropher Kardiomyopathie als effektiv erwiesen, noch nicht klar ist die Situation bei der Primärprävention [29].
- Patienten mit fortgeschrittener Herzinsuffizienz
Bei Patienten mit dilatiertem linken Ventrikel und schwer eingeschränkter linksventrikulärer Funktion besteht häufig eine schwere Einschränkung der körperlichen Leitungsfähigkeit mit Dyspnoe NYHA III oder IV. Bei diesen Patienten kann man eine dyssynchrone linksventrikuläre Kontraktion beobachten, so dass eine Resynchronisationstherapie mittels biventrikulärem Pacing eine Verbesserung der Herzinsuffizienzsymptome bewirken kann. Die COMPANION-Studie hat untersucht, ob bei Patienten mit fortgeschrittener Herzinsuffizienz und einer QRS-Intervall-Verlängerung eine Resynchronisationstherapie ohne und mit einem ICD zu einer Reduktion des Risikos für Tod und Hospitalisation führt [23]. Es wurden 1520 Patienten mit fortgeschrittener Herzinsuffizienz (NYHA III oder IV, mittlere LV-EF = 22%) als Folge einer ischämischen oder nicht-ischämischen Kardiomyopathie eingeschlossen. Die Resynchronisationstherapie allein reduzierte das Risiko für den kombinierten Endpunkt Tod oder Hospitalisation wegen Herzinsuffizienz und wenn die Resynchronisationstherapie mit einem ICD kombiniert war, so wurde auch die Mortalität signifikant reduziert. Folglich muss man bei Patienten mit schwerer Herzinsuffizienz nicht nur eine ICD-Therapie, sondern auch eine Resynchronisationstherapie evaluieren.
Konklusion
Insgesamt weist die aktuelle Studienlage darauf hin, dass bei Patienten mit einer eingeschränkten LV-EF (unabhängig von der Ätiologie) sowohl in der Sekundär- als auch in der Primärprophylaxe eine Reduktion der Gesamtmortalität durch eine ICD-Implantation erreicht werden kann. Jedoch handelt es sich bei der ICD-Therapie um eine relativ teure Behandlung, weshalb eine noch genauere Risikostratifizierung, die zu einer Reduktion der NNT führen würde, wünschenswert wäre. Man sollte sich dabei bewusst sein, dass die NNT nicht linear mit der Zeit verläuft: Das Benefiz nach ICD-Implantation (gemessen in gewonnenen Lebensjahren) nimmt mit der Zeit zu, nach den ersten 3 Jahre nach Implantation sogar im Quadrat mit der Zeit [30]. Wenn ein Patient gleichzeitig zur Herzinsuffizienz auch ein Linksschenkelblock hat, einen sehr langen AV-Block I oder echokardiographische Zeichen der intraventrikulären Dyssynchronie, bietet sich eine Resynchronisationstherapie mit der Implantation des ICD an, welches dann über mehrere Mechanismen den Krankheitsverlauf und die Mortalität beeinflusst.
References
- Zipes, D.P.; Wellens, H.J. Sudden cardiac death. Circulation 1998, 98, 2334–2351. [Google Scholar] [CrossRef] [PubMed]
- Myerburg, R.J.; Castellanos, A. Emerging paradigms of the epidemiology and demographics of sudden cardiac arrest. Heart Rhythm. 2006, 3, 235–239. [Google Scholar] [CrossRef] [PubMed]
- Stevenson, W.G.; Stevenson, L.W.; Middlekauff, H.R.; Saxon, L.A. Sudden death prevention in patients with advanced ventricular dysfunction. Circulation 1993, 88, 2953–2961. [Google Scholar] [CrossRef] [PubMed]
- Fox, C.S.; Evans, J.C.; Larson, M.G.; Kannel, W.B.; Levy, D. Temporal trends in coronary heart disease mortality and sudden cardiac death from 1950 to 1999: The Framingham Heart Study. Circulation 2004, 110, 522–527. [Google Scholar]
- The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II): A randomised trial. Lancet 1999, 353, 9–13. [CrossRef]
- Packer, M.; Fowler, M.B.; Roecker, E.B.; Coats, A.J.; Katus, H.A.; Krum, H.; et al. Effect of carvedilol on the morbidity of patients with severe chronic heart failure: Results of the carvedilol prospective randomized cumulative survival (COPERNICUS) study. Circulation 2002, 106, 2194–2199. [Google Scholar] [CrossRef]
- Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet 1999, 353, 2001–2007. [CrossRef]
- Sheldon, R.; Connolly, S.; Krahn, A.; Roberts, R.; Gent, M.; Gardner, M. Identification of patients most likely to benefit from implantable cardioverter-defibrillator therapy: The Canadian Implantable Defibrillator Study. Circulation 2000, 101, 1660–1664. [Google Scholar] [CrossRef]
- Kuck, K.H.; Cappato, R.; Siebels, J.; Ruppel, R. Randomized comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest: The Cardiac Arrest Study Hamburg (CASH). Circulation 2000, 102, 748–754. [Google Scholar] [CrossRef]
- A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias. The Antiarrhythmics versus Implantable Defibrillators (AVID) Investigators. N Engl J Med. 1997, 337, 1576–1583. [CrossRef]
- Connolly, S.J.; Gent, M.; Roberts, R.S.; Dorian, P.; Roy, D.; Sheldon, R.S.; et al. Canadian implantable defibrillator study (CIDS): A randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000, 101, 1297–1302. [Google Scholar] [CrossRef]
- Connolly, S.J.; Hallstrom, A.P.; Cappato, R.; Schron, E.B.; Kuck, K.H.; Zipes, D.P.; et al. Meta-analysis of the implantable cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs Implantable Defibrillator study. Cardiac Arrest Study Hamburg. Canadian Implantable Defibrillator Study. Eur Heart J. 2000, 21, 2071–2078. [Google Scholar] [CrossRef] [PubMed]
- Moss, A.J.; Hall, W.J.; Cannom, D.S.; Daubert, J.P.; Higgins, S.L.; Klein, H.; et al. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med. 1996, 335, 1933–1940. [Google Scholar] [CrossRef] [PubMed]
- Moss, A.J.; Zareba, W.; Hall, W.J.; Klein, H.; Wilber, D.J.; Cannom, D.S.; et al. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med. 2002, 346, 877–883. [Google Scholar] [CrossRef] [PubMed]
- Buxton, A.E.; Lee, K.L.; DiCarlo, L.; Gold, M.R.; Greer, G.S.; Prystowsky, E.N.; et al. Electrophysiologic testing to identify patients with coronary artery disease who are at risk for sudden death. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med. 2000, 342, 1937–1945. [Google Scholar] [CrossRef]
- Hohnloser, S.H.; Kuck, K.H.; Dorian, P.; Roberts, R.S.; Hampton, J.R.; Hatala, R.; et al. Prophylactic use of an implantable cardioverter-defibrillator after acute myocardial infarction. N Engl J Med. 2004, 351, 2481–2488. [Google Scholar]
- Bardy, G.H.; Lee, K.L.; Mark, D.B.; Poole, J.E.; Packer, D.L.; Boineau, R.; et al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med. 2005, 352, 225–237. [Google Scholar] [CrossRef]
- Bigger, J.T., Jr. Prophylactic use of implanted cardiac defibrillators in patients at high risk for ventricular arrhythmias after coronary-artery bypass graft surgery. Coronary Artery Bypass Graft (CABG) Patch Trial Investigators. N Engl J Med. 1997, 337, 1569–1575. [Google Scholar] [CrossRef]
- Antman, E.M.; Anbe, D.T.; Armstrong, P.W.; Bates, E.R.; Green, L.A.; Hand, M.; et al. ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction: A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Revise the 1999 Guidelines for the Management of Patients with Acute Myocardial Infarction). Circulation 2004, 110, 282–292. [Google Scholar]
- Bansch, D.; Antz, M.; Boczor, S.; Volkmer, M.; Tebbenjohanns, J.; Seidl, K.; et al. Primary prevention of sudden cardiac death in idiopathic dilated cardiomyopathy: The Cardiomyopathy Trial (CAT). Circulation 2002, 105, 1453–1458. [Google Scholar]
- Strickberger, S.A.; Hummel, J.D.; Bartlett, T.G.; Frumin, H.I.; Schuger, C.D.; Beau, S.L.; et al. Amiodarone versus implantable cardioverter-defibrillator: Randomized trial in patients with nonischemic dilated cardiomyopathy and asymptomatic nonsustained ventricular tachycardia—AMIOVIRT. J Am Coll Cardiol. 2003, 41, 1707–1712. [Google Scholar] [CrossRef] [PubMed]
- Kadish, A. Prophylactic defibrillator implantation—Toward an evidence-based approach. N Engl J Med. 2005, 352, 285–287. [Google Scholar] [CrossRef] [PubMed][Green Version]
- Bristow, M.R.; Saxon, L.A.; Boehmer, J.; Krueger, S.; Kass, D.A.; De Marco, T.; et al. Cardiac-resynchronization therapy with or without an implantable defibrillator in advanced chronic heart failure. N Engl J Med. 2004, 350, 2140–2150. [Google Scholar] [CrossRef] [PubMed]
- Kadish, A.; Dyer, A.; Daubert, J.P.; Quigg, R.; Estes, N.A.; Anderson, K.P.; et al. Prophylactic defibrillator implantation in patients with nonischemic dilated cardiomyopathy. N Engl J Med. 2004, 350, 2151–2158. [Google Scholar] [CrossRef]
- Desai, A.S.; Fang, J.C.; Maisel, W.H.; Baughman, K.L. Implantable defibrillators for the prevention of mortality in patients with nonischemic cardiomyopathy: A meta-analysis of randomized controlled trials. JAMA 2004, 292, 2874–2879. [Google Scholar] [CrossRef]
- Wichter, T.; Paul, M.; Wollmann, C.; Acil, T.; Gerdes, P.; Ashraf, O.; et al. Implantable cardioverter/defibrillator therapy in arrhythmogenic right ventricular cardiomyopathy: Single-center experience of long-term follow-up and complications in 60 patients. Circulation 2004, 109, 1503–1508. [Google Scholar] [CrossRef]
- Prakasa, K.R.; Calkins, H. Arrhythmogenic right ventricular dysplasia/cardiomyopathy. Curr Treat Options Cardiovasc Med. 2005, 7, 467–475. [Google Scholar] [CrossRef]
- Hodgkinson, K.A.; Parfrey, P.S.; Bassett, A.S.; Kupprion, C.; Drenckhahn, J.; Norman, M.W.; et al. The impact of implantable cardioverter-defibrillator therapy on survival in autosomal-dominant arrhythmogenic right ventricular cardiomyopathy (ARVD5). J Am Coll Cardiol. 2005, 45, 400–408. [Google Scholar] [CrossRef]
- Begley, D.A.; Mohiddin, S.A.; Tripodi, D.; Winkler, J.B.; Fananapazir, L. Efficacy of implantable cardioverter defibrillator therapy for primary and secondary prevention of sudden cardiac death in hypertrophic cardiomyopathy. Pacing Clin Electrophysiol. 2003, 26, 1887–1896. [Google Scholar] [CrossRef]
- Salukhe, T.V.; Dimopoulos, K.; Sutton, R.; Coats, A.J.; Piepoli, M.; Francis, D.P. Life-years gained from defibrillator implantation: Markedly nonlinear increase during 3 years of follow-up and its implications. Circulation 2004, 109, 1848–1853. [Google Scholar] [CrossRef]
© 2006 by the author. Attribution - Non-Commercial - NoDerivatives 4.0.