Zusammenfassung
Die Behandlung sogenannter «Lifestyle»-Risikofaktoren wie Übergewicht und Rauchen ist schwierig. Diese beiden Risikofaktoren spielen in der kardiovaskulären Medizin eine grosse Rolle. Die assoziierten metabolischen Veränderungen (tiefes HDL-Cholesterin, InsulinResistenz) lassen sich mit den verfügbaren Medikamenten kaum beeinflussen. Rimonabant ist der erste Vertreter der Substanzgruppe der Cannabinoid-Rezeptor-Antagonisten und blockiert CB1-Rezeptoren. Klinische Studien zeigen die Wirksamkeit bei der Behandlung übergewichtiger Patienten. Die mit Rimonabant erzielte Gewichtsreduktion in den einzelnen Studien liegt konsistent bei etwa 7 kg. Über den bisher untersuchten maximalen Zeitraum von 2 Jahren bleibt die Gewichtsreduktion erhalten. Die erreichten Verbesserungen des Lipid-Profils mit der Zunahme des HDL-Cholesterins (um 25%) und Senkung von Entzündungsmarkern versprechen spannende Ergebnisse von Mortalitäts- und Morbiditäts-Studien mit Rimonabant. Rimonabant wurde ausserdem in Rauchentwöhnungsprogrammen erfolgreich getestet. In der Rauchentwöhnung waren nach 10 Wochen Behandlung mit Rimonabant fast doppelt so viele Patienten unter Rimonabant abstinent wie unter Plazebo (28% vs.16%). Dabei wurde eine Gewichtszunahme in der Rimonabant-Gruppe vermieden, während die Plazebo-Gruppe leicht zunahm.
Einleitung
Die Pharmakotherapie atherosklerotischer Erkrankungen hat grosse Fortschritte gemacht. Grosse klinische Studien haben den Nutzen von Statinen, ACE-Hemmern, Betablockern, Plättchen- und Gerinnungshemmern eindrücklich bewiesen. Die Behandlung sogenannter «Lifestyle»-Risikofaktoren wie Übergewicht und Rauchen ist hingegen weitaus schwieriger. Diese beiden Risikofaktoren spielen in der kardiovaskulären Medizin eine grosse Rolle (Abb. 1) [
1]. Die mit Übergewicht und Rauchen assoziierten metabolischen Veränderungen (tiefes HDL-Cholesterin, Insulin-Resistenz) lassen sich mit den verfügbaren Medikamenten kaum beeinflussen [
2].
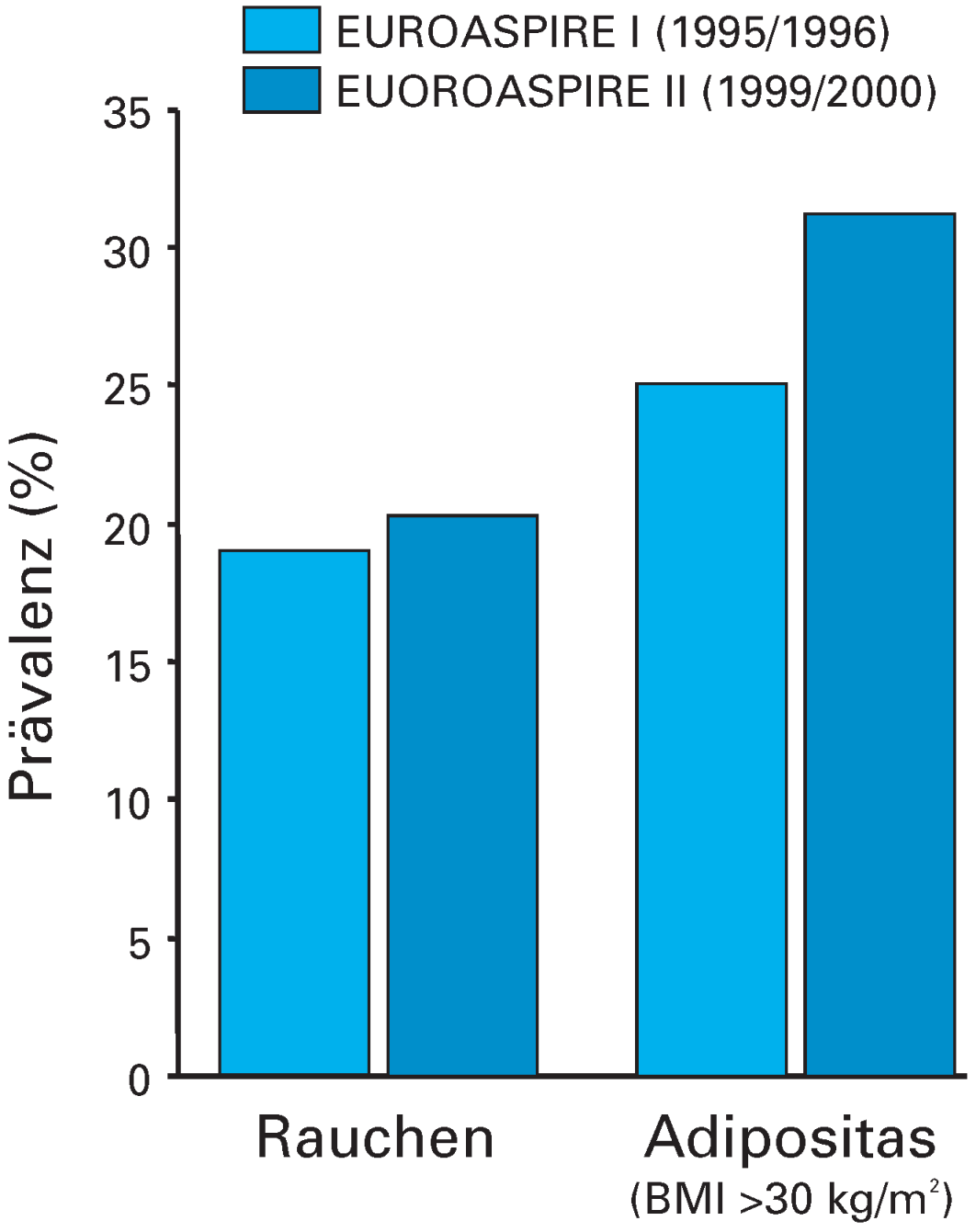
Abbildung 1.
Die Prävalenz der Risikofaktoren Rauchen und Adipositas bei Patienten mit koronarer Herzkrankheit hat in den letzten Jahren noch zugenommen. Aus EUROASPIRE I und II. Modifiziert nach [
1].
Abbildung 1.
Die Prävalenz der Risikofaktoren Rauchen und Adipositas bei Patienten mit koronarer Herzkrankheit hat in den letzten Jahren noch zugenommen. Aus EUROASPIRE I und II. Modifiziert nach [
1].
Nur wenige schaffen es ohne Unterstützung mit dem Rauchen aufzuhören. Rasch sind die guten Vorsätze wieder vergessen und die Zigarette wieder angesteckt. Ebenso mühsam ist der Kampf gegen überzählige Pfunde, die oft so rasch wieder zu- wie abgenommen sind. Die American Heart Association (AHA) empfiehlt in ihren Richtlinien zur Behandlung der Adipositas diätetische Interventionen mit Kalorien-reduzierter Ernährung, vermehrte körperliche Aktivität, Verhaltenstherapie sowie je nach Situation pharmakologische (bei einem Body Mass Index über 30 kg/m
2) und chirurgische Methoden (BMI >35 kg/m
2) [
3]. Regelmässige Konsultationen zur Verlaufskontrolle und Motivation mit dem Stecken erreichbarer Ziele sind notwendig. Ein Gewichtsverlust von ein bis zwei Pfund pro Woche wird empfohlen.
Ein Medikament, das gleichzeitig hilft, mit dem Rauchen aufzuhören, Gewicht zu reduzieren und ein metabolisches Syndrom zu behandeln, erscheint wie eine Wunderdroge. Dieser Artikel gibt einen Überblick über die Pharmakologie von Rimonabant, dem ersten Vertreter einer neuen Medikamentenklasse der Cannabinoid-Rezeptor-Antagonisten. Die Ergebnisse klinischer Studien mit Rimonabant werden vorgestellt.
Pharmakologie
Anders als bereits auf dem Markt verfügbare Substanzgruppen, wie Lipase-Hemmer (Orlistat) oder Serotonin-Noradrenalin-Wiederaufnahmehemmer (Sibutramin), entfaltet Rimonabant seine Wirkung durch spezifische Blockade des Cannabinoid-Rezeptors CB1.Rimonabant (SR 141716A) ist ein Pyrazol-Derivat (Abb. 2).
Das endogene Cannabinoid-System
Cannabinoid-Rezeptoren
Es existieren zwei Cannabinoid-RezeptorSubtypen: CB
1 und CB
2 [
4]. Der CB
1-Rezeptor mit sieben Transmembran-Regionen ist bei vielen Spezies konstant und weist eine bemerkenswerte phylogenetische Konservierung in der Evolution auf. Das CB
1-Gen wurde beim Menschen auf dem Chromosom 6 in der Region 6q14–q15 lokalisiert, der CB
2-Rezeptor wird von 1p36 codiert. Der CB
2-Rezeptor findet sich vor allem auf Immunzellen. Beim Menschen weisen die Transmembran-Regionen der beiden Subtypen Ähnlichkeit auf.
Der CB
1-Rezeptor bewirkt eine G
i-Proteinvermittelte Aktivierung der Mitogen-aktivierten Proteinkinase (MAPK), die von Insulin und Insulin-like Growth Factor (IGF1) stimuliert wird [
4]. Rimonabant blockiert diese Aktivierung [
5]. Man geht von einem Modell von drei Rezeptor-Zuständen aus, wobei Rimonabant einen Suppressor-Zustand des autoaktivierten Rezeptors induziert mit GDP-gekoppeltem G
i-Protein.
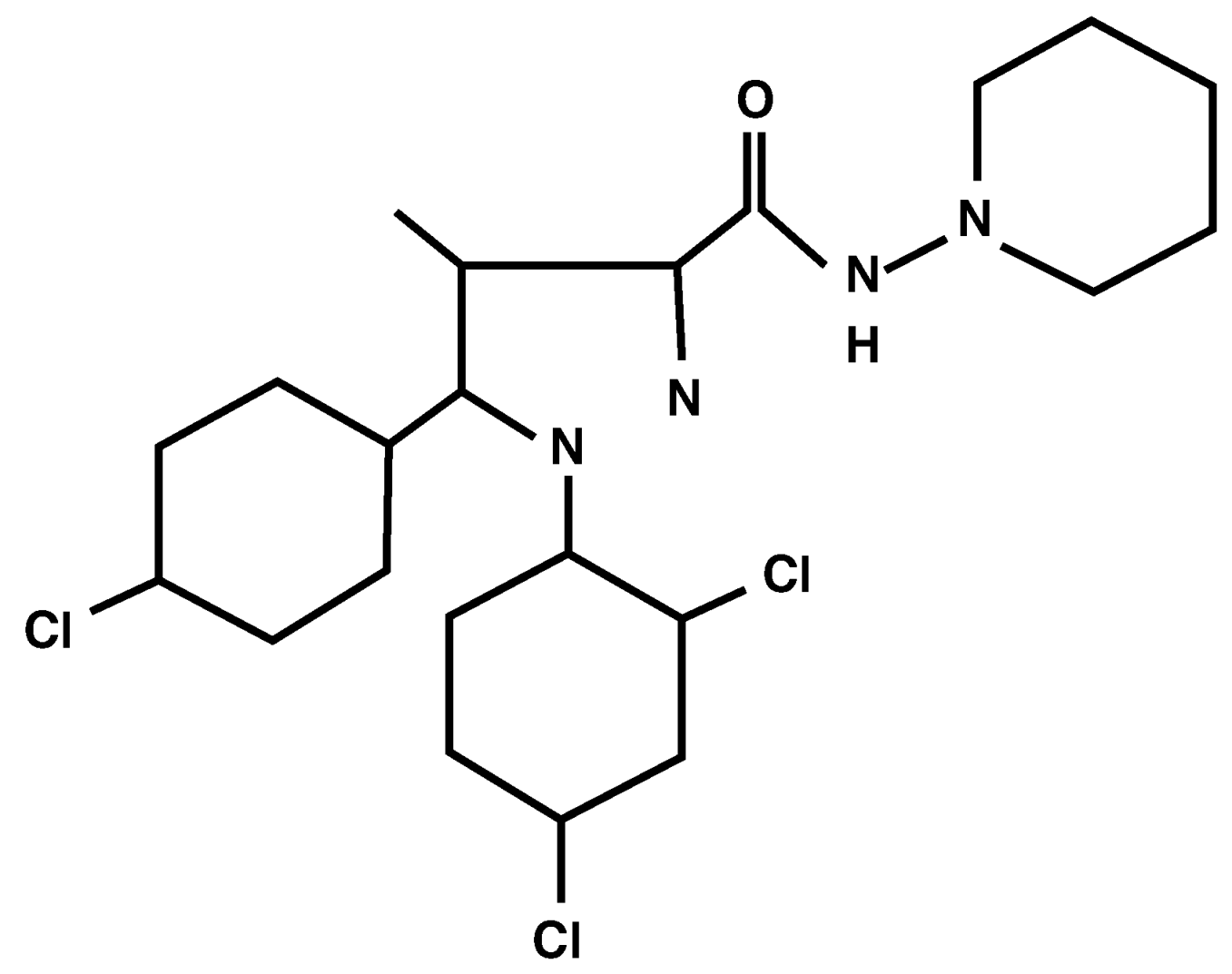
Abbildung 2.
Chemische Struktur von Rimonabant (SR 141716A), einem Cannabinoid-Rezeptor(CB)-Antagonisten. Rimonabant, ein Pyrazol-Derivat, blockiert selektiv CB
1-Rezeptoren. Modifiziert nach [
4].
Abbildung 2.
Chemische Struktur von Rimonabant (SR 141716A), einem Cannabinoid-Rezeptor(CB)-Antagonisten. Rimonabant, ein Pyrazol-Derivat, blockiert selektiv CB
1-Rezeptoren. Modifiziert nach [
4].
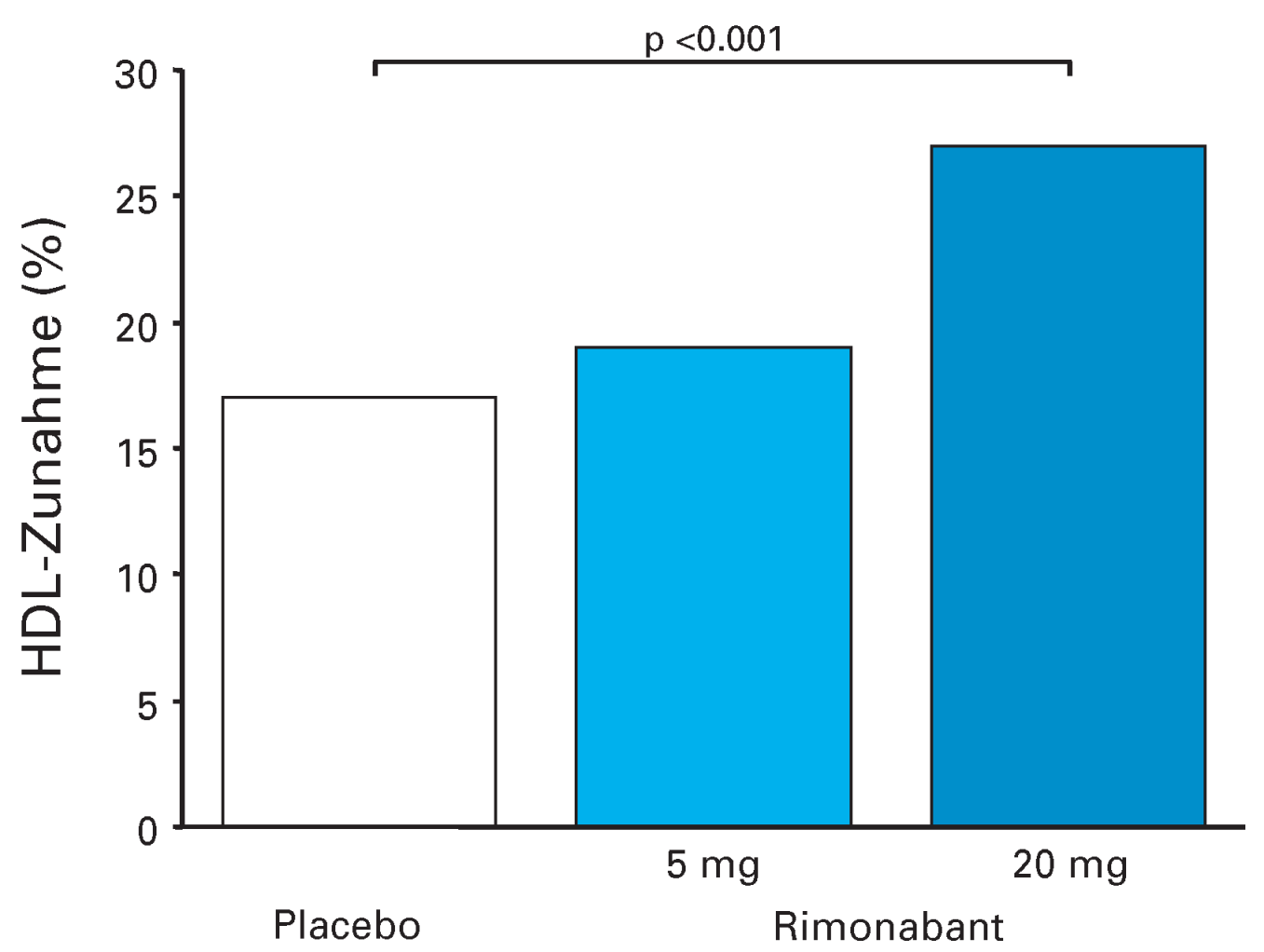
Abbildung 3.
Wirkung von Rimonabant auf das HDL-Cholesterin in der RIO-Europe-Studie. Modifiziert nach Van Gaal L. European Society of Cardiology Congress 2004, München.
Abbildung 3.
Wirkung von Rimonabant auf das HDL-Cholesterin in der RIO-Europe-Studie. Modifiziert nach Van Gaal L. European Society of Cardiology Congress 2004, München.
Liganden und ihre Wirkungen
Endogene Liganden für Cannabinoid-Rezeptoren sind Anandamid (Arachidonylethanolamid), 2-Arachidonylglycerol, Sphingosin-lphosphat und Sphingosylphosphorylcholin. Diese Liganden bewirken im Tierexperiment ähnliche Wirkungen wie die exogene Gabe von ∆9-Tetrahydrocannabinol (THC), der psychoaktiven Komponente von Marihuana (Cannabis sativa). Die chemische Struktur von THC und seine Bindung an Rezeptoren im Hirn sind seit längerem bekannt. Die kardiovaskulären Wirkungen von THC sind Tachykardie und orthostatische Hypotonie, vermittelt durch Inhibition des Sympathikus. Interesse hat THC in den letzten Jahren als Analgetikum, AppetitStimulans (bei AIDS-Patienten), Antiemetikum (bei Patienten unter Chemotherapie) und Spasmolytikum (bei multipler Sklerose) gewonnen (Tab. 1).
CB1-Rezeptoren in GABAergen Neuronen in den Basalganglien und im Kleinhirn beeinflussen die Motorik, jene im Hippocampus kognitive Funktionen, besonders das Gedächtnis. Die Rezeptordichte im Hirnstamm und Rückenmark ist gering. Bei Tieren finden sich im peripheren Gewebe CB1-Rezeptoren in Darm, Blase, Uterus und Hoden. Endocannabinoide spielen auch eine Rolle beim Schock und in der fötalen neuronalen Entwicklung.
Tabelle 1.
Wirkungen der Aktivierung des endogenen Cannabinoid-Systems.
Tabelle 1.
Wirkungen der Aktivierung des endogenen Cannabinoid-Systems.
| Reduktion der motorischen Aktivität |
| Gesteigerte visuelle und auditive Sensorik |
| Psychische Entspannung |
| Stimulation des Appetits |
| Antiemesis |
| Hemmung der intestinalen Motilität |
| Senkung des Augeninnendruckes |
| Vasodilatation, Tachykardie |
| Bronchodilatation |
Tabelle 2.
Wirkungen von Rimonabant, einem CannabinoidRezeptor-Antagonisten.
Tabelle 2.
Wirkungen von Rimonabant, einem CannabinoidRezeptor-Antagonisten.
| Gewichtsreduktion |
| Reduktion des Bauchumfanges |
| Verbesserung der Insulin-Sensitivität |
| Verbesserung des Lipid-Profils: HDL-Cholesterin-Anstieg und Triglycerd-Senkung |
| Senkung des C-reaktiven Proteins (CRP) |
| Unterstützung bei Rauchentwöhnung |
Rimonabant bei Patienten mit Übergewicht
Die RIO-Trials (Rimonabant In Obesity) untersuchten die Wirkung des Medikamentes bei Patienten mit Übergewicht. Diese Studien sind die grössten je durchgeführten Studien bei Patienten mit Adipositas.
In RIO-LIPIDS (präsentiert am ACC-Meeting 2004 in New Orleans) wurden 1036 übergewichtige Patienten mit Rimonabant (5 mg oder 20 mg) oder Plazebo behandelt. Die Patienten in der 20-mg-Gruppe reduzierte ihr Körpergewicht um 15 Pfund mehr als die Plazebo-Gruppe. Ausserdem wurden Bauchumfang, Insulin-Sensitivität und Lipid-Profil günstig beeinflusst (Tab. 2). Die HDL-Cholesterin- (+23%) und Adiponectin-Spiegel wurden deutlich erhöht, während Triglyzeride gesenkt wurden (–15%). Adiponectin ist ein prädiktiver Marker für die Entstehung eines Diabetes mellitus. Das C-reaktive Protein als Entzündungsmarker wurde gesenkt (–27%), ebenso Biomarker metabolischer Veränderungen bei Übergewicht (Leptin).
In der RIO-EUROPE-Studie (präsentiert am ESC-Meeting 2004 in München) wurden 1507 Patienten randomisiert mit Rimonabant (5 mg oder 20 mg) oder Plazebo behandelt. Ausserdem wurde eine hypokalorische Diät empfohlen (600 kcal weniger pro Tag). Nach einem Jahr wurde mit 20 mg Rimonabant eine Gewichtsreduktion von 6,6 kg erzielt, mit 5 mg 3,4 kg und unter Plazebo 1,8 kg. Viele Patienten schlossen die Studie allerdings nicht ab, nämlich um die 40% in allen drei Studiengruppen; die hypokalorische Diät dürfte die Compliance erschwert haben. Nebenwirkungen waren meist mild und vorübergehend und umfassten Nausea, Diarrhoe und Schwindel. Die HDL-Spiegel wurden in der 20-mg-Gruppe um 27% angehoben (17% in der Plazebo-Gruppe, Abb. 3). Die Prävalenz des metabolischen Syndroms wurde in der 20-mg-RimonabantGruppe halbiert. In der Rimonabant-Gruppe sank der Blutdruck um 1 mm Hg, während in der Plazebo-Gruppe keine Veränderung auftrat. Herzfrequenz und QT-Zeit wurden nicht verändert. Ein Fragebogen zur Lebensqualität zeigte eine Verbesserung in allen Bereichen gegenüber Plazebo.
Tabelle 3.
Unerwünschte Wirkungen von Rimonabant, einem Cannabinoid-Rezeptor-Antagonisten, in der RIO-NorthAmerica-Studie.
Tabelle 3.
Unerwünschte Wirkungen von Rimonabant, einem Cannabinoid-Rezeptor-Antagonisten, in der RIO-NorthAmerica-Studie.
| | Rimonabant 20 mg | Plazebo |
| Depression | 2,9% | 1,5% |
| Angstgefühle | 1,1% | 0,4% |
| Nausea | 1,3% | <0,1% |
RIO-North America (präsentiert am AHAMeeting 2004 in New Orleans) ist der bislang grösste Trial mit Rimonabant. In dieser Studie wurden 3040 Patienten über zwei Jahre mit Rimonabant (5 mg oder 20 mg) oder Plazebo behandelt. Interessanterweise nahmen mehr Frauen an der Studie teil als Männer. Die mit Rimonabant behandelten Patienten hatten nach zwei Jahren 7,4 kg abgenommen gegenüber 2,3 kg unter Plazebo. Damit verbunden war eine Zunahme des HDL-Cholesterins sowie der Triglyzeride. Die Verbesserung des Lipid-Profils beruht nicht nur auf der Gewichtsreduktion, sondern auf zusätzlichen metabolischen Wirkungen des Medikamentes. Nebenwirkungen waren eine leichte Zunahme der Inzidenz von Depression, Angstgefühlen und Nausea (Tab. 3).
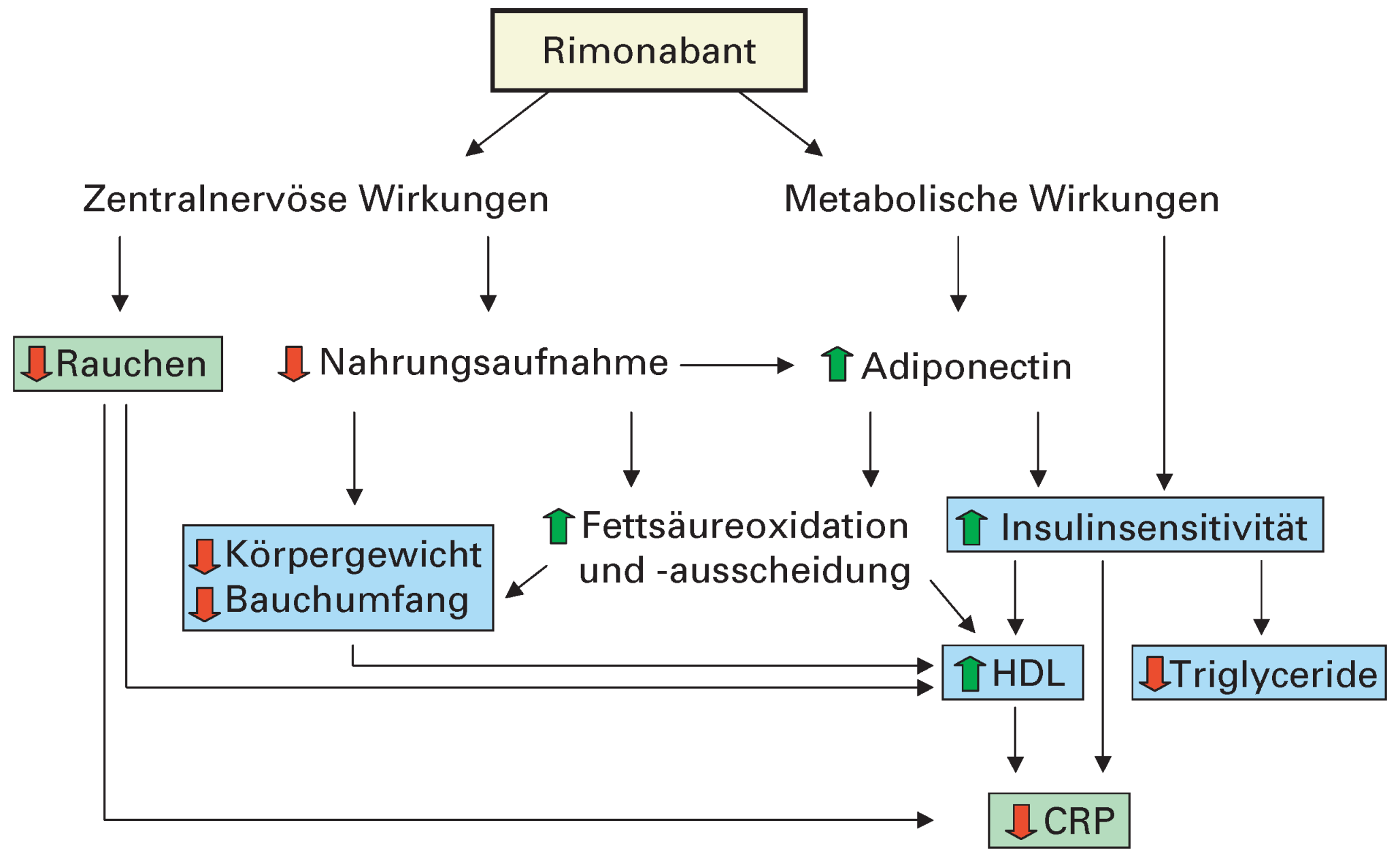
Abbildung 4.
Wirkungen von Rimonabant. Zentralnervöse Mechanismen führen zu einer Reduktion der Nahrungseinnahme und helfen bei der Rauchentwöhnung. Periphere metabolische Effekte führen zu einer Verbesserung des Lipid-Profils, verbesserter Insulin-Sensitivität und Reduktion inflammatorischer Marker wie des C-reaktiven Proteins (CRP). Blau unterlegt sind definierende Komponenten des metabolischen Syndroms.
Abbildung 4.
Wirkungen von Rimonabant. Zentralnervöse Mechanismen führen zu einer Reduktion der Nahrungseinnahme und helfen bei der Rauchentwöhnung. Periphere metabolische Effekte führen zu einer Verbesserung des Lipid-Profils, verbesserter Insulin-Sensitivität und Reduktion inflammatorischer Marker wie des C-reaktiven Proteins (CRP). Blau unterlegt sind definierende Komponenten des metabolischen Syndroms.
Rimonabant bei der Rauchentwöhnung
Rauchen ist für knapp 20% aller Todesfälle verantwortlich. Kardiovaskuläre Erkrankungen stellen neben Neoplasien und respiratorischen Krankheiten ein grosses Problem dar. Obwohl 70% der Raucher gerne aufhören möchten, schaffen nur wenige den Ausstieg. Pro Jahr versuchen ca. 30% der Raucher aufzuhören, meist ohne unterstützende Massnahmen (ärztliche Hilfe, Nikotin-Ersatz). Nur 3% der Raucher schaffen es, das Rauchen ohne Hilfe aufzugeben. Beim Aufhören kommt es meist zu einer Gewichtszunahme.
Die Rolle von Rimonabant bei der Rauchentwöhnung wird im STRATUS-Studienprogramm untersucht (STRATUS: Studies with Rimonabant and Tobacco Use). Die STRATUS-US-Studie (präsentiert am ACCMeeting 2004 in New Orleans) mit 787 Rauchern, die bereits mehrmals versucht hatten, mit den Rauchen aufzuhören, wurde im März 2004 von Anthenelli vorgestellt. Nach 10 Wochen Behandlung mit Rimonabant (20 mg pro Tag) waren fast doppelt so viele Patienten unter Rimonabant abstinent wie unter Plazebo (28% vs. 16%; p = 0,0004). Dabei wurde eine Gewichtszunahme in der Rimonabant-Gruppe vermieden, während die Plazebo-Gruppe um 1,1 kg zunahm. Die niedrigere Dosis von 5 mg steigerte die Abstinenzrate nicht.
Die Wunderpille?
Die mit Rimonabant erzielte Gewichtsreduktion in den einzelnen Studien ist bemerkenswert konsistent. Über den bisher untersuchten Zeitraum von 2 Jahren bleibt die Gewichtsreduktion erhalten. Ein Rebound-Phänomen wie bei vielen Diät-Programmen zur Gewichtsreduktion wurde nicht beobachtet. Aufgrund der vorliegenden Daten scheint Rimonabant ein ideales Medikament zur Behandlung des metabolischen Syndroms zu sein (Abb. 4). Die erreichten Verbesserungen des Lipid-Profils mit der Zunahme des HDL-Cholesterins und Senkung von Entzündungsmarkern versprechen spannende Ergebnisse von Mortalitäts- und Morbiditäts-Studien mit Rimonabant.
Das pharmakologische Profil von Rimonabant widerspricht dem Einsatz bei Patienten mit Herzerkrankungen nicht, entsprechende Sicherheitsdaten sind jedoch nicht verfügbar. Ein Blutdruck- und Herzfrequenzanstieg wie bei anderen Medikamenten, die zur Gewichts-reduktion eingesetzt werden, wurde nicht beobachtet.
Aufgrund der Blockierung des Endocannabinoid-Systems wären neuropsychiatrische Effekte durch Cannabinoid-Rezeptorblocker möglich. Validierte Scores zeigen jedoch keine signifikante Zunahme von Depressionen oder Angststörungen. In der RIO-Europe-Studie traten allerdings zwei Fälle von vorübergehender Amnesie unter Rimonabant auf. Weitere Studien werden die Daten zur Sicherheit bei anderen Patientengruppen erweitern (RIO-Diabetes).
Schlussfolgerung
Rimonabant ist der erste Vertreter der Substanzgruppe der Cannabinoid-Rezeptor-Antagonisten. Klinische Studien zeigen die Wirksamkeit bei der Behandlung übergewichtiger Patienten, bei denen eine deutliche Gewichtsreduktion erreicht werden kann. Daneben werden Lipid-Profil und Insulin-Resistenz günstig beeinflusst. Rimonabant wurde ausserdem in Rauchentwöhnungsprogrammen erfolgreich getestet. Mit Interesse erwartet werden Studien, die untersuchen, ob die Behandlung mit Rimonabant bei Hochrisikopatienten zu einer Verminderung kardiovaskulärer Ereignisse führt.