Fallbeschreibung
Der 70-jährige Patient wurde uns zugewiesen zur stationären kardialen Rehabilitation bei St. n. mechanischem Aortenklappenersatz wegen schwerer degenerativer Aortenstenose. Wegen ungerichtetem Schwindel wurde im Verlauf der Rehabilitation ein 24-h-EKG durchgeführt mit der Frage nach Auftreten von Vorhofflimmern. Das Telemetrie-EKG konnte folgende Rhythmusstörung dokumentieren (Abb. 1):
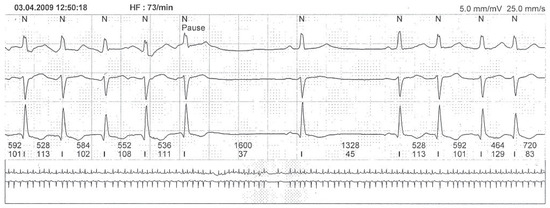
Abbildung 1.
Telemetrie-EKG mit paroxysmalem Vorhofflimmern.
Kommentar
In der Telemetrie konnten mehrere Phasen von paroxysmalem Vorhofflimmern von mehreren Minuten Dauer dokumentiert werden. Oben abgebildeter Telemetrie-Ausschnitt zeigt ein Vorhofflimmern mit präautomatischer Pause. Nach zwei Sinusschlägen folgt erneut Vorhofflimmern. Als präautomatische Pause wird das Aussetzen des Herzschlages nach Beendigung eines anfallsartig auftretenden Vorhofflimmerns oder -flatterns bezeichnet, wenn der Sinusknoten als Schrittmacherzentrum nicht unmittelbar seine Arbeit wieder aufnimmt.
Das Telemetrie-EKG zeigt ein paroxysmales Vorhofflimmern. Das paroxysmale Vorhofflimmern ist allerdings nicht die typische Herzrhythmusstörung nach Herzchirurgie. Die typische Tachyarrhythmie nach Herzchirurgie ist das sogenannte postoperative Vorhofflimmern, dessen pathophysiologischer Mechanismus ein anderer ist als beim paroxysmalen und persistierenden Vorhofflimmern. In der Folge sollen die Pathomechanismen der unterschiedlichen Formen von Vorhofflimmern erläutert und die Therapie des postoperativen Vorhofflimmerns erörtert werden.
Bei der Entstehung von paroxysmalem Vorhofflimmern spielt die fokale Automatie eine bedeutende Rolle. Dem Beginn von paroxysmalem Vorhofflimmern gehen fokale Automatien voraus, die zu salvenartigen Entladungen führen. Mapping-Untersuchungen konnten zeigen, dass sich diese ektopen Foci überwiegend in der Region der Pulmonalvenen befinden.
Die Pathophysiologie des persistierenden Vorhofflimmerns wird noch immer zumindest teilweise durch die «multiple wavelet»-Theorie erklärt [1]. Sie beschreibt die Annahme, dass bei Vorhofflimmern mehrere Erregungswellen durch das Vorhofmyokard laufen und dabei beständig auf erregbares Myokard treffen.
Die Pathophysiologie des postoperativen Vorhofflimmerns ist multifaktoriell und nicht abschliessend geklärt. Involvierte Mechanismen sind chemische Entzündung und Reizung, exzessive Ausschüttung von Katecholaminen, Flüssigkeitsverschiebungen (intravaskulär und interstitiell) mit Volumen- und Druckänderungen sowie Aktivierung neurohumoraler Prozesse. Das Ausmass der operativen Manipulation am Myokard (Anzahl der Bypässe, Ort der Operation), die peri- oder postoperative Volumenüberladung mit konsekutiver Dehnung der Vorhöfe oder die Art der Kardioplegie führen zu einer Veränderung der atrialen Leitungsgeschwindigkeit und zu zunehmender Inhomogenität der Refraktärzeiten [2,3]. Diese Veränderungen begünstigen somit die Ausbildung von Reentry-Kreisläufen. Zudem bieten sich den Flimmerwellen ebenfalls mehr anatomische Hindernisse (durch das manipulierte verletzte Myokard) an denen sie sich aufteilen und vermehren können, ein weiterer Faktor, der den Unterhalt der kleinen Reentrykreisläufe fördert.
Vor diesem Hintergrund wird verständlich, warum Vorhofflimmern eine häufige postoperative Komplikation nach kardiochirurgischen Eingriffen darstellt. Prozentuale Angaben über die Häufigkeit sind unterschiedlich, dies liegt allerdings an uneinheitlichen Patientenkollektiven (koronare Revaskularisation 15–40%, Klappenchirurgie bis 50%, kombinierte Eingriffe bis 60%) [3].
Studien konnten belegen, dass die Leitungsverzögerung der atrialen Myokardzellen am zweiten und dritten postoperativen Tag am höchsten ist. Korrelierend dazu besteht die grösste Wahrscheinlichkeit für postoperatives Vorhofflimmern in diesem Zeitfenster [3]. Es kann allerdings auch mit einer Latenz von mehreren Wochen auftreten.
Die Therapie des postoperativen Vorhofflimmerns umfasst wie auch die Therapie des nicht mit einem herzchirurgischen Eingriff assoziierten Vorhofflimmerns eine Frequenzkontroll- und eine Rhythmuskontroll-Strategie. Wir favorisieren in unserem klinischen Setting (postoperativer Patient in der kardialen Rehabilitation) klar die Rhythmuskontroll-Strategie, ist nach Wiederherstellung des Sinusrhythmus doch die körperliche Leistungsfähigkeit der Patienten in der Regel besser und auch die Hospitalisationsdauer kürzer [4]. Postoperatives Vorhofflimmern ist assoziiert mit einem erhöhten thromboembolischen Risiko. Dieses Risiko kann durch eine therapeutische Antikoagulation verringert werden, allerdings muss diese Risikoreduktion sorgfältig gegen das erhöhte Blutungsrisiko (im Operationsgebiet, insbesondere Perikardtamponade) abgewogen werden. In unserem klinischen Alltag wird eine therapeutische Antikoagulation dann eingeleitet, wenn das postoperative Vorhofflimmern >24–48h persistiert oder bei häufigen Flimmer-Episoden, insbesondere bei Hochrisikopatienten (mit St. n. zerebrovaskulärem Insult) [5]. Die Antikoagulation wird nach Wiederherstellung des Sinusrhythmus für mind. 30 Tage weitergeführt, aus praktischen Gründen jedoch meist bis zur nächsten kardiologischen Kontrolle 3 Monate postoperativ. Dann muss die Indikation der Antikoagulation (und auch allfälliger Antiarrhythmika) vom nachbehandelnden Kardiologen neu evaluiert werden.
Funding/Potential Competing Interests
No financial support and no other potential conflict of interest relevant to this article was reported.
References
- Moe, G.K.; Abildskov, J.A. Atrial fibrillation as a self-sustaining arrhythmia independent of focal discharge. Am Hear J. 1959, 58, 59–70. [Google Scholar] [CrossRef] [PubMed]
- Arnsdorf, M.; Goldberger, A.; et al. Electrocardiographic and electrophysiologic features of atrial fibrillation, last literature view for version 17.1: 1 January 2009, last updated: 21 December 2006. www.uptodate.com.
- Maisel, W.H.; Rawn, J.D.; et al. Atrial fibrillation after cardiac surgery. Ann Intern Med. 2001, 135, 1061–1073. [Google Scholar] [CrossRef] [PubMed]
- Lee, J.K.; Klein, G.J.; et al. Rate-control versus conversion strategy in postoperative atrial fibrillation: Trial design and pilot study results. Card Electrophysiol Rev. 2003, 7, 178–184. [Google Scholar] [CrossRef] [PubMed]
- Echahidi, N.; Pibarot, P.; et al. Mechanisms, Prevention, and Treatment of Atrial Fibrillation After Cardiac surgery: Review. J Am Coll Cardiol. 2008, 51, 793–801. [Google Scholar] [CrossRef] [PubMed]
© 2011 by the author. Attribution - Non-Commercial - NoDerivatives 4.0.