Zusammenfassung
Allgemeine milde Reaktionen auf nichtionische Kontrastmittel sind häufig, schwere Reaktionen (z.B. Dyspnoe, Hypotonie, Kreislaufstillstand) sind selten. Ein Lungenödem wird in 10–20% der Fälle einer fatalen Reaktion nach intravenöser Kontrastmittelgabe beschrieben. Bei kontrastmittelinduzierten Lungenödemen muss zwischen kardiogener und nichtkardiogener Ätiologie unterschieden werden. Dem kontrastmittelinduzierten kardiogenen Lungenödem liegt eine akute Volumenüberladung mit konsekutiver Erhöhung des intravasalen hydrostatischen Druckes und Übertritt von Flüssigkeit in die Alveolen zugrunde. Beim nichtkardiogenen Lungenödem kommt es zu einer erhöhten Kapillarpermeabilität bei normalen hydrostatischen Druckverhältnissen.
Wir präsentieren einen Fall eines nichtkardiogenen Lungenödems nach Kontrastmittelexposition im Rahmen einer Koronarangiographie und perkutanen Intervention.
Fallvorstellung
Ein 70jähriger Patient wurde zur angiographischen Evaluation bei pektanginösen Beschwerden (CCS-Klasse III) bei langjähriger koronarer Herzkrankheit zugewiesen. Der Patient litt zudem an einer mittelschweren Niereninsuffizienz (errechnete Kreatinin-Clearance 18 mL/min; kompensierte Retention, Stadium II b) mit seit Jahren stabilem Verlauf nach Diagnose einer membranösen Glomerulonephritis im Jahre 1959. Als kardiovaskuläre Risikofaktoren bestanden eine arterielle Hypertonie und eine Hypercholesterinämie.
1989 klagte er erstmals über Angina pectoris; im November 1992 wurde er chirurgisch revaskularisiert (Endarterektomie des Ramus diagonalis, LIMA auf RIVA, Vene zum RIVP, Vene zum PLA der RCA mit Jump zum PLA der RCX und zum Ramus diagnonalis). Nach Auftreten von erneuten medikamentös nichtkontrollierbaren pektanginösen Beschwerden wurde im Dezember 2001 wiederum eine 3fache ACBP-Operation (off-pump) mittels eines Venengrafts auf den distalen RIVA und eines weiteren Venen-Jump-Grafts auf den RCX und den Diagonalast durchgeführt. Im Anschluss an die präoperative Koronarangiographie kam es erstmalig zu Gewichtszunahme, Lungenödem und peripheren Ödemen. Die linksventrikuläre Auswurffraktion war normal. Nach beschwerdefreiem Intervall folgte im Dezember 2004 die oben erwähnte erneute kardiologische Evaluation bei wiederum zunehmenden pektanginösen Beschwerden: die bei Eintritt durchgeführte Echokardiographie dokumentierte einen normal grossen linken Ventrikel mit normaler Auswurffraktion (EF 56%) und eine diastolische Dysfunktion im Sinne einer Relaxationsstörung, keine relevanten Valvulopathien sowie einen systolischen transtrikuspidalen Druckgradienten von 26 mm Hg über dem rechten Vorhofdruck.
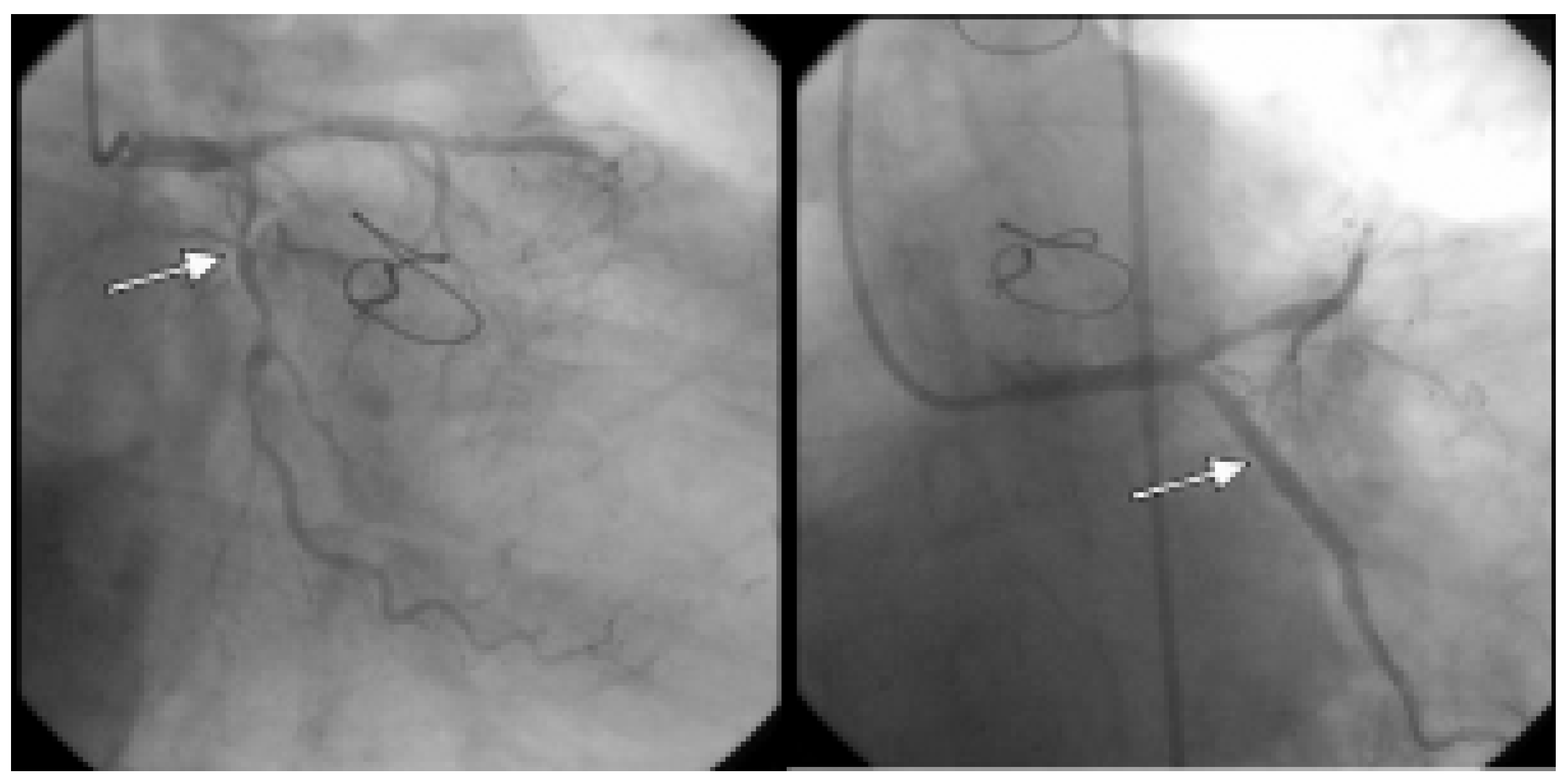
Nach Vorbehandlung mit Flüssigkeit und N-Acetylcystein fand sich koronarangiographisch als Hauptbefund eine subtotale komplexe mittlere RCX-Stenose, welche interventionell mittels mehrfacher Stent-Implantation behandelt wurde (
Abbildung 1). Im Verlauf kam es zu einem CK-Anstieg bis max. 861 U/l bei einem RCX-Seitenastverschluss im Bereiche des gestenteten Segments. Nach anfänglich beschwerdefreiem Verlauf und Mobilisation des Patienten kam es in der Nacht nach dem Eingriff zu zunehmenden Thoraxschmerzen und Atemnot. Eine erneute notfallmässige Koronarangiographie wurde durchgeführt. Eine subakute Stent-Thrombose wurde ausgeschlossen, eine vorgängig belassene grenzwertig signifikante proximale RCX-Stenose wurde mittels Stent-Implantation versorgt. Insgesamt wurden innerhalb von 48 Stunden bei diesen zwei Koronarangiographien 550 mL (400 mL und 150 mL) Iopromid (Ultravist
®)—ein nichtionisches niederosmolares jodiniertes Kontrastmittel—verabreicht. Im Laufe des nachfolgenden Tages entwickelte der stets hämodynamisch stabile Patient bei unveränderten Gewichtsverhältnissen und ausgeglichener Volumenbilanzierung klinisch-radiologisch ein Lungenödem mit Hämoptoe und transkutan gemessenen peripher-arteriellen O
2-Sättigungen zwischen 70–80%. Daraufhin wurde der Patient maschinell beatmet, der Pulmonaliskatheter dokumentierte normale Druckverhältnisse (insbesondere normale pulmonal-kapilläre Verschlussdrücke) sowie einen normalen Cardiac Index (stets zwischen 4–5 l/min/m
2). In der Bronchoskopie zeigte sich lediglich eine diffuse alveoläre Hämorrhagie. Laborchemisch imponierten u.a. erniedrigte Komplementwerte und eine temporäre Thrombozytopenie (minimal 98 × 10
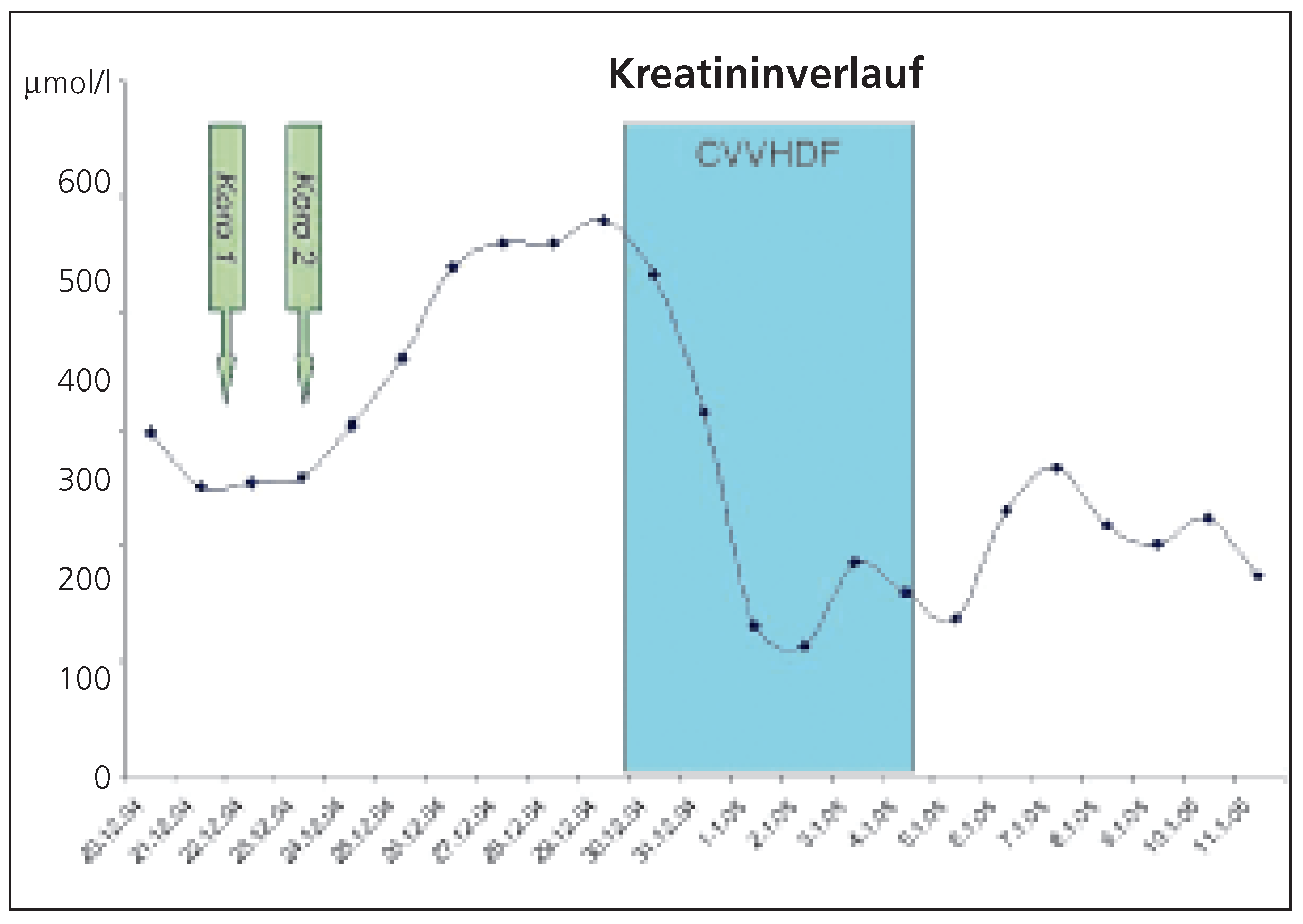
3/μL). Eine Überwässerung wurde trotz steigenden Kreatinin-Werten bei ausgeglichener Bilanzierung und normalen Füllungsdrucken ausgeschlossen. Aufgrund dieser Befunde wurde ein nichtkardiogenes Lungenödem bei erhöhter Permeabilität der Lungenkapillaren nach Kontrastmittelexposition im Sinne eines ARDS diagnostiziert. Ein sekundärer pulmonaler Infekt wurde antibiotisch behandelt. Zudem kam es zu einem Nierenversagen (acute on chronic, kontrastmittelbedingt), welches mit temporärer veno-venöser Hämodiafiltration behandelt werden musste (
Abbildung 2). Im weiteren Verlauf erholte sich der Patient zusehends und er konnte schlussendlich beschwerdefrei nach Hause entlassen werden.
Diskussion
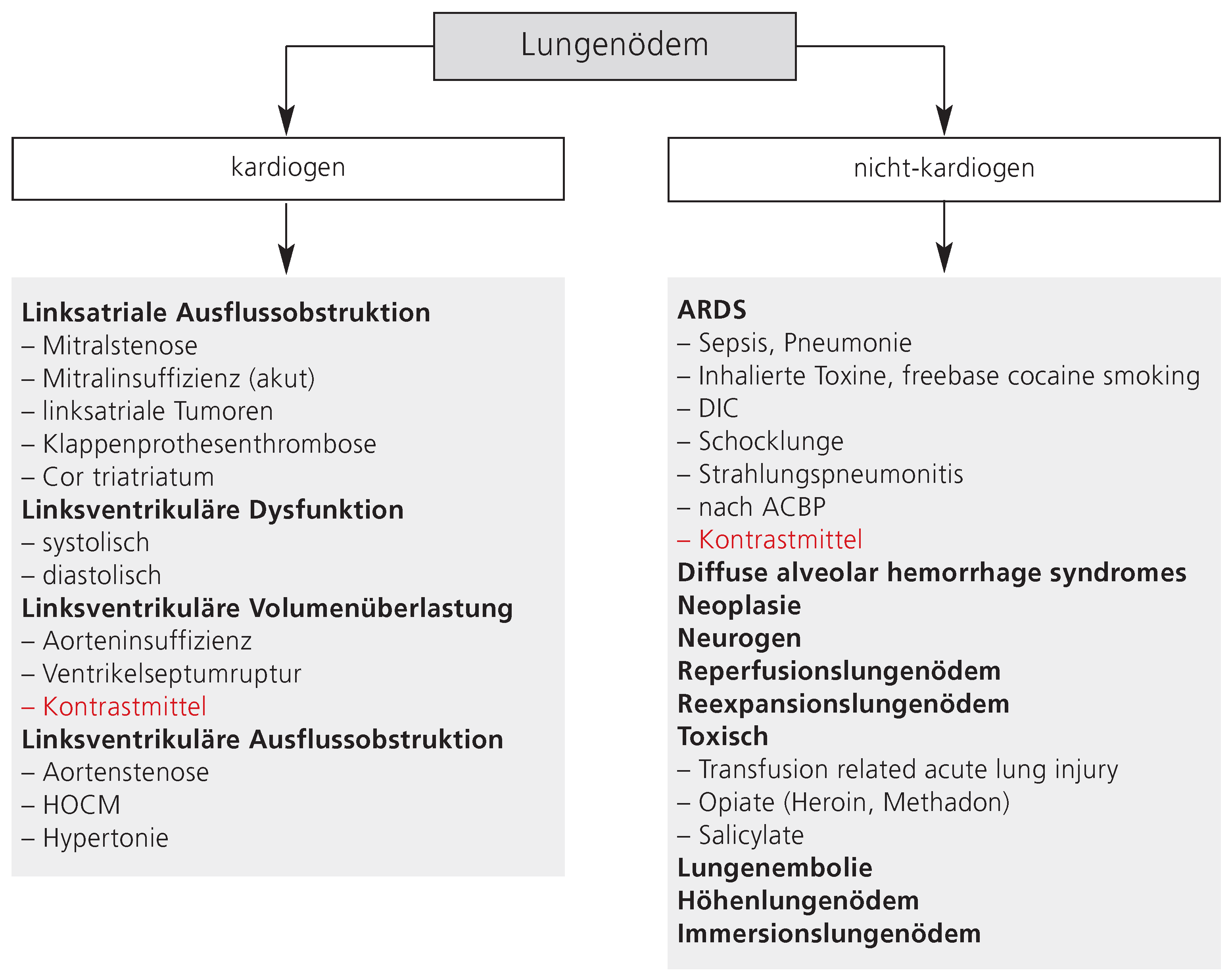
Das Lungenödem hat eine mannigfaltige Ätiologie (
Abbildung 3). Allgemeine milde Reaktionen auf nichtionische Kontrastmittel sind häufig, schwere Reaktionen (z.B. Dyspnoe, Hypotonie, Kreislaufstillstand) sind selten und kommen in ca. 0,04% der Patienten vor, welche Kontrastmittel erhalten [
1]. Ein Lungenödem wird in 10–20% der Fälle einer fatalen Reaktion nach intravenöser Kontrastmittelgabe beschrieben, ein subklinisches Lungenödem ohne klinische respiratorische Probleme scheint dagegen häufig zu sein, allerdings ist es schwierig, Angaben zur wahren Inzidenz zu machen [
2].
Bei kontrastmittelinduzierten Lungenödemen muss zwischen kardiogener und nichtkardiogener Ätiologie unterschieden werden. Dem kontrastmittelinduzierten kardiogenen Lungenödem liegt eine akute Volumenüberladung mit konsekutiver Erhöhung des intravasalen hydrostatischen Druckes und Übertritt von Flüssigkeit in die Alveolen zugrunde. Dieser Effekt wird bei älteren Kontrastmitteln mit höherer Osmolarität durch zusätzlichen osmotischen Flüssigkeitseinstrom ins Gefässsystem verstärkt.
Beim nichtkardiogenen Lungenödem kommt es zu einer erhöhten Kapillarpermeabilität bei normalen hydrostatischen Druckverhältnissen. Der pathophysiologische Hintergrund ist nicht vollständig geklärt. Der Permeabilitätserhöhung scheint keine anaphylaktische histaminvermittelte Reaktion zugrundezuliegen [
3]. Vielmehr werden Mechanismen wie Komplementaktivierung, Bildung von Sauerstoffradikalen, die Freisetzung von proteolytischen Enzymen [
4] oder direkt toxische Effekte des Kontrastmittels am Endothel postuliert.
Das nichtkardiogene kontrastmittelinduzierte Lungenödem ist extrem selten. Es gibt in der Literatur lediglich vereinzelte Fallberichte [
1,
3,
4,
5,
6,
7]. Erstmalig wurde es 1995 beschrieben [
6]. Es tritt vermehrt bei ionischen Kontrastmitteln auf, kommt aber auch bei der Verwendung von nichtionischen Kontrastmitteln vor. In den meisten Fällen sind Frauen von dieser seltenen Komplikation betroffen [
3].
Das ARDS (acute respiratory distress syndrome) ist ein ernsthafter Zustand, welcher mit einer beträchtlichen Mortalität zwischen 34–58% behaftet ist [
8]. Eine anti-anaphylaktische Behandlung ist beim nichtkardiogenen kontrastmittelinduzierten Lungenödem nicht von Nutzen. Die Gabe von Diuretika oder Vasodilatoren kann die Situation gar aggravieren [
4]. Die Therapie besteht primär aus konzentrierter Sauerstoffzufuhr mit nichtinvasiver CPAP (continous positive airway pressure)-Ventilation oder invasiver Ventilation mit PEEP (positive end expiratory pressure) [
5,
7].