Einleitung
Kardiovaskuläre Herzerkrankungen gehören nach wie vor zu den führenden Todesursachen in Industrieländern [1]. Das akute Koronarsyndrom (ACS) – die schwerwiegendste Komplikation der koronaren Herzerkrankung – hat weiterhin die grösste Bedeutung unter allen kardiovaskulären Erkrankungen und geht mit einer hohen Morbidität und Mortalität einher.
Das ACS wird über verschiedene elektrokardiographische sowie laborchemische Charakteristika definiert. Entsprechend werden ST-Hebungs-Infarkte (STE-ACS) von Nicht-ST-Hebungs-Infarkten (NSTE-ACS) unterschieden. Letztere präsentieren sich klinisch mit (NSTEMI) oder ohne Dynamik des Troponins (instabile Angina pectoris).
Die Mortalität beim ACS ist in den letzten Jahren aufgrund der verbesserten Prä-Hospitalisationsphase sowie einer gezielten Akutversorgung mit frühzeitiger Revaskularisierung mittels perkutaner Koronarintervention (PCI) und Gebrauch potenter Thrombozytenaggregationshemmer deutlich zurückgegangen. Sie liegt aber gemäss den Daten verschiedener nationaler Register nach wie vor zwischen 6% und 14% [2,3]. Das Outcome von Patienten ist jedoch weiterhin stark abhängig von der klinischen Präsentation und dem Schweregrad der Erkrankung bei Eintritt [4,5,6], sodass in gewissen Fällen trotz modernster Therapie dennoch eine hohe Morbidität sowie Mortalität persistiert.
Ziel der Studie war es, die Spitalmortalität sowie den Einfluss hämodynamischer Faktoren (z.B. kardiogener Schock) und akuter Therapiemassnahmen (z.B. Katecholamingabe, Intubation, Reanimation, Einsatz kreislaufunterstützender Systeme wie extrakorporale Membranoxygenierung (ECMO) und intraaortale Ballonpumpe (IABP) auf das Outcome beim ACS der im UniversitätsSpital Zürich (USZ) behandelten Patienten zu untersuchen.
Methoden
Patientenpopulation
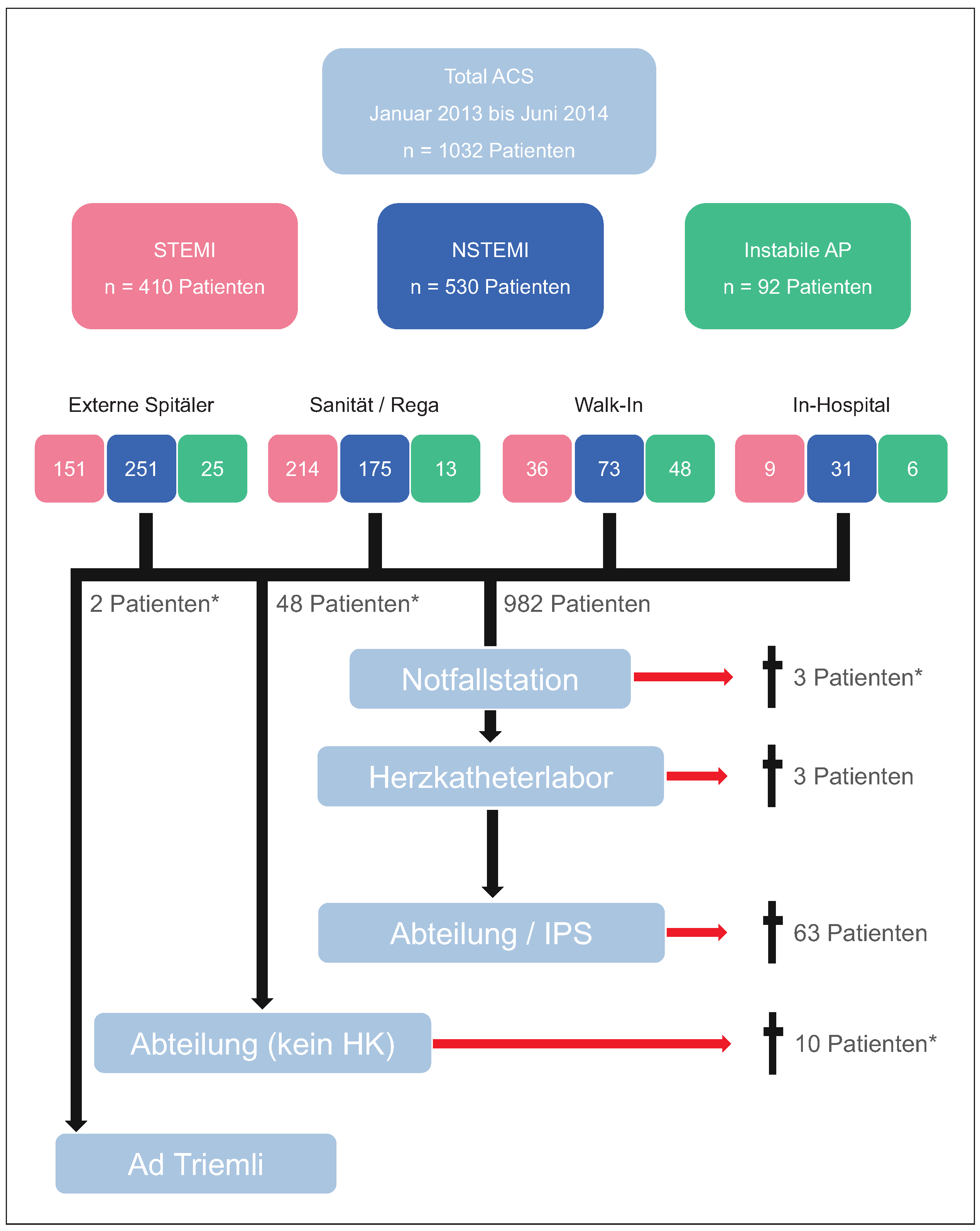
Im Zeitraum von Januar 2013 bis Juni 2014 wurden alle Patienten mit ACS, die in den Andreas-Grüntzig-Herzkatheterlaboratorien am USZ eine Koronarangiographie erhielten, in die Studie eingeschlossen. ACS wurde definiert als ST-Hebungs-Myokardinfarkt (STEMI), Nicht-ST-Hebungs-Myokardinfarkt (NSTEMI) oder instabile Angina pectoris (instabile AP) basierend auf den Klassifikationen nach Thygessen et al. [7]. Folgende Daten wurden retrospektiv aus der Datenbank des KISIM («Klinik-Information-System Innere Medizin») – einer spitalinternen Datenbank des USZ – erhoben: Alter, Geschlecht, kardiovaskuläre Risikofaktoren und Medikamente, Koronarbefund, hämodynamische Parameter wie Blutdruck und Herzfrequenz sowie linksventrikuläre Ejektionsfraktion (angiographisch oder post-interventionell mittels Echokardiographie ermittelt). Ebenfalls wurde die Hospitalisationsdauer (ab Eintritt ins USZ bis Austritt aus dem USZ) berücksichtigt. Die Eintrittsweise der Patienten ins USZ wurde wie folgt kategorisiert:
- –
Walk-In: Patienten mit ACS, welche die Notfallstation des USZ selbstständig aufgesucht haben.
- –
Sanität/REGA: Patienten mit ACS, welche via Sanität oder REGA auf die Notfallstation des USZ eingetreten sind. Ebenfalls in dieser Gruppe inbegriffen sind Patienten, welche von Hausarztpraxen via Sanität aufgrund eines ACS ins USZ zugewiesen wurden.
- –
Externe Spitäler: Patienten mit ACS, welche von externen Spitälern zur weiteren Behandlung zugewiesen wurden.
- –
In-Hospital: Patienten, welche während ihrer Hospitalisation im USZ an einem ACS erkrankten.
Um den Einfluss der klinischen Präsentation und der eingesetzten akuten Therapiemassnahmen zu untersuchen, wurden die Patienten in folgende Untergruppen eingeteilt:
- –
Reanimation: Patienten mit ACS, welche ausserhalb des Spitals oder im Spital (USZ oder externes Spital) mechanisch und/oder elektrisch reanimiert wurden.
- –
Kardiogener Schock: Patienten mit ACS, welche bei Eintritt, während der Koronarangiographie oder während der Hospitalisation einen kardiogenen Schock entwickelt haben (BD syst. <100 mm Hg, Herzfrequenz >100/min und klinische Symptome).
- –
Katecholamingabe: Patienten mit ACS, welche während der Koronarangiographie bzw. der Hospitalisation vasoaktive Medikamente wie Noradrenalin oder Adrenalin erhalten haben.
- –
Intubation: Patienten mit ACS, welche vor bzw. während der Hospitalisation invasiv beatmet werden mussten. Patienten, welche operativ revaskularisiert (ACBP-Operation) und innerhalb der ersten 24 Stunden postoperativ extubiert werden konnten, wurden hier nicht berücksichtigt.
- –
Kreislaufunterstützungssysteme: Patienten mit ACS, welche im Rahmen der Koronarangiographie/Operation oder im Verlauf der Hospitalisation eine ECMO oder IABP benötigt haben.
Die Daten wurden im Rahmen einer universitätsinternen Qualitätskontrolle erhoben und analysiert.
Outcome
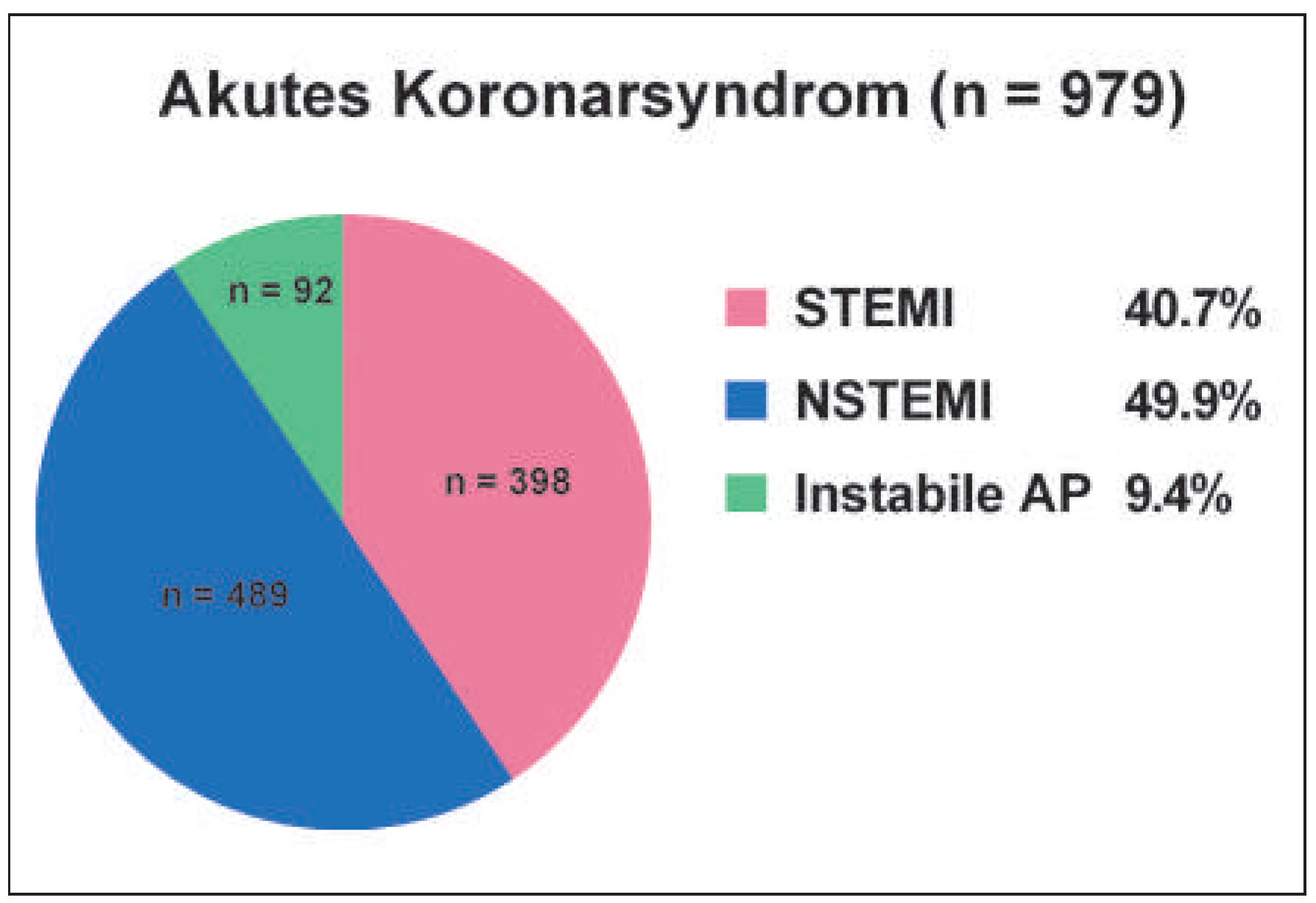
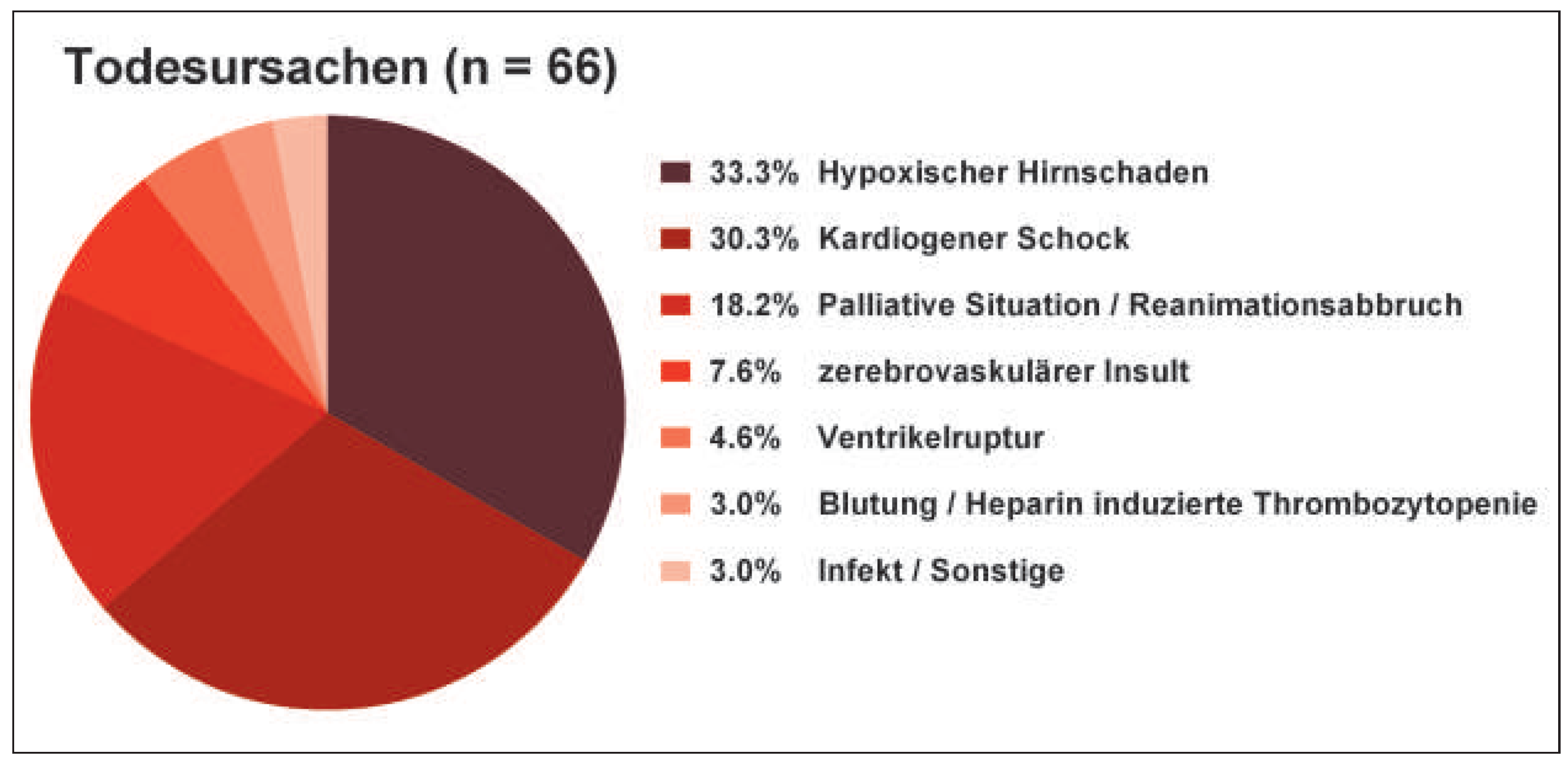
Analysiert wurden die Gesamtspitalmortalität sowie die Mortalität einzelner ACS-Subgruppen (STEMI, NSTEMI bzw. instabile AP). Zudem wurde die Mortalität hinsichtlich unterschiedlicher klinischer Präsentationen sowie hinsichtlich oben genannter akuter Therapiemassnahmen ermittelt. Peri- und postinterventionelle Todesursachen wurden in hypoxischen Hirnschaden, therapierefraktären kardiogenen Schock, palliative Situation / frustrane Reanimation, zerebrovaskuläres Ereignis (zerebrovaskulärer Insult / Blutung), Ventrikelruptur, Blutungen / Heparin-induzierte Thrombozytopenie sowie Infekt / Sonstige unterteilt. Ebenso wurden Komplikationen, welche im Rahmen der Behandlung erfolgten, analysiert und in die Untergruppen akutes Nierenversagen, Stent-Thrombose, Reinfarkt während der Hospitalisation, Perikardtamponade, Aneurysma spurium, retroperitoneales Hämatom sowie Kompartmentsyndrom aufgeteilt.
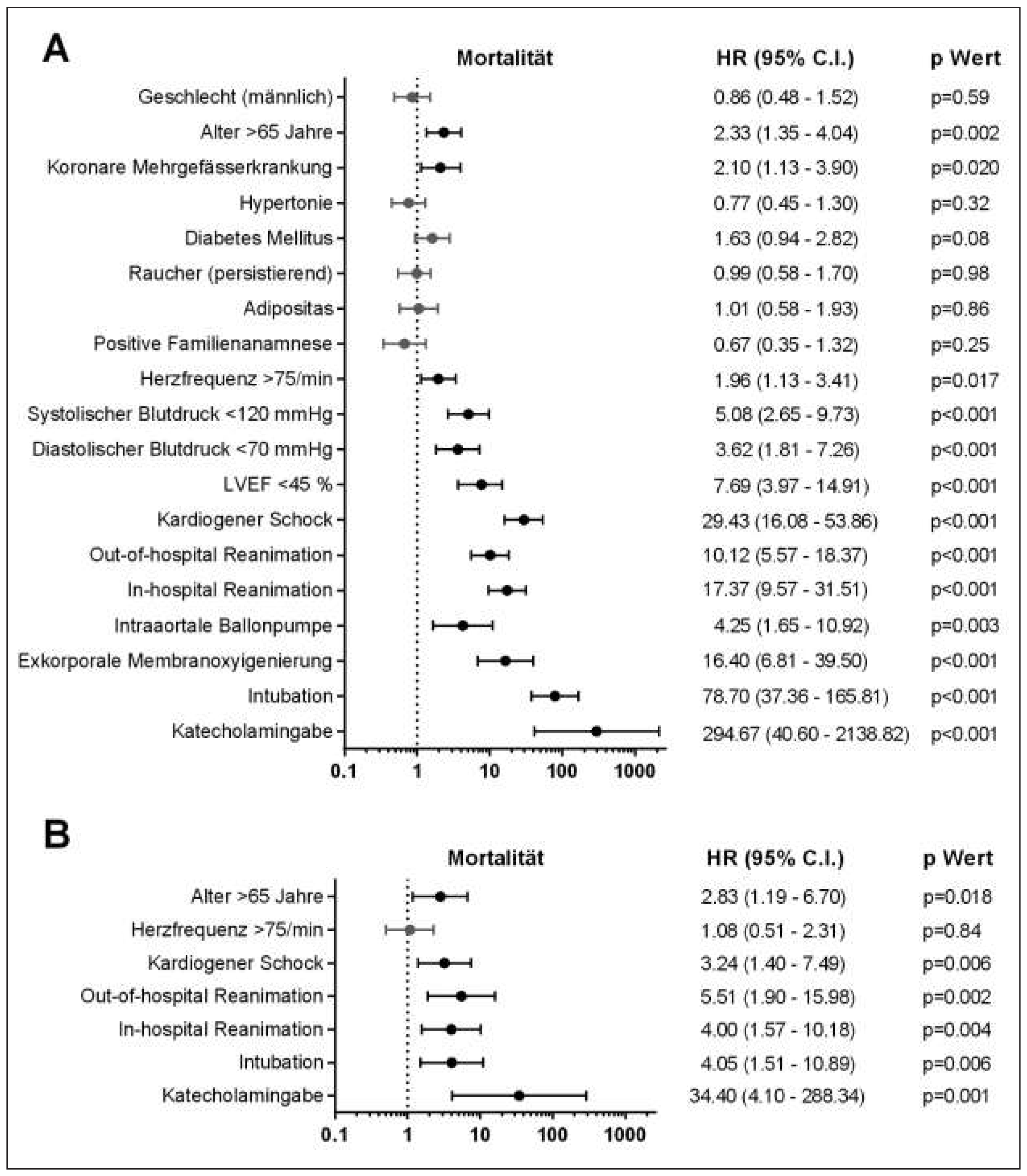
Des Weiteren wurden uni- sowie multivariate Prädiktoren der Mortalität der gesamten Kohorte ermittelt und deren statistische Signifikanz getestet.
Statistik
Kontinuierliche Variablen sind als Mittelwert ± Standardabweichung und kategoriale Variablen als Zahlen und in Prozent dargestellt. Unterschiede zwischen den Gruppen wurden mittels Chi-Quadrat-Test für nominale oder mit einer einfaktoriellen ANOVA für kontinuierliche Variablen berechnet. Zwecks Ermittlung univariater Prädiktoren der Mortalität wurde eine Chi-Square-Analyse sowie ein Student’s T-Test durchge-führt. Mittels einer multiplen logistischen Regression wurden anschliessend signifikante Variablen aus der univariaten Analyse berücksichtigt, um unabhängige Prädiktoren der Mortalität zu ermitteln. Die entsprechenden Hazard Ratios sind mit 95% Konfidenzintervallen dargestellt. Ein p-Wert von <0,05 wurde als statistisch signifikant definiert. Statistische Analysen wurden mit SPSS 22,0 (SPSS Inc., Chicago, IL, USA) durchgeführt. Sämtliche Abbildungen wurden mit PowerPoint (Microsoft Office Professional Plus, Microsoft PowerPoint 2010) oder GraphPad Prism Version 6,00 (GraphPad, La Jolla, CA, USA) erstellt.
Diskussion
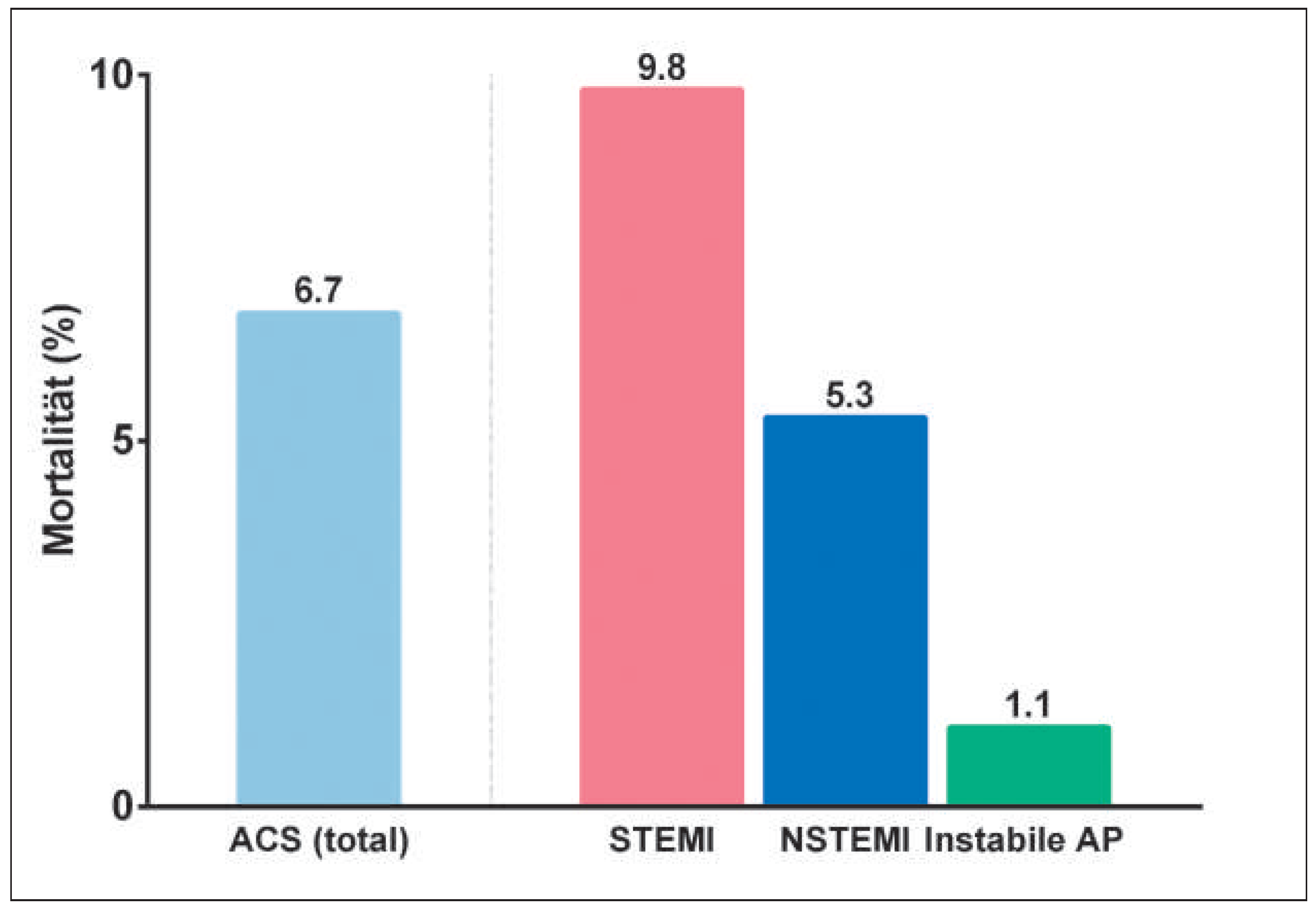
In dieser «Real World Population» von knapp 1000 konsekutiven Patienten, welche aufgrund eines ACS in den Andreas-Grüntzig-Herzkatheterlaboratorien des USZ eine Koronarangiographie erhielten, konnten wir folgende wichtigen Befunde erheben: (1) Die Gesamtmortalität in einem tertiären Zentrum liegt heute bei rund 7%; (2) Patienten mit STEMI, NSTEMI oder instabiler AP unterscheiden sich demographisch und hämodynamisch sowie auch bezüglich Mortalität erheblich und (3) die Spitalmortalität wird massiv durch die initiale Präsentation, d.h. durch eine hämodynamische Stabilität bzw. Instabilität oder einem Status nach Reanimation bestimmt.
Seit Eisenhowers berühmtem Herzinfarkt 1955 [8] hat sich die Spitalsterblichkeit dank Entwicklungen wie dem Defibrillator, der Intensivstation, Betablockern und ACE-Hemmern und schliesslich der Thrombolyse sowie der primären PCI massiv von über 50% auf heutige Werte von unter 10% vermindert. Die im vorliegenden «Real World»-Kollektiv konsekutiv an einem tertiären Zentrum interventionell behandelten Patienten erhobene mittlere Mortalität von 6,7% ist im Vergleich mit dem internationalen GRACE-Register sehr gut (GRACE-Mortalität: 7,7%) [9]. Beachtlich hierbei ist insbesondere, dass sämtliche in diesem Zeitraum behandelten Patienten – das heisst auch solche mit deutlich erhöhtem Mortalitätsrisiko – in die Studie miteingeschlossen wurden, was in den meisten Registern nicht der Fall ist. Das Schweizerische AMIS-Register, welches diesem Standard etwas näher kommt, weist eine Spitalmortalität der 76 beteiligten Zentren von 6,8% aus [10], wobei hier zu berücksichtigen ist, dass der Anteil hämodynamisch instabiler oder reanimierter Patienten von Zentrum zu Zentrum sehr unterschiedlich ist. Wie bei einem tertiären Zentrum zu er-warten, lag der Anteil hämodynamisch instabiler und/ oder beatmeter Patienten, welche einer Kreislaufunterstützung bedurften in diesem Register mit 27,4% im Quervergleich sehr hoch.
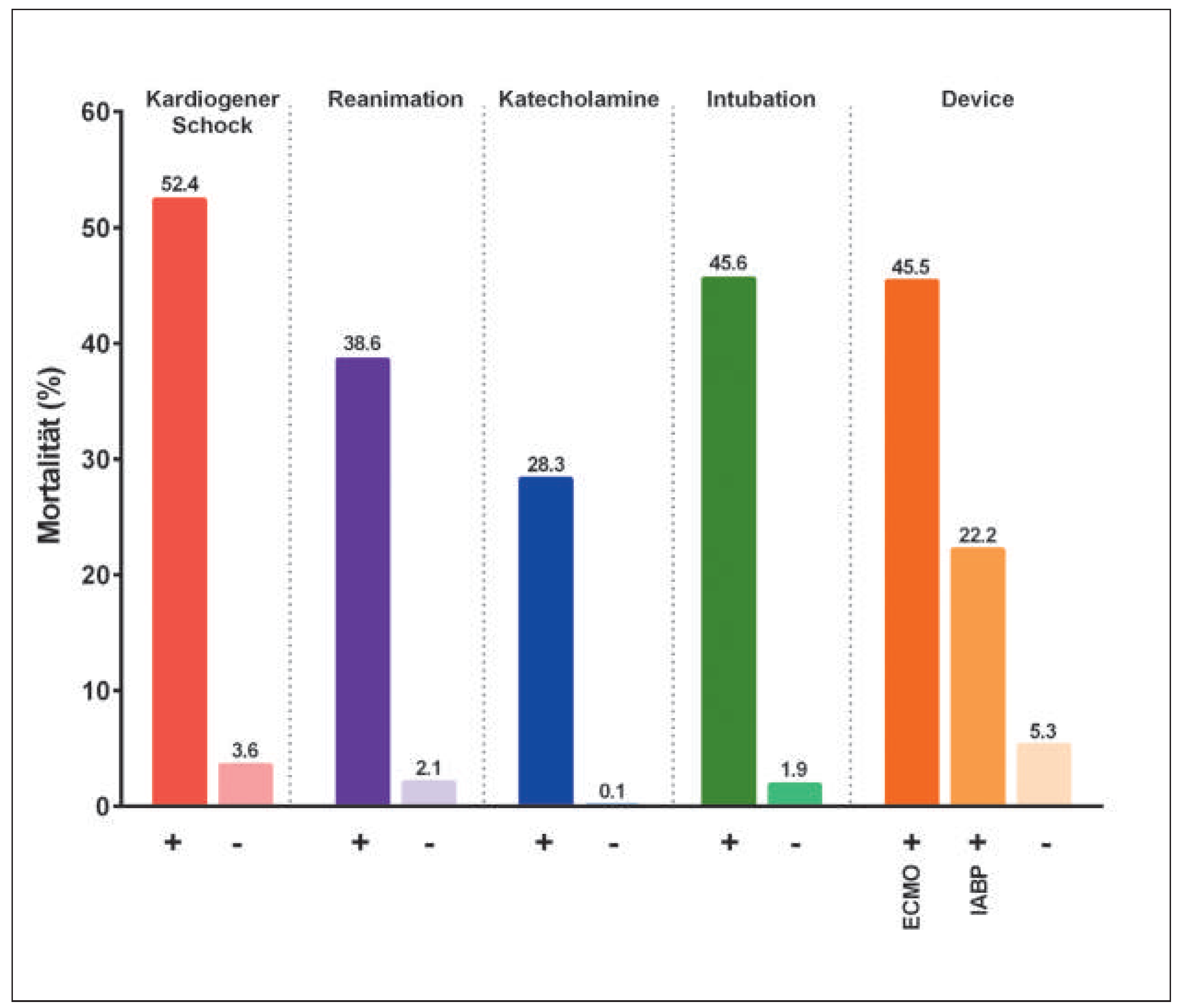
Durch stetige Verbesserung der medizinischen Versorgung und Entwicklung der therapeutischen Möglichkeiten mit neuen Technologien werden vor allem in tertiären Zentren zunehmend komplexere ACS Patienten mit schwersten kardiovaskulären Erkrankungen und Komorbiditäten oder mit Status nach externer Reanimation mittels perkutaner Koronarintervention im Spital versorgt. Trotz enormer Fortschritte in der Frühbehandlung, der Logistik, der medikamentösen Begleittherapie und den Interventionstechniken bleibt der kardiogene Schock weiterhin mit einer sehr hohen Sterblichkeit vergesellschaftet [4,11], was auch unsere Zahlen mit einer Mortalitätsrate von 52,4% widerspiegeln. Somit wird die mittlere Mortalität eines Zentrums massiv vom Anteil hämodynamisch instabiler, reanimierter und/oder intubierter Patienten beeinflusst.
In der Tat erreichen heute durch die insgesamt verbesserte medizinische Versorgung mit ambulanten Reanimationsteams zahlreiche Patienten nach Herz-Kreislauf-Stillstand tertiäre Zentren. Verschiedene Studien über Patienten mit ACS und Herzkreislaufstillstand, die interventionell behandelt wurden, berichten über Spitalmortalitätsraten zwischen 15% und 60% [5,6]. In unserer Studie lag die Mortalitätsrate bei reanimierten Patienten bei 38,6%, was entsprechend gut mit den in der aktuellen Literatur vorliegenden Zahlen übereinstimmt. Es gilt zu erwähnen, dass es sich bei den oben erwähnten Studien in diesem Gebiet zumeist um retrospektive Arbeiten handelt, in welchen kein Vergleich zwischen Behandlungsregime und Outcome bei ACS-Patienten mit und ohne Reanimation durchgeführt wurde. Des Weiteren liegen häufig auch keine Angaben bezüglich neurologischem Outcome vor.
Von besonderem Interesse ist weiter die Todesursache verstorbener Patienten. Besonders beeindruckend ist die Tatsache, dass trotz hohem Anteil hämodynamisch instabiler Patienten nur 0,3% im Rahmen der Akutintervention verstarben, was die technische Qualität der vorgenommenen Interventionen unterstreicht. Auch die tiefe peri- bzw. postinterventionelle Komplikationsrate zwischen 0,3 bis 1,2% spricht für qualitativ gute Katheterinterventionen im UniversitätsSpital Zürich. Zu beachten ist, dass beim akuten Nierenversagen (4,7%) nicht zwischen einer direkt nephrotoxischen Wirkung des Kontrastmittels während der Intervention und hämodynamisch bedingtem Nierenversagen unterschieden werden kann. Weiterhin ist bemerkenswert und bisher wenig beachtet, dass in mehr alseinem Drittel der Fälle die Patienten nicht aufgrund einer kardialen Ursache, sondern vielmehr im Rahmen einer hypoxischen Enzephalopathie während der Hospitalisation verstarben. Somit sollte besonderes Augenmerk auf eine weitere Optimierung der Prähospitalisierungsphase gelegt werden bzw. die Laienreanimation und Verwendung automatischer Defibrillatoren vermehrt propagiert werden, um den Zeitraum bis zum Eintreffen der Ambulanz zu überbrücken. In der Tat zeigen verschiedene Untersuchungen, dass eine frühe Laienreanimation und/oder Defibrillation für das Überleben von Patienten mit Herzstillstand entscheidend ist. In einer schwedischen Studie mit über 30 000 Patienten mit Herzstillstand ausserhalb des Spitals lag die 30-Tage-Mortalität bei 89,5%, wenn vor dem Eintreffen der Ambulanz eine Laienreanimation stattgefunden hatte und bei 96%, falls nichts unternommen wurde [12]. Eine frühe Defibrillation vor Ort war mit einer mehr als doppelt so hohen Überlebensrate assoziiert. Diese epidemiologisch kompletten Daten, wie sie nur das schwedische Gesundheitssystem zu liefern vermag, zeigen, dass die in Studien und Registern und durch viele Zentren berichteten Mortalitätsraten offensichtlich nicht der Wirklichkeit entsprechen und dass in der Prähospitalisationsphase noch viel, wie vor allem die Verbreitung der Laienreanimation, die Verfügbarkeit von automatischen Defibrillatoren, die Logistik und Neuroprotektion, verbessert werden müsste.
Jährlich werden in der Schweiz sogenannte Qualitätsfaktoren der Schweizer Akutspitäler durch das Bundesamt für Gesundheit (BAG) der Schweiz erhoben (www. bag.admin.ch). Dabei werden anhand eines Kodierungssystems mittlere Mortalitätsdaten von Patienten verschiedener Zentrums- und Bezirksspitäler erstellt und anhand von Fallzahlen sowie Anzahl der Todesopfer bei gewissen Diagnosen (beispielsweise ACS u.a.m.) Rückschlüsse hinsichtlich der Behandlungsqualität eines Spitals gezogen. Betrachtet man nun den bedeutenden Einfluss verschiedener Faktoren auf das Outcome beim ACS, wie in der vorliegenden Studie eindrücklich dokumentiert, so müssen diese Daten aus folgenden Gründen kritisch hinterfragt werden: (1) Die Verteilung hämodynamisch stabiler und instabiler Patienten ist von Zentrum zu Zentrum massiv unterschiedlich und variiert zwischen 0% und 10%; (2) Tertiäre Zentren wie insbesondere das UniversitätsSpital im Raum Zürich haben einen besonders hohen Anteil hämodynamisch instabiler oder reanimierter Patienten (27,4%), was die mittleren Mortalitätsraten beeinflusst; (3) das fehlende Monitoring der Datenerhebung und der verwendeten Kodierung beeinträchtigt die Qualität und Vergleichbarkeit der verschiedenen Da-tenbanken, und damit lässt sich (4) mit den heutigen Zahlen ohne Risikoadjustierung über Alter und Geschlecht hinaus kein sinnvoller Vergleich öffentlicher Mortalitätsdaten machen.
Wenig beachtet wird insbesondere, dass bei den zugrundeliegenden ICD-Kodierungen beim ACS (ICD-10 GM 2015: Kapitel IX Krankheiten des Kreislaufsystems [I20 bis I22]) die hämodynamische Präsentation wenig bis gar nicht erfasst wird, was hinsichtlich Mortalitätsstatistiken und darauf basierenden Beurteilungen der Behandlungsqualität grundsätzlich unabdingbar wäre. Werden Infarktpatienten im Kodierungssystem nicht korrekt erfasst (beispielsweise plötzlicher Herztod anstelle von Infarkt u.a.m.), wird dadurch die Mortalitätsrate signifikant verändert.
Die Veröffentlichung der Outcome-Daten verschiedener Spitäler kann nebst der grundsätzlich sinnvollen Überwachung und Verbesserung der Behandlungsqualität auch unbeabsichtigte und für schwerstkranke Patienten inakzeptable Folgen nach sich ziehen, was in der Literatur unter dem Begriff «avoidance creep» zusammengefasst wird. So nimmt die Bereitschaft, Patienten mit einem hohen Mortalitätsrisiko zu behandeln und somit das Risiko einer weniger guten Outcome-Statistik einzugehen, mit zunehmender Transparenz der Outcome-Daten markant ab, wie Erfahrungen aus den USA zeigen [13,14]. Unsere Daten dokumentieren demgegenüber eindrücklich, dass gerade Patienten mit hohem Mortalitätsrisiko von einer Optimierung der Prähospital-Behandlung sowie des Managements im Zentrum profitieren. Die «avoidance creep»-Denkweise, wie sie eine nicht Risiko-adjustierte Transparenz mit sich bringt, führt daher zu einer Unter-Behandlung derjenigen Patienten, welche am meisten von einer optimalen Behandlung profitieren. Daher scheint es zwingend, dem Komplexitätsgrad der Patienten bei Spitaleintritt respektive vor der Koronarangiographie als wichtig(st)em Parameter in zukünftigen Outcome-Statistiken entsprechende Beachtung zu geben.
Limitationen
Die in dieser Studie analysierten Daten weisen eine differenzierte Beurteilung des Outcomes von ACS-Patienten auf. Dennoch müssen die vorliegenden Resultate auch kritisch begutachtet werden. Methodologisch limitierend ist einerseits die nicht prospektive Datenerhebung. Auch die Tatsache, dass nur die Komplikationen und Todesfälle, die während der Hospitalisation im UniversitätsSpital Zürich aufgetreten sind, analysiert wurden, muss bei der Beurteilung der Resultate berücksichtigt werden, da wir als tertiäres Zentrum Patienten nach erfolgter Intervention oft zur weiteren Betreuung in periphere Spitäler verlegen, so dass die vorliegenden Resultate nicht die gesamte Behandlungsdauer bzw. Events, welche natürlich auch nach Rückverlegung auftreten können, erfassen.