Einleitung
Herz-Kreislauf-Krankheiten stellen in der Schweiz gemäss den Angaben des Bundesamtes für Statistik aus dem Jahre 2010 weiterhin die häufigste Todesursache dar. Der häufigste Risikofaktor der koronaren Herzkrankheit und damit für einen Herzinfarkt ist der Bluthochdruck. Die klinische Bedeutung des Bluthochdrucks wurde früher lange Zeit verkannt [
1]. In den 1950er Jahren wurden erste Medikamente gegen Bluthochdruck eingeführt. Während des zweiten Weltkriegs standen noch kaum Medikamente zur Senkung des Blutdrucks zur Verfügung. In den 1970er Jahrenkonnte dann erstmals gezeigt werden, dass eine Blutdrucksenkung zu einer Reduktion der Häufigkeit von Hirnschlag und Herzinfarkt bei Hypertonikern führt [
2]. Wirksamere und verträglichere Antihypertensiva wie Kalziumantagonisten und ACE-Hemmer wurden ebenfalls in den 1970er Jahren eingeführt. Heute verfügen wir über eine breite Palette von Antihypertensiva, welche bei den meisten Patienten ohne gravierende Nebenwirkungen ermöglichen, Blutdruckwerte um 140/90 mm Hg oder darunter zu erreichen [
2].
Trotz vorhandener wirksamer antihypertensiver Medikamente können einige Patienten mit arterieller Hypertonie allerdings nicht adäquat behandelt werden (sogenannte therapieresistente Hypertonie) [
3]. Eine therapierefraktäre arterielle Hypertonie liegt vor, wenn der Blutdruck trotz antihypertensiver Therapie mit 3 maximal dosierten Medikamenten, davon eines ein Diuretikum, nicht adäquat gesenkt werden kann [
4]. Die Ursachen der therapierefraktären Hypertonie sind vielfältig. Eine sehr wichtige Rolle spielt dabei das sympathische Nervensystem [
3]. Patienten mit essentieller arterieller Hypertonie zeigen eine sehr hohe Aktivität des sympathischen Nervensystems, wobei bei der Entwicklung und Aufrechterhaltung der Hypertonie insbesondere die efferente und die afferente sympathische Innervation der Nieren eine wesentliche Rolle spielen. Die Gesamtaktivität des sympathischen Nervensystems wird in bedeutender Weise durch die afferenten Nervenfasern der Nieren reguliert [
5,
6]. In den 1950er Jahren hat man deshalb bei sehr schwerem Bluthochdruck diese Nerven chirurgisch durchtrennt. Dieser Eingriff hat den Blutdruck und die Mortalität reduziert, war aber mit hohen Nebenwirkungen verbunden und wurde deshalb schnell vergessen, sobald eine medikamentöse Therapie zur Verfügung stand.
Ein neues und vielversprechendes Verfahren zur Behandlung solcher therapierefraktärer Hypertoniker stellt die katheterbasierte renale Sympathikusdenervation dar [
6,
7].
Experimentell konnte bereits seit langem gezeigt werden, dass eine Unterbrechung der afferenten Nerven aus den Nieren über eine verminderte Aktivierung der kardiovaskulären Zentren des Hirnstamms zu beeindruckenden Blutdrucksenkungen führen kann [
6,
8,
9,
10].
Weiter aktivieren efferente sympathische Fasern über Beta-Rezeptoren die Renin-Freisetzung in der Niere, regulieren den Nierenblutfluss und damit die glomeruläre Filtrationsfraktion sowie die Natriumund Wasserausscheidung. Die Aktivierung des efferenten Sympathikusnervs führt somit zu einer Verminderung des renalen Blutflusses und in der Folge zu einer Erhöhung des Blutdrucks [
11,
12].
Verschiedene Studien haben eine blutdrucksenkende Wirkung der renalen Denervation bei Patienten mit therapierefraktärer arterieller Hypertonie beschrieben [
5,
13,
14,
15].
Die vorliegende Studie berichtet über erste Erfahrungen aus zwei Schweizer Zentren.
Methoden und Patienten
Patienten
Zwischen September 2010 und Februar 2013 untersuchten wir 38 Patienten mit therapieresistenter arterieller Hypertonie, bei denen trotz Therapie mit 3 blutdrucksenkenden Medikamenten (davon eines ein Diuretikum, sofern toleriert) in optimaler Dosierung keine adäquate Blutdruckeinstellung mit Werten <140/90 mm Hg zu erzielen war. Die Blutdruckmessung wurde oszillometrisch mit einem automatischen Microlife
®- oder Omron
®-Gerät durchgeführt, entsprechend den gängigen Richtlinien [
4,
16].
Patienten mit Niereninsuffizienz (GFR >45 ml/min) oder mit anatomischen Kontraindikationen für eine renale Nervenablation (Nierenarteriendurchmesser <4 mm, doppelt angelegte Nierenarterien, Nierenarterienstenosen, ermittelt mittels abdomineller Magnetresonanztomographie oder Computertomographie und schlussendlich angiographisch) wurden aus der Studie ausgeschlossen. Zur Beurteilung der Nierenarterienanatomie wurden die Kriterien der multizentrischen Studie «Symplicity HTN-2» [
16] verwendet, d.h. einzeln angelegte Arteria renalis sinistra und dextra mit einer Mindestlänge von 20 Millimetern (Abgang Aorta bis zur ersten Bifurkation) und einem Durchmesser, der grösser ist als 4 Millimeter.
Bei Spitaleintritt zur elektiven renalen Sympathikusdenervation lag der klinisch gemessene Blutdruck trotz Einnahme der verordneten Antihypertensiva bei allen Patienten über 140 mm Hg systolisch (Tab. 1). Am Tag der Intervention wurden die laborchemischen und hämatologischen Routineparameter, entsprechend dem Vorgehen vor einer elektiven Koronarangiographie, nochmals gemessen.
Bei allen Patienten wurden vor dem Eingriff sowie 1, 3, 6 und 12 Monate danach die Laborwerte und der Blutdruck gemessen und eine 24-Stunden-Blutdruckmessung durchgeführt. Die antihypertensive Medikation blieb während mindestens 4 Wochen vor der renalen Nervenablation stabil und wurde während der folgenden Monate möglichst unverändert belassen. Die Therapie wurde adäquat ausdosiert und über Wochen eingesetzt und eine Pseudoresistenz wie eine sekundäre Form wurden ausgeschlossen.
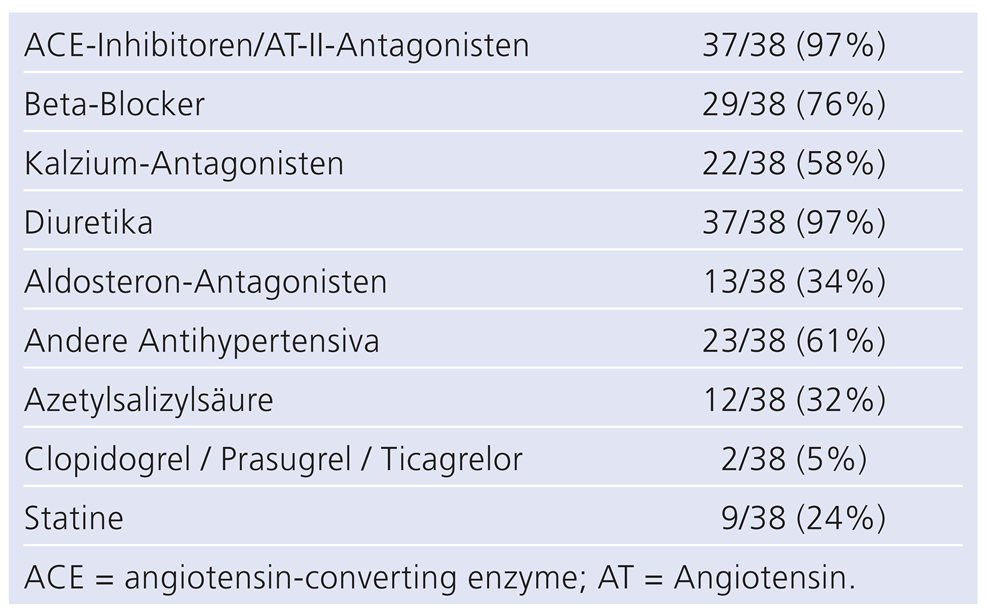
38 Patienten (Alter 61,9 ± 13,4 Jahre, Mittelwert ± SD) mit diagnostiziertem therapieresistentem arteriellem Bluthochdruck wurden eingeschlossen (Tab. 1). Die antihypertensive Medikation bei Studienbeginn ist in Tabelle 2 dargestellt.
Die Daten wurden im Rahmen einer medizinischen Konsultation erhoben und in anonymisierter Form verwendet sowie retrospektiv analysiert.
Eine Einverständniserklärung für die Katheterablation wurde bei allen Patienten vor dem Eingriff eingeholt.
Ausschluss sekundärer arterieller Hypertonie
Vor der Intervention wurden allfällige sekundäre Ursachen einer therapieresistenten Hypertonie ausgeschlossen, und zwar entsprechend den aktuellen Guidelines der Schweizerischen Gesellschaft für Hypertonie [
4,
15]: (1.) Phäochromozytom (Bestimmung des Metanephrins im 24-Stunden-Urin oder der Chromogranin-A im Plasma; Bildgebung der Nebennieren mit Magnetresonanztomographie oder Computertomographie); (2.) Primärer Hyperaldosteronismus (Aldosteronglucoronid im 24-Stunden-Urin, Plasma-Aldosterone und Plasma-Renin-Aktivität bzw. direkte Bestimmung des Renins, Bildgebung der Nebennieren); (3.) Cushing-Syndrom (Plasma-Cortisol und Bildgebung der Nebennieren); (4). Renovaskuläre Hypertonie (Nierenarterien-Duplex, Magnetresonanztomographie oder Computertomographie); (5.) renoparenchymatöse Hypertonie (Plasma-Kreatinin, Urinsediment und Bildgebung der Nieren); (6.) Schilddrüsenfunktionsstörung (Plasma TSH und FT
3/4); sowie (7.) Obstruktives Schlafapnoe-Syndrom (Anamnese und ggf. Schlafstudie) und (8.) Medikamentenanamnese.
Tabelle 1.
Baseline-Charakteristika von 38 Patienten mit therapieresistenter Hypertonie.
Tabelle 1.
Baseline-Charakteristika von 38 Patienten mit therapieresistenter Hypertonie.
Tabelle 2.
Antihypertensive Medikation vor renaler Nierennervenablation.
Tabelle 2.
Antihypertensive Medikation vor renaler Nierennervenablation.
Technik der Nierennervenablation
Die renale Denervation wurde mittels zweier verschiedener Systeme durchgeführt (Symplicity™-RDN (Renal Denervation)-System von Medtronic bei 31 Patienten, EnligHTN™-Multi-Electrode-Renal-Denervation-System von St. Jude Medical bei 7 Patienten).
Die Durchführung der renalen Sympathikusdenervation erfolgte im standardmässig eingerichteten Herzkatheterlabor unter monoplaner Durchleuchtung.
Nach lokaler Anästhesie der vorgesehenen Punktionsstelle erfolgte die Punktion der rechten Arteria femoralis. Mittels Seldinger-Technik wurde dann eine 6- bis 8-French-Schleuse, je nach System, eingeführt. Anschliessend erfolgte erneut die Darstellung der renalen Gefässanatomie zwecks Überprüfung der Eignung der Anatomie der beiden Nierenarterien gemäss bildgebendem Vorbefund. Dann wurde ein 6-oder 8-French-LIMA (left internal mammary artery) oder-Judkins Führungskatheter rechts eingeführt und die Nierenarterie intubiert. Bei Verwendung des Erstgenerationen-Symplicity-Ablationskatheters wurde daraufhin über einen Führungsdraht (BMW, Abbott Laboratories, Illinois, USA) ein 5-F-Multipurpose-Katheter bis zur Bifurkation der Nierenarterie eingeführt. Nach dem Rückzug des Führungskatheters wurde über den liegenden 5-F-Katheter der Simplicity™-Ablationskatheter in der linken bzw. rechten Nierenarterie platziert. Dann wurde der 5-F-Katheter zurückgezogen und ein Kontakt der Spitze des Ablationskatheters mit der Nierenarterienwand hergestellt. Bei Verwendung des Zweitgenerationen-Symplicity-Katheters wurde der Ablationskatheter direkt in die Nierenarterie eingeführt. Bei Verwendung des St.-Jude-Medical-Basket-Katheters wurde der Führungskatheter mittels Telescope-Technik über einen 8-F-Multipurpose-Katheter, der über einen Führungsdraht tief in die Nierenarterie eingeführt wurde, tief intubiert (sogenannte «deepthroat-intubation»).
Vor der Durchführung der Radiofrequenzablation wurden 5000–7000 IU Heparin verabreicht, um eine «activated clotting time» (ACT) von 200–250 s zu erreichen. Da die renale Ablation der afferenten Nerven mit Schmerzen verbunden ist, wurde zu Beginn jeweils eine Analgosedation mit Remifentanil (Ultiva®-Perfusor) oder Morphin und Midazolam (Dormicum®) oder Propofol durch einen Anästhesisten durchgeführt. Um mögliche durch den Ablationsvorgang ausgelöste Gefäss-Spasmen zu vermeiden, wurde zudem Nitroglycerin intraarteriell (0,2 mg) verabreicht.
Die Hochfrequenzenergie wurde durch einen Generator (Symplicity™-Generator, Ardian/Medtronic [EnligHTN™]) oder EnligHTN™-RF-Ablationsgenerator bereitgestellt. Danach erfolgte mit dem Symplicity-System die schrittweise Ablation der rechten und danach der linken Nierenarterie an 4 bis 6 verschiedenen Positionen mit jeweils 5 Millimeter Abstand (im Mittel 6,7 ± 1,4 [R] und 6,0 ± 1,2 [L] Ablatiopositionen). Dazu wurde spiralförmig von distal nach proximal wiederholt lokal Radiofrequenzenergie über 3 Minuten abgegeben. Durch die Erhöhung der lokalen Temperatur auf rund 70 °C kam es zur angestrebten partiellen Zerstörung der sympathischen Nerven. Nach erfolgreicher Ablation konnte angiographisch eine Dissektion oder eine renale Stenosierung der Nierenarterie bei allen Patienten ausgeschlossen werden. Die durchschnittliche Dauer für die gesamte Intervention betrug etwa 60 ± 7 Minuten. Bei Verwendung des St.-Jude-Medical-Katheters wurde eine Ablation in der distalen Nierenarterie und danach – nach 45° Rotation des Basket-Katheters in der proximalen Nierenarterie wiederholt. Die durchschnittliche Dauer für die gesamte Intervention ist damit deutlich kürzer und betrug etwa 45 ± 8 Minuten. Die Patienten konnten jeweils einen Tag nach dem Eingriff nach Hause entlassen werden. Weder kurzfristige noch langfristige Komplikationen traten auf. Es wurde darauf geachtet, dass sich die Medikamenteneinnahme auch in den Folgemonaten nicht änderte.
Statistische Analyse
Als primärer Endpunkt für die Wirksamkeit wurde die Veränderung des vor Ort gemessenen systolischen und diastolischen Blutdrucks nach 3-minütiger Sitzpause 1, 3, 6 und 12 Monate nach dem Eingriff festgelegt. Als sekundäre Endpunkte für die Wirksamkeit wurden die Veränderungen des systolischen und des diastolischen 24-Stunden-Blutdrucks nach 1, 3, 6 und 12 Monaten definiert.
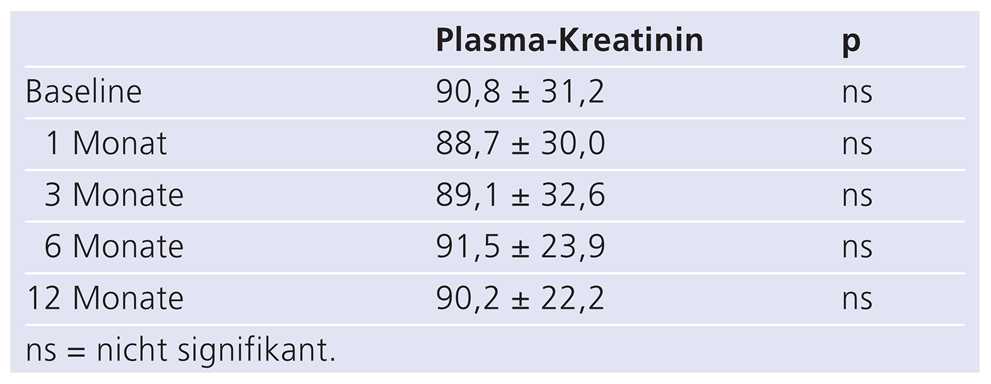
Der primäre Sicherheitsendpunkt war die Veränderung des Plasma-Kreatinin-Spiegels nach 1, 3, 6 und 12 Monaten.
Die Resultate werden als Mittelwerte +/– SD aufgeführt.
Die Werte wurden mittels Student-Zweistichproben-t-Test und mittels univariater Varianzanalyse (ANOVA) mit Messwiederholung analysiert. Für alle statistischen Vergleiche wurde ein zweiseitiges Alpha = 0,05 verwendet, ein Alpha-Wert ≤0,05 wurde als signifikant betrachtet. Die statistische Analyse wurde mit SPSS Version 17.0 durchgeführt.
Tabelle 3.
Systolischer/diastolischer Blutdruckwert in der Praxis und Herzfrequenz während eines 12-monatigen Follow-ups nach Nierennervenablation (Mittelwert ± SD, n = 38).
Tabelle 3.
Systolischer/diastolischer Blutdruckwert in der Praxis und Herzfrequenz während eines 12-monatigen Follow-ups nach Nierennervenablation (Mittelwert ± SD, n = 38).
Resultate
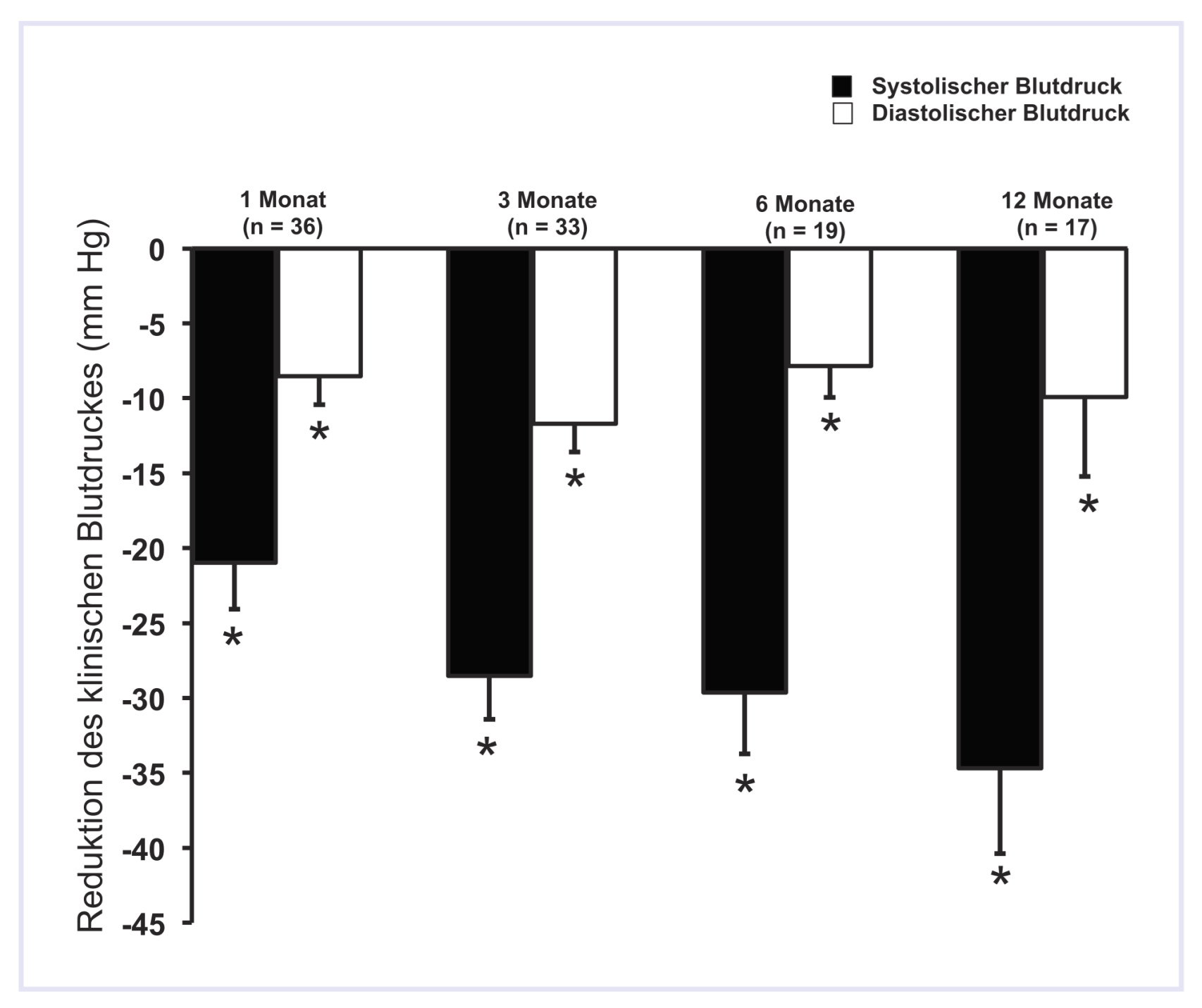
Ein, 3, 6 und 12 Monate nach der renaler Denervation konnte eine signifikante Abnahme des systolischen und diastolischen Blutdrucks beobachtet werden (Tab. 3 und Abb. 1). Der systolische Blutdruckabfall nach 6 und 12 Monaten betrug (Mittelwert ± SD) 29,6 ± 8 mm Hg bzw. 34,7 ± 23,1 mm Hg. Eine patientenbasierte Analyse ergab, dass die Nierennervenablation bei 21/23, 15/19, 14/17 der 38 Patienten nach 3, 6 und 12 Monaten eine Senkung des systolischen Blutdrucks von 10 mm Hg oder mehr bewirkte (Abb. 2).
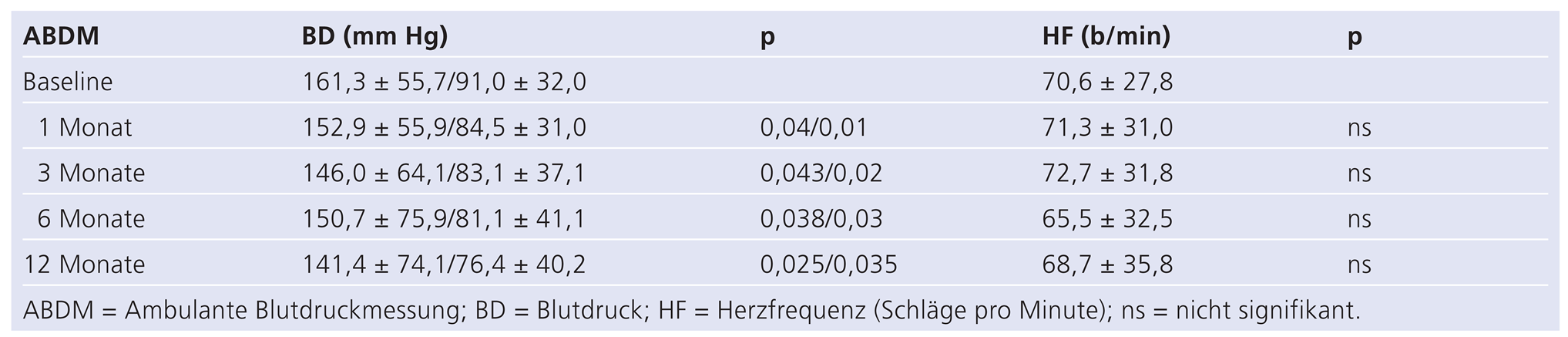
Bei 3 Patienten reduzierte sich der Blutdruck so stark, dass eine Reduktion der antihypertensiven Medikation notwendig wurde. Parallel dazu beobachteten wir eine signifikante Reduktion des 24-Stunden-Blutdrucks in den Folgemessungen (Tab. 4 und Abb. 2).
Diskussion
Die vorliegende Anwendungsstudie bei 38 Patienten mit therapieresistenter Hypertonie bestätigt, dass die katheterbasierte Nierennervenablation in dieser Patientengruppe eine sichere und äusserst wirksame Methode ist, um eine bessere, z.T. optimale Blutdruckeinstellung zu erreichen. In der Tat sank der bei der Arztvisite erhobene systolische und diastolische Blutdruck im Mittel nach 6 Monaten um beeindruckende 29,6 ± 18 mm Hg bzw. 11 ± 2,3 mm Hg. Insgesamt fiel der systolische Blutdruck bei 14 von 17 Patienten nach 12 Monaten um mehr als 10 mm Hg ab (Abb. 2). Die Daten deuten darauf hin, dass die katheterbasierte Nierennervenablation bei der überwiegenden Zahl unserer therapieresistenten Hypertoniker wirksam und sicher war.
Abbildung 1.
Darstellung der Reduktion des klinischen Blutdrucks (mm Hg) nach renaler Denervation. *= p <0,05 vs. Basale.
Abbildung 1.
Darstellung der Reduktion des klinischen Blutdrucks (mm Hg) nach renaler Denervation. *= p <0,05 vs. Basale.
Abbildung 2.
Darstellung der Reduktion des 24-Stunden-Blutdrucks (mm Hg) nach renaler Denervation. *= p <0,05 vs. Basale.
Abbildung 2.
Darstellung der Reduktion des 24-Stunden-Blutdrucks (mm Hg) nach renaler Denervation. *= p <0,05 vs. Basale.
Tabelle 4.
Veränderungen der systolischen und diastolischen 24-Stunden-Blutdruckmittelwerten und der Herzfrequenz (Mittelwert ± SD) nach Nierennervenablation.
Tabelle 4.
Veränderungen der systolischen und diastolischen 24-Stunden-Blutdruckmittelwerten und der Herzfrequenz (Mittelwert ± SD) nach Nierennervenablation.
Die renale Sympathikusdenervation ist ein neues und vielversprechendes Verfahren zur Behandlung einer therapierefraktären arteriellen Hypertonie. Die Methode ist bei entsprechender Erfahrung relativ einfach durchzuführen. In verschiedenen internationalen Registern und kleineren randomisierten Studien [
17,
18,
19,
20,
21,
22] konnte eine sehr vielversprechende Blutdrucksenkung erzielt werden. Unsere Studie steht im Einklang mit anderen Untersuchungen [
15,
21,
23], welche zeigten, dass bei Patienten mit therapieresistentem Bluthochdruck, die mit mindestens drei oder mehr blutdrucksenkenden Medikamenten erfolglos behandelt wurden, eine renale Denervation zu einer signifikanten Reduktion des Praxis- und des 24-Stunden-Blutdrucks führen kann. Besonders bedeutsam ist, dass in unserem Studienkollektiv bei der Mehrheit der Patienten eine signifikante Blutdrucksenkung erreicht wurde. Bei drei Patienten reduzierte sich der Blutdruck gar so stark, dass eine Reduktion der antihypertensiven Medikation notwendig wurde.
Bemerkenswerterweise konnte die renale Denervation bei allen 38 Patienten ohne Komplikationen durchgeführt werden. Dies ist wichtig, da die Ablation in den Nierenarterien akut relevante Läsionen (Ödeme, Endothelerosionen, Intimaablösungen sowie Spasmen und Thrombenbildung) hervorrufen kann [
24]. Auch wurden Nierenarteriendissektionen und Restenosen beschrieben [
6,
25]. Diese guten Ergebnisse zeigen, dass die Intervention in erfahrenen Händen sicher durchführbar ist und generell nur durch ein erfahrenes Team gemacht werden sollte [
4].
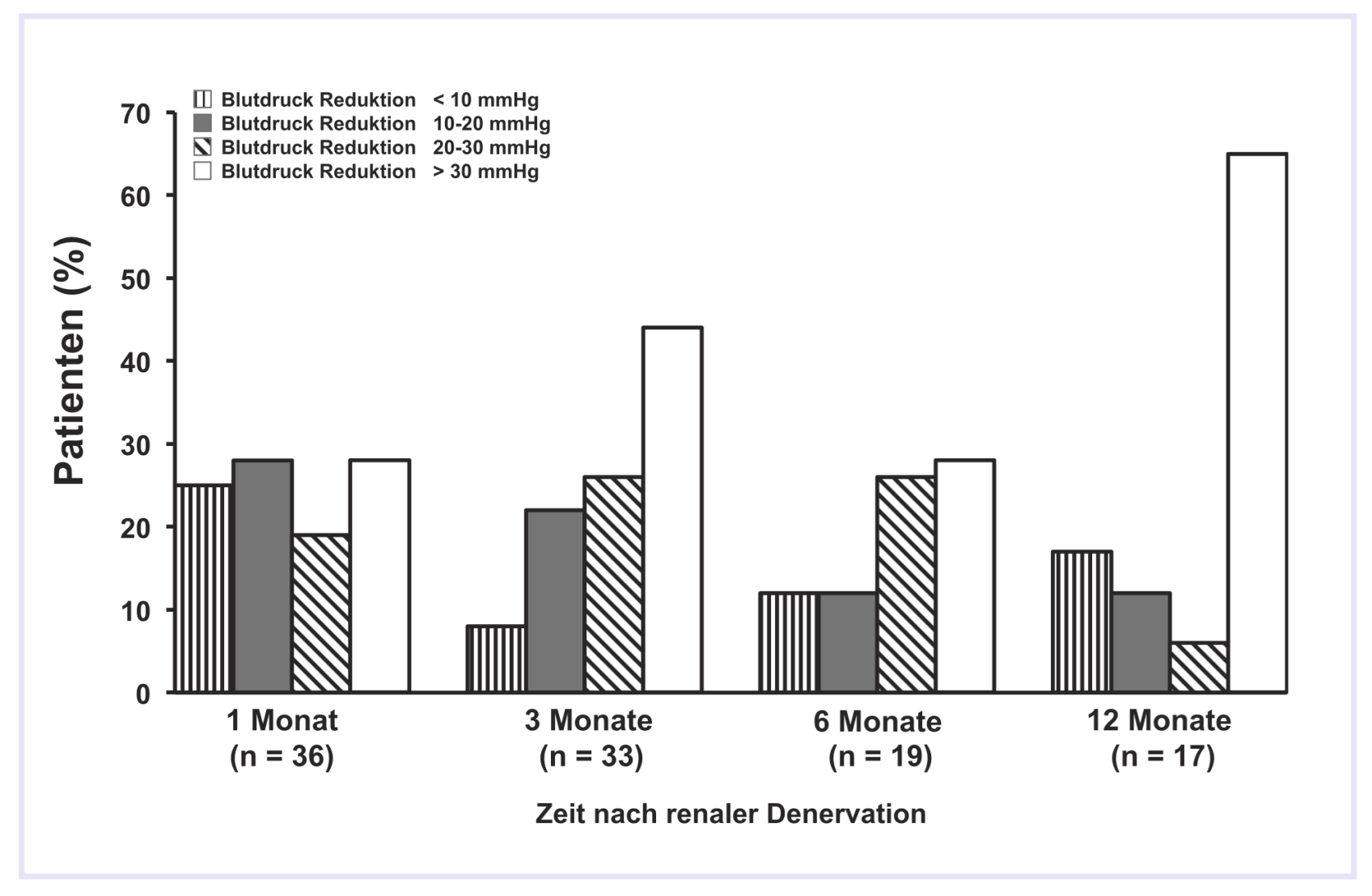
Abbildung 3.
Darstellung der Patienten (in %), die nach einer renalen Denervation eine Blutdruckreduktion von 10, 10–20, 20–30 und mehr als. 30 mm Hg erreichten.
Abbildung 3.
Darstellung der Patienten (in %), die nach einer renalen Denervation eine Blutdruckreduktion von 10, 10–20, 20–30 und mehr als. 30 mm Hg erreichten.
Tabelle 5.
Plasmakonzentrationen des Kreatinins (mmol/l) im Verlauf.
Tabelle 5.
Plasmakonzentrationen des Kreatinins (mmol/l) im Verlauf.
Die Nierenfunktion wird ebenfalls durch die sympathische Innervation geregelt, entweder direkt an den Nierengefässen oder indirekt über die Aktivierung der Renin-Sekretion. Entsprechend ist es wichtig, nach jeder Nierennervenablation zu zeigen, dass sich auch die Nierenfunktion nicht verändert.
Es ist noch nicht bekannt, wie nachhaltig diese Methode wirkt. In der Tat könnten die abladierten sympathischen Nerven nachwachsen und somit den Behandlungseffekt abschwächen oder ganz aufheben, wie dies beispielsweise bei einigen Patienten nach Herztransplantation beobachtet wurde [
26]. Diese Frage lässt sich zurzeit noch nicht sicher beantworten. Langzeitresultate der Symplicity-HTN1 [
22] zeigen allerdings, dass der blutdrucksenkende Effekt der Nierennervenablation über einen postinterventionellen Zeitraum von bis zu 36 Monaten stetig zunimmt. Dies weist darauf hin, dass ein «re-setting» des renalen afferentenefferenten Regelkreises stattfindet, der zu einer langsamen, aber stetig ausgeprägteren Blutdrucksenkung führt. Es bleibt abzuwarten, ob die Wirkungen der Nierennervenablation auch im Langzeitverlauf über mehrere Jahre anhält. Zu untersuchen bleibt auch, wie häufig Narbenstenosen an den abladierten Stellen auftreten [
27].
Eine weitere Sorge bei der Einführung dieser Intervention war das mögliche Auftreten einer orthostatischen Hypotonie [
6]. In der Tat führte die chirurgische Sympathektomie, wie sie vor allem in den 1950er Jahren durchgeführt wurde [
28], zu zum Teil ausgeprägten orthostatischen Blutdruckabfällen [
29]. In unserem Patientenkollektiv konnte bis anhin keine Orthostase-Problematik beobachtet werden. Es scheint, dass die selektive renale Sympathektomie im Gegensatz zur wenig selektiven chirurgischen Sympathektomie nicht mit dieser Nebenwirkung assoziiert ist.
Als mögliche Limitation der Studie zählen die retrospektive Natur der Analyse und die relativ kleine Anzahl von Patienten.
Zusammenfassend zeigen auch unserer Daten, dass sich die katheterbasierte Nierennervenablation bestens für Hypertoniepatienten eignet, bei denen trotz einer 3fachen blutdrucksenkenden Medikation keine optimale Blutdruckeinstellung zu erzielen ist. Sie ermöglicht komplikationslos eine signifikante Reduktion des Blutdrucks. Ob zudem eine Senkung der kardiovaskulären Komplikationen der Hypertonie wie Hirnschlag und Herzinfarkt dokumentiert werden kann, muss durch bereits geplante Multizenterstudien mit mehreren tausend Patienten geklärt werden. Die Metaanalysen grosser Interventionsstudien mit Antihypertensiva weisen allerdings darauf hin, dass die Blutdrucksenkung als solche der wesentlichste Faktor für eine Reduktion der kardiovaskulären Ereignisse darstellt [
30,
31]. Entsprechend akzeptieren sowohl die Federal Drug Administration wie auch die European Medical Agency weiterhin die Blutdrucksenkung als überzeugenden Surrogatendpunkt.