Abstract
Catheter-based aortic valve replacement: an interdisci- plinary intervention. Transcatheter aortic valve intervention (TAVI) is visibly establishing itself as a valid alternative to surgical aortic valve replacement, particularly in high-risk patients. In view of the patient population and the complexity of the intervention, the latter requires close cooperation between cardiologist and cardiac surgeon, ideally in a hybrid operating theatre permanently equipped for angiography. This report illustrates how a real, credible cardiac team is built up and what advantages a properly functioning heart team offers.
Einleitung
Der chirurgische Aortenklappenersatz ist die Therapie der Wahl zur Behandlung einer hochgradigen Aorten- klappenstenose. Entsprechend den aktuellen Leitlinien der nordamerikanischen bzw. europäischen kardiologischen und herzchirurgischen Gesellschaften ist ein chirurgischer Aortenklappenersatz spätestens dann indiziert, wenn der Patient symptomatisch ist [1]. Jedoch kann auch bei Vorliegen einer asymptomatischen hochgradigen Aortenklappenstenose nach Risikostratifizierung ein Klappenersatz indiziert sein [2]. Die derzeitige Technik des chirurgischen Aortenklap- penersatzes beinhaltet eine mediane Sternotomie oder im Falle eines minimalinvasiven Zuganges eine late- rale Minithorakotomie im 2. oder 3. Interkostalraum rechts bzw. eine obere Ministernotomie. Anschliessend wird unter Verwendung der Herz-Lungen-Maschine die Aorta ascendens ausgeklemmt und das Herz still-gelegt. Die Aorta wird eröffnet, die verkalkte Aortenklappe unter kontrollierten Bedingungen reseziert und durch eine biologische oder mechanische Klappenprothese ersetzt. Die Fixierung der Prothese erfolgt unter Sicht durch Einnähen, wodurch eine suffiziente, abdichtende Verankerung der Prothese im Aortenannulus sichergestellt werden kann. Individuelle anatomische Variationen und zusätzliche Erkrankungen an der Aorta lassen sich direkt beurteilen und ggf. chirurgisch mitbehandeln. Ebenfalls erlaubt der chirurgische Eingriff, dass zusätzlich notwendige Eingriffe am Herzen (andere Herzklappen oder Koronargefässe) gleichzeitig durchgeführt werden können.
Die Resultate des chirurgischen Aortenklappenersatzes sind sehr gut dokumentiert und weisen heute eine Sterblichkeitsrate aller Patienten mit isolierter Aortenstenose von nur mehr 2–3% auf [3]. Ebenfalls eingeschlossen sind Patienten mit hohem Risiko, die entweder viele Komorbiditäten oder ein Alter >80 Jahren aufweisen. Wie verschiedentlich gezeigt wurde, ist das Langzeitüberleben nach chirurgischem Aortenklappenersatz bei Patienten über 80 Jahren sehr gut. In der Studie von Varadarajan und Kollegen konnte gezeigt werden, dass das mediane 5-Jahres-Überleben der über 80-Jährigen nach Aortenklappenersatz 69% beträgt, was etwa derjenigen der Normalbevölkerung entspricht [4].
Nichtsdestotrotz scheint der katheterbasierte Aorten- klappenersatz (transcatheter aortic valve implantation [TAVI]) als neue Modalität die therapeutischen Optionen des Managements der schweren Aortenklap- penstenose vor allem bei Patienten mit hohem Operationsrisiko zu erweitern und bei betagten Hochrisiko- patienten gewissermassen zu revolutionieren. Dieser Tatsache müssen sich die Chirurgen stellen, die bis anhin als einzige in der Lage waren, diese Patienten adäquat behandeln zu können. Dieses Wissen kann und muss bei der Indikationsstellung und auch in die Verwendung von katheterbasierten Klappeninterventionen einfliessen, was die Resultate und die Akzeptanz bei Patienten als auch bei den Zuweisern deutlich verbessert. Diese interdisziplinäre Zusammenarbeit trägt dazu bei, dass diese doch zukunftsweisende Technologie weiter expandieren kann.
Momentaner Stand der TAVI weltweit
Vier kommerziell erhältliche TAVI-Systeme werden momentan weltweit eingesetzt: die Sapien XT (Edwards Lifesciences, Irvine, USA) (Abb. 1), die Core-Valve® (Medtronic, Minneapolis, USA) (Abb. 2), die Symetis Acurate™ TA (Symetis SA, Schweiz) (Abb. 3) und die Jena Valve (JenaValve Technology, Deutschland) (Abb. 4), wobei die letzten zwei Klappen momentan nur für den transapikalen Zugang zu Verfügung stehen. Wahrscheinlich sind bis dato in über 30 Ländern mehr als 25 000 Patienten weltweit behandelt worden. Einige Länder, allen voran Deutschland, gelten als fast adopters der TAVI-Technologie und laut des nationalen TAVI-Registers in Deutschland werden momentan etwa 30% aller Aortenklappenersatzoperationen mittels Katheter durchgeführt. In der Schweiz hingegen, wie auch in den meisten anderen europäischen Ländern, werden die Indikationen für TAVI noch vorsichtiger und selektionierter gestellt, nichtdestotrotz steigt auch hier die Prozentrate deutlich an. Nur erahnen lässt sich der Anstieg der TAVI, wenn die Indikations- stellung von Hochrisikopatienten zu Patienten mit einem mittelgradigen Risiko erweitert wird, nur aus Gründen der schnelleren Rehabilitation.
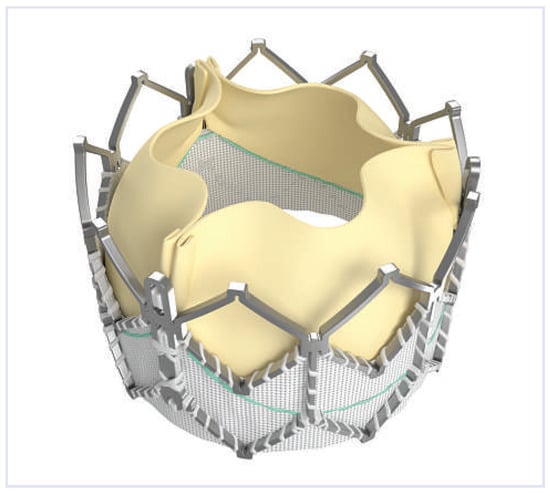
Abbildung 1.
Edwards Sapien XT aus bovinem Perikard (© Edwards Lifesciences, Irvine, USA. Nachdruck mit freundlicher Genehmigung).
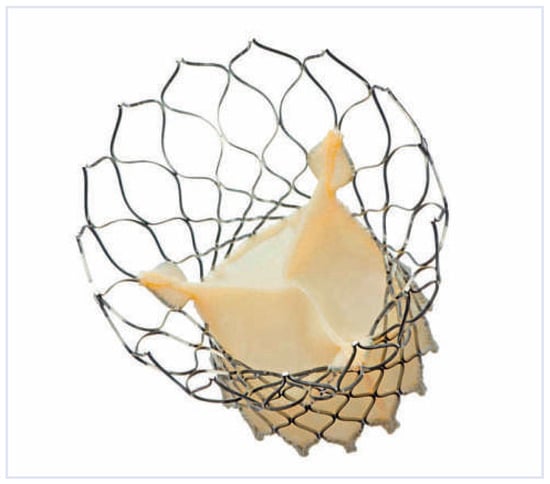
Abbildung 2.
Medtronic CoreValve® aus porcinem Perikard (© Medtronic Schweiz AG, Münchenbuchsee, Schweiz. Nachdruck mit freundlicher Genehmigung).

Abbildung 3.
Symetis Acurate™ TA aus porciner Klappe (© Symetis, Ecublens SA, Schweiz. Nachdruck mit freundlicher Genehmigung).

Abbildung 4.
JenaValve aus porciner Klappe und Perikard (© JenaValve Technology GmbH, München, Deutschland. Nachdruck mit freundlicher Genehmigung).
Gegenwärtig sind TAVI-Eingriffe mit einer 30-Tages-Mortalitätsrate von <10% weltweit assoziiert, wobei sie etwas höher liegt, wenn ein transapikaler Zugang gewählt wurde, was mit dem noch risikoreicheren Patientengut zusammenhängt [5]. Die hämodynamischen Auswirkungen der TAVI können bezüglich Aufhebung des Aortenklappengradienten und der Symptome als exzellent bezeichnet werden. Hingegen bleibt häufig wegen des im Annulus verbleibenden Kalkes eine paravalvuläre Aorteninsuffizienz zurück, die im Ausmass meist leicht ist, deren Langzeitverlauf aber noch genauer beobachtet werden muss [6]. Die Klappe kann über vier Zugangswege in den nativen Aortenannulus bzw. in die degenerierte Aortenklap- penprothese eingebracht werden: direkt über die Herz-spitze (transapikal), über die Leiste (transfemoral), falls die Gefässgrösse der Beckenarterien dies erlaubt, sowie alternativ über die A. subclavia (trans-subclavia) oder direkt über die Aorta ascendens (transaortal) mittels rechtsseitiger anterolateraler Minithorakotomie oder Ministernotomie. Die vaskulären Komplikationen durch das transfemorale Einführen der grosslumigen Schleusen, die in bis zu 30% der Fälle vorkommen, haben nachgewiesenermassen einen grossen Einfluss auf das Überleben der Patienten [7,8]. Durch die kontinuierliche Verkleinerung der Katheter und Schleusen als auch durch die gemachten Erfahrungen konnte die Komplikationsrate im Verlaufe der Zeit jedoch deutlich gesenkt werden. Eine andere gefürchtete Kompli- kation ist der Hirnschlag, der sowohl beim transfemoralen, jedoch etwas seltener auch beim transapikalen Zugang vorkommt. Die meisten Studien zeigen eine klinische Hirnschlagrate von 3–10% [9]. In einer kürzlich publizierten MRI-Studie konnte nachgewiesen werden, dass bei über 84% der TAVI-Patienten Diffusionsstörungen im Hirn durch neue Läsionen vorkommen, die jedoch klinisch meist stumm verlaufen [10]. Eine weitere Komplikation der TAVI sind die AV-Blockierungen, die bei den selbstexpandierenden Systemen (CoreValve®) häufiger vorkommen (bis zu 29%) als bei den ballondilatierbaren Klappen (Sapien XT), so dass die Kosten der schon sehr teuren Prozeduren durch die notwendige Schrittmacherimplantation noch weiter steigen [11,12]. Weitere seltene Komplikationen, die während einer TAVI auftreten können, sind eine Koronarokklusion, Ventrikelruptur, Aortenannulusruptur, Aortendissektion, kardiogener Schock und Embolisation der Klappen ventrikelwärts oder in die Aorta. All diese Komplikationen sind potentiell letal, können jedoch konventionell chirurgisch behandelt werden. Deswegen ist es vor der TAVI wichtig, mit diesen Hochrisiko- und zum Teil inoperablen Patienten genau zu besprechen, inwieweit bei Auftreten einer schweren Komplikation noch chirurgisch interveniert werden soll.
Das Herzteam
Beim Aufbau eines Herzteams müssen der interventionelle Kardiologe und der Herzchirurg eine kollaborative Partnerschaft eingehen, damit nicht nur die technische, sondern auch die klinische und ethische Expertise aus beiden Kulturen eingebracht werden kann. In diesem Artikel beschreiben wir die Rolle des Chirurgen in einem Herzteam, der nicht nur eine unvoreingenommene klinische Beurteilung des Behandlungsteams garantiert (da er das gesamte Behandlungsspektrum anbieten kann), sondern auch durch sein anatomisches und physiologisches Verständnis sowie der zusätzlichen technischen Expertise, dieser neuen Therapieform zum Erfolg verhelfen kann.
Vorgehen einer TAVI-Intervention
Nicht nur die generelle Akzeptanz der Methode, sondern auch die Art und Weise und wie das Team zusammenstellt wird, welches die Interventionen durchführt, unterscheidet sich von Land zu Land und von Zentrum zu Zentrum. Die transfemoralen Interventionen können entweder in Lokalanästhesie als auch in Allgemei- nanästhesie durchgeführt werden, auch jeweils abhängig davon, wie wichtig eine transösophageale Echokar- diographie während der Implantation für die Operateure ist. Ebenfalls kann der Leistenzugang voll perkutan oder mittels chirurgischer Freilegung der Femoralgefässe gemacht werden. Was in den jeweiligen Zentren vorgezogen wird, hängt vom durchführenden Team ab und basiert meistens auf den eigenen Erfahrungen. Ebenfalls variiert die Rolle des Chirurgen stark und ist abhängig von den jeweiligen institutionellen Begebenheiten und den persönlichen Charakteren der involvierten Ärzte des entsprechenden Zentrums. Das Spektrum erstreckt sich vom primären Operateur bis hin zum Chirurgen, der erst dann einschreitet, wenn not- fallmässig chirurgisch eingegriffen werden muss. Jedoch nur durch eine partnerschaftliche Zusammenarbeit zwischen Kardiologen und Herzchirurgen kann diese neue Technologie den grösstmöglichen Erfolg bezüglich Überleben und Lebensqualität der Patienten, Akzeptanz bei den Zuweisern und Kosteneffizienz haben.
Diese enge Zusammenarbeit zwischen Kardiologen und Herzchirurgen bedingt natürlich, dass interven- tionelle Klappeninterventionen nur an denjenigen Zentren angeboten werden sollten, die auch eine Herzchirurgie im Hause haben, was auch den Richtlinien der Europäischen Kardiologen- und Herzchirurgen- gesellschaften (ESC-EACTS) entspricht.
Vorteile eines TAVI-Teams
Da es sich bei den TAVI um Prozeduren mit potentiell hohem Risiko handelt, welche zudem mit hohen Kosten verbunden sind, ist schon die Wahrnehmung einer voreingenommenen Indikationsstellung durch die involvierten Ärzte bei den Patienten als auch Zuweisern und Spitälern sicherlich unerwünscht. Deshalb ist es zwingend notwendig, dass es bei der Auswahl der the- rapeutischen Verfahren zu einer ehrlichen Güterabwägung innerhalb eines kompetenten und interdisziplinären Teams kommt. Dies sollte zur Folge haben, dass nur für diejenigen Patienten TAVI gewählt wird, bei welchen nach bestem Wissen und Gewissen der klinische Nutzen dieser Methode optimal ist, und nicht nur weil es eine Alternative zu einer offenen Operation darstellt. Unsere Erfahrung am Universitätsspital Zürich zeigt, dass uns gerade wegen dieser konsequent durchgeführten Praxis des interdiziplinären TAVI- Teams grosses Vertrauen von den Zuweisern entgegen- gebracht wird. Dieses Vertrauen basiert darauf zu wissen, dass für ihren Patienten die für ihn beste Behandlungsmethode gewählt wird.
Seit der Einführung des TAVI-Programms am Universitätsspital Zürich besteht ein Herzchirurgen-Kardiologen-Team, in welchem die einzelnen Ärzte nicht nur in der Abklärung von Patienten, Indikationsstellung und in der Nachbetreuung, sondern auch in der Ausführung der kathetertechnischen Interventionen gleichgestellt sind. Dies führt dazu, dass dem Patienten beide therapeutischen Optionen unvoreingenommen und offen erklärt werden können, um sogenannte «ad-hoc»-TAVI zu verunmöglichen. Ein solches TAVI- Team hat sich bei uns äusserst gut bewährt, denn es bringt nicht nur eine hohe Glaubwürdigkeit eines solchen Programms bei internen und externen Zuweisern entgegen, sondern führt auch innerhalb des Teams zu einem deutlich besseren Bewusstsein über die potentiellen klinischen und technischen Komplikationen. Dies führt besonders in Situationen mit ungünstigem Ausgang zu einer generell besseren Akzeptanz und Identifikation im gesamten Team [13].
Entsprechend haben wir in unserem Zentrum eine interdisziplinäre Konferenz eingerichtet, in welcher Hochrisiko-Patienten mit Aortenklappenerkrankun- gen einmal wöchentlich besprochen werden. An dieser Konferenz nehmen regelmässig mindestens zwei Herzchirurgen und zwei interventionelle Kardiologen teil, wobei einer der Chirurgen und einer der Kardiologen idealerweise nicht aktiv im Katheterprogramm mitmachen sollten, um eine neutrale Stimme zu repräsentieren. Vervollständigt wird die Gruppe durch einen Herzanästhesisten und einen nicht-interventionellen Kardiologen, der eine besondere Expertise in der Echokardiographie ausweisen kann. Alle Patienten, die für eine Transkatheterklappenintervention in Frage kommen, werden in dieser Konferenz besprochen, und die Empfehlungen werden dokumentiert und den Patienten und zuweisenden Ärzten kommuniziert. Die Selek- tionskriterien für eine kathetertechnische Intervention bei Hochrisikopatienten sind bei uns variabel, jedoch hat der Chirurg das letzte Wort für oder gegen eine bestimmte Methode.
Alle kathetertechnischen Klappeninterventionen werden routinemässig in unserem Hybrid-Operationssaal durchgeführt, der im April 2011 offiziell in Betrieb genommen wurde und heute europaweit als einer der modernsten gilt (Abb. 5). Unser Programm haben wir so ausgelegt, dass alle Team-Mitglieder zwischen first operator und second operator rotieren, so dass über das Jahr verteilt jeder gleich viele Implantationen als first operator durchführen kann. Dies schliesst natürlich nicht aus, dass schwierige kathetertechnische Passagen oder im Notfall Koronarobstruktionen als auch Ge- fässoder Apexzugänge bzw. Verletzungen nicht durch die jeweiligen Spezialisten versorgt werden sollten. Alles andere kann vom Kardiologen oder Herzchirurgen, alternierend ausgeführt werden, um Routine in allen Schritten der Implantation zu erlangen. Dieser Grundsatz führt gleichsam auch zu einem verbesserten Lerneffekt innerhalb des Teams, da es sich für alle um eine gänzlich neue Methode handelt. Der Vorteil bei dieser Zusammensetzung des Teams besteht darin, dass sowohl der Kardiologe als auch der Herzchirurge verschiedene Fähigkeiten und Erfahrungen einbringt, so dass ein sofortiges Feedback während der Intervention möglich ist. Die Expertise der Gefässpunktion, Drahtwahl, die Drahtführung und die Handhabung der Fluoroskopie liegt bei dem Kardiologen. Bei dem Herzchirurgen liegt die Erfahrung im anatomischen Verständnis der Aortenklappe, Aortenwurzel und der angrenzenden Strukturen sowie im offenen Zugang zu den Gefässen und der Herzspitze. Bei einem eingespielten Team sollte jedes Mitglied als first operator und als second operator problemlos eingesetzt werden können, so dass die anfänglichen intrinsischen Unterschiede beinahe gänzlich verschwinden. Dieser Zustand führt zu einer äusserst privilegierten Position des Herzteams, in dem die technischen als auch die Wissenskompetenzen aller Mitglieder optimal genutzt werden, damit ein unvoreingenommener Umgang mit dieser neuen Technologie möglich ist.
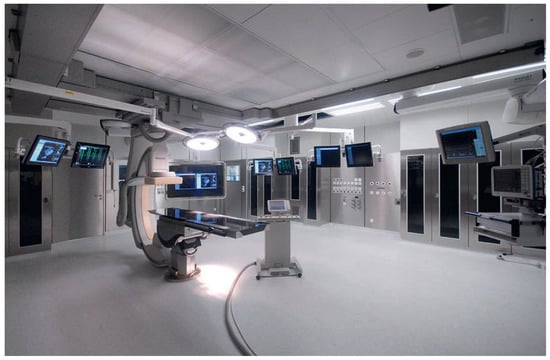
Abbildung 5.
Hybrid-Operationssaal im Universitätsspital Zürich.
Zusammenfassung
Das gut funktionierende Herzteam mit Herzchirurgen, Kardiologen und Herzanästhesisten stellt eine moderne Arbeitsgruppe von ausgewiesen Fachkräften dar, das sich an die neuzeitlichen, komplexen und schnellwandelden Therapieformen im Bereiche der kardiovaskulären Medizin am besten anpassen kann. Durch diesen team approach ist nicht nur eine bessere Behandlung der schweren Aortenstenose bei Hochrisi- kopatienten möglich, sondern es führt auch zu einer verbesserten Auswahl der Patienten für eine gewisse Therapieform (medikamentös, TAVI, Chirurgie), was letztlich zu einer besseren Zufriedenheit bei Patienten, Angehörigen und Zuweisern führt. Solche Herzteams wären ohne das Aufkommen der TAVI in dieser Art nicht möglich gewesen, könnten jedoch ohne weiteres auch auf andere Bereiche in der kardiovaskulären Medizin übertragen werden (koronares Revaskularisationsteam, Herzinsuffizienzteam, Rhythmusteam).
Funding/potential competing interests
Volkmar Falk (consultant for Edwards, Medtronic). No other potential conflict of interest relevant to this article was reported.
Literatur
- Vahanian, A.; Baumgartner, H.; Bax, J.; Butchart, E.; Dion, R.; Filippatos, G.; et al. ECS Committee for practice guidelines. Guidelines on the management of valvular heart disease: the Task Force on the management of valvular heart disease of the European Society of Cardiology. Eur Heart J 2007, 28, 230–268. [Google Scholar] [PubMed]
- Baumgartner, H. Aortic stenosis: medical and surgical management. Heart 2005, 91, 1483–1489. [Google Scholar] [CrossRef] [PubMed]
- Brown, J.M.; O’Brien, S.M.; Wu, C.; Sikora, J.A.; Griffith, B.P.; Gammie, J.S. Isolated aortic valve replacement in North America comprising 108,687 patients in 10 years: changes in risks, valve types, and outcomes in the Society of Thoracic Surgeons National Database. J Thorac Cardiovasc Surg 2009, 137, 82–90. [Google Scholar] [CrossRef] [PubMed]
- Varadarajan, P.; Kapoor, N.; Bansal, R.C.; Pai, R.G. Survival in elderly patients with severe aortic stenosis is dramatically improved by aortic valve replacement: results from a cohort of 277 patients aged > or = 80 years. Eur J Cardiothorac Surg 2006, 30, 722–727. [Google Scholar] [CrossRef] [PubMed]
- Rodés-Cabau, J.; Webb, J.G.; Cheung, A.; Ye, J.; Dumont, E.; Feindel, C.M.; Osten, M.; et al. Transcatheter aortic valve implantation for the treatment of severe symptomatic aortic stenosis in patients at very high or prohibitive surgical risk: acute and late outcomes of the multicenter Canadian experience. J Am Coll Cardiol 2010, 16, 1080–1090. [Google Scholar] [CrossRef] [PubMed]
- Clavel, M.A.; Dumont, E.; Pibarot, P.; Doyle, D.; De Larochellière, R.; Villeneuve, J.; et al. Severe valvular regurgitation and late prosthesis embolization after percutaneous aortic valve implantation. Ann Thorac Surg 2009, 87, 618–621. [Google Scholar] [CrossRef] [PubMed]
- Van Mieghem, N.M.; Nuis, R.J.; Piazza, N.; Apostolos, T.; Ligthart, J.; Schultz, C.; et al. Vascular complications with transcatheter aortic valve implantation using the 18 Fr Medtronic CoreValve System: the Rotterdam experience. EuroIntervention 2010, 5, 673–679. [Google Scholar] [CrossRef] [PubMed]
- Kahlert, P.; Al-Rashid, F.; Weber, F.; Wendt, D.; Heine, T.; Kottenberg, E.; Tet, a.l. Vascular access site complications after percutaneous transfemoral aortic valve implantation. Herz 2009, 34, 398–408. [Google Scholar] [CrossRef] [PubMed]
- Dworakowski, R.; MacCarthy, P.A.; Monaghan, M.; Redwood, S.; El-Gamel, A.; Young, C.; et al. Transcatheter aortic valve implantation for severe aortic stenosis – a new paradigm for multidisciplinary intervention: a prospective cohort study. Am Heart J 2010, 160, 237–243. [Google Scholar] [CrossRef] [PubMed]
- Kahlert, P.; Knipp, S.C.; Schlamann, M.; Thielmann, M.; Al-Rashid, F.; Weber, M.; et al. Silent and apparent cerebral ischemia after percutaneous transfemoral aortic valve implantation: a diffusion-weighted magnetic resonance imaging study. Circulation 2010, 121, 870–878. [Google Scholar] [CrossRef] [PubMed]
- Tchetche, D.; Dumonteil, N.; Sauguet, A.; Descoutures, F.; Luz, A.; Garcia, O.; et al. Thirty-day outcome and vascular complications after transarterial aortic valve implantation using both Edwards Sapien and Medtronic CoreValve bioprostheses in a mixed population. EuroIntervention 2010, 5, 659–665. [Google Scholar] [CrossRef] [PubMed]
- Bleiziffer, S.; Ruge, H.; Hörer, J.; Hutter, A.; Geisbüsch, S.; Brockmann, G.; et al. Predictors for new-onset complete heart block after transcatheter aortic valve implantation. JACC Cardiovasc Interv 2010, 3, 524–530. [Google Scholar] [CrossRef]
- Ruel, M.; Dickie, S.; Chow, B.J.; Labinaz, M. Interventional valve surgery: building a team and working together. Semin Thorac Cardiovasc Surg 2010, 22, 145–149. [Google Scholar] [CrossRef]
© 2012 by the author. Attribution - Non-Commercial - NoDerivatives 4.0.