Fibrillation auriculaire: un énorme challenge
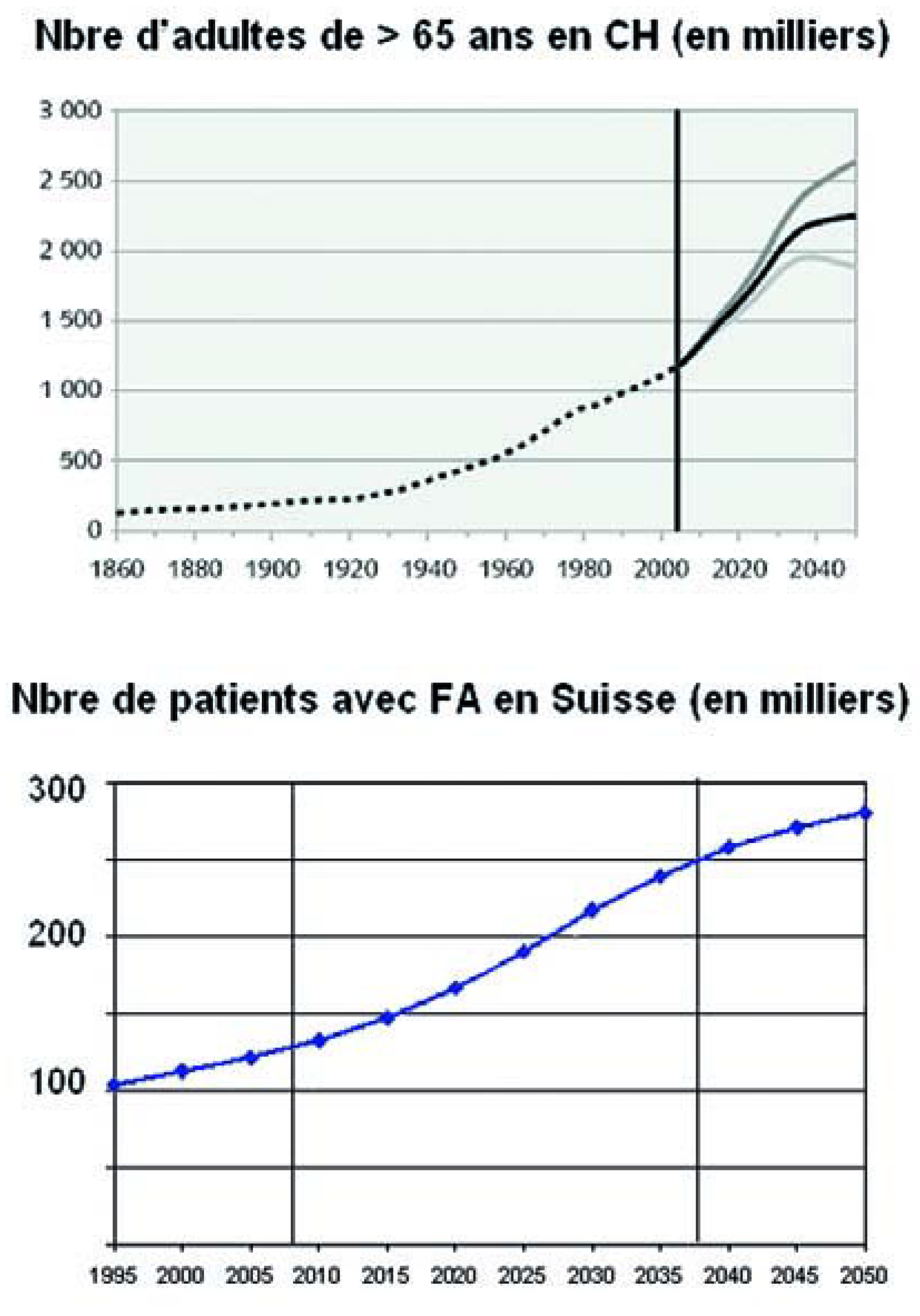
Au vu du vieillissement de la population, la prévalence de la fibrillation auriculaire (FA) en Suisse pourrait doubler ces trente à quarante prochaines années, selon une évaluation à partir des projections américaines et des données de l’Office Fédéral de la Statistique (
Figure 1). La FA est une cause fréquente d’accident vasculaire cérébral et d’insuffisance cardiaque et a des répercussion importante sur la morbidité et le pronostic des patients atteints. Elle est une fréquente cause d’hospitalisation et génère des coûts financiers importants. Vu sa prévalence croissance et à ses conséquences, la FAconstitue un des défis de la médecine ces prochaines années.
De nombreux espoirs sont placés dans différentes stratégies de prévention de la FA (
upstream strategies,
Table 1). L’efficacité de ces mesures n’est pas encore démontrée, mais de nombreuses études ont récemment été entreprises ou sont planifiées ces prochaines années.
Le blocage du système rénine angiotensine est parmi les stratégies les plus prometteuses [
1]. Les inhibiteurs de l’enzyme de conversion et les antagonistes de l’angiotensine II diminuent la fibrose à l’origine des troubles de conduction intra-auriculaire favorisant le maintien de la FA. La diminution de la pression intra-auriculaire joue probablement un rôle bénéfique, notamment chez les patients insuffisants cardiaques et hypertendus. Deux sous-analyses de l’étude LIFE suggèrent que le blocage du système rénine angiotensine permet d’une part de diminuer l’incidence de la FA chez des patients hypertendus, et d’autre part de réduire le risque d’accident vasculaire lié à la FA [
2,
3]. Ces résultats cliniques se sont ajoutés à de nombreuses observations expérimentales et cliniques démontrant l’effet favorable de l’inhibition du système rénine angiotensine [
1,
4]. De futures études devraient montrer si les inhibiteurs peuvent diminuer le risque de FA en l’absence d’hypertension ou d’insuffisance cardiaque. L’étude ANTIPAF (Angiotensin II-Antagonist in Paroxysmal Atrial Fib Trial) analysera l’effet de l’olmésartan sur les taux de récidive d’arythmie chez des patients avec FA paroxystique. L’étude ACTIVE-I (AF Clopidogrel Trial with Irbesartan for prevention of Vascular Events) permettra de comparer l’effet de l’irbésartan au placebo chez des patients hypertendus. De plus, l’étude ONTARGET nous montrera si l’adjonction de telmisartan au traitement d’inhibition de l’enzyme de conversion diminue le risque de FA chez les hypertendus. Le rôle des antagonistes de l’aldosterone, des statines, et des gluco-corticoïdes dans la diminution de la FA chez des populations à risques est également en cours d’évaluation. L’effet anti-inflammatoire et anti-oxydant des statines peuvent prévenir le remodeling auriculaire favorisant la FA. Les statines pourraient jouer un rôle dans le maintien en rythme sinusal lors du traitement de la FA. Dans les traitements non anti-arythmiques qui se sont récemment avérées efficaces, il faut noter la ventilation positive chez les patients souffrant d’un syndrome des apnées du sommeil. Le sport intensif chez l’adulte de plus de 40 ans semble être un facteur de risque pour la FA, et il sera important de déterminer comment ce risque peut être évité ou réduit.
Les anti-arythmiques actuellement à disposition sont limités par leur effet insuffisant et/ou par leur toxicité. La toxicité cardiaque est avant tout due à l’effet pro-arythmique et le risque de bradycardie. L’amiodarone se démarque des autres agents par le faible risque pro-arythmique. Cependant, de multiples effets non cardiaques limitent son utilisation. La dronédarone, analogue déiodé de l’amiodarone, ne semble pas avoir une efficacité comparable à celle de l’amiodarone, mais il n’existe aucune étude comparant les deux agents. L’usage de certains nouveaux composés, comme l’azimilide et la dofétilide (non commercialisé en Europe), restera certainement limité à cause de leur potentiel arythmogène [
5]. Ces agents sont des bloqueurs des courants I
Kr, comme le sotalol; ils prolongent la repolarisation dans le ventricule, allongent le QT, et augmentent le risque de torsades de pointes.
Les agents anti-arythmiques en évaluation les plus intéressants sont les bloqueurs de canaux ioniques inhibant les courants I
Kur (ultrarapid delayed rectifier current), I
TO (transient outward current) et I
KACh [
6,
7]. Ces agents prolongent la repolarisation sélectivement au niveau auriculaire, et sont dépourvus d’effet sur les ventricules. Le courant I
Kur est médié par les sous-unités Kv1,5, qui sont absentes dans les ventricules. Il existe plusieurs composés en évaluation, dont un composé de Sanofi-Aventis AVE0118 et le Xention. Ces agents ont également une action faible sur les courants I
TO et I
KACh. Le blocage des canaux Kv4,3 (courant I
TO) permet également la prolongation de la période réfractaire sélectivement au niveau auriculaire. Une autre cible potentielle est le blocage des canaux
Kir3,1/3,4, eux aussi absents des ventricules, et qui sont médiateurs du courant IKACh au niveau auriculaire. Ce courant est actif lors de la stimulation para-sympathique, qui raccourcit la période réfractaire auriculaire et favorise la FA. D’autres agents en développement incluent le tédisamil, agissant sur plusieurs canaux ioniques différents, des agents augmentant la conductibilité de certaines connexines, et des antagonistes des récepteurs à la sérotonine. Pour que ces agents s’imposent dans le traitement de la FA, il faut que leur efficacité soit démontrée, comparée à celle des médicaments connus, et avant tout que l’absence d’effets secondaires dangereux soit établie. Dans l’attente, ce sont les alternatives non médicamenteuses qui se développent à grande vitesse.
La thermo-ablation de la fibrillation auriculaire permet une amélioration dramatique des symptômes chez la majorité des patients. Les résultats sont durables et il est fort probable que cette approche permette un traitement définitif [
8,
9]. Dans la fibrillation auriculaire paroxystique, la thermo-ablation permet des taux de succès chez plus de 80% des patients, pour autant que l’on pratique une deuxième intervention en cas de récidive, c’est-à-dire chez 20–40% des patients. Dans la fibrillation persistante, les résultats sont semblables, pour autant que le patient ne présente pas de cardiopathie importante ou de dilatation sévère de l’oreillette gauche. Cependant, l’intervention est plus complexe, car des lésions supplémentaires doivent être appliquées (par exemple ligne du toit de l’oreillette, défragmentation peri-ostiale, septale, du plancher de l’oreillette, ou ablation ciblée des potentiels multifragmentés, etc.) [
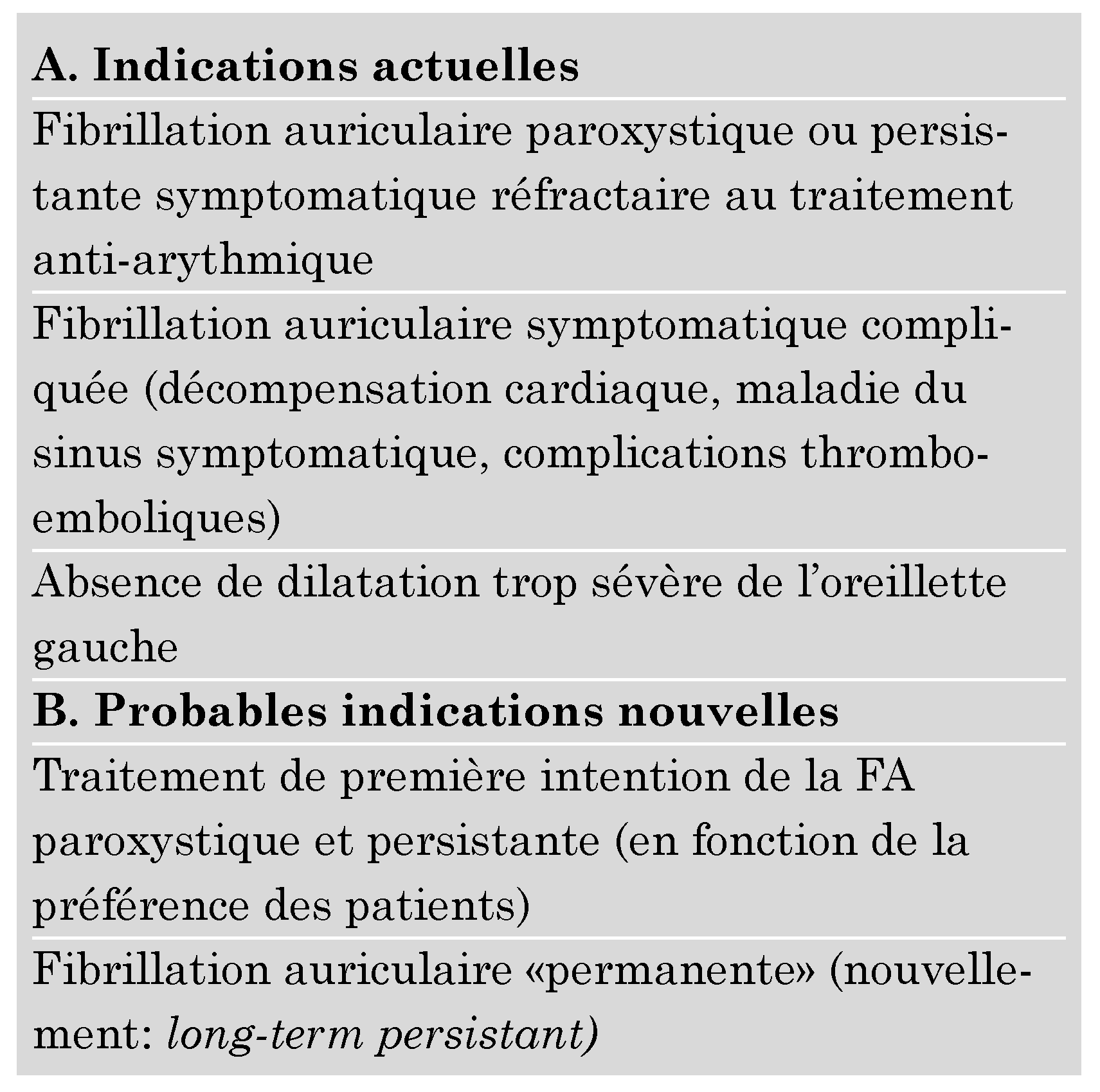
10]. L’ablation de la FA est avant tout réservée à des patients présentant des symptômes important réfractaires aux traitement anti-arythmique (
Table 2) [
11,
12]. Mais avec les succès de l’intervention, les indications sont en train de s’élargir, notamment chez certains patients qui désirent éviter un traitement anti-arythmique au long cours, ou chez des patients avec une insuffisance cardiaque associée à la FA [
13,
14]. Il est important de référer les patients à un électrophysiologue pratiquant ces interventions, de façon à ce qu’ils reçoivent une information optimale sur les taux de succès et les risques de l’intervention, ainsi que les alternatives. En général, il existe lors de l’intervention un risque d’accident vasculaire cérébral d’environ 1%, un risque de tamponnade de 1–2%, alors que les sténoses des veines pulmonaires sont devenues très rares, depuis que l’on évite de pratiquer des lésions dans les veines pulmonaires, préférant les régions ostiales et péri-ostiales. Par contre, lorsque des lésions linéaires sont pratiquées dans l’oreillette gauche, notamment dans le traitement d’une FA persistante, il existe un risque ultérieur de flutter auriculaire gauche, qui peut s’avérer plus gênant et plus dangereux que la FA (risque de cardiomyopathie rythmique en cas de flutter rapide persistant quelques semaines), et qui doit en général être traité par une nouvelle intervention. Ces 5 dernières années, le nombre de patients traités par thermo-ablation de leur FAa été en très forte hausse (
Figure 2), et ce n’est très probablement que le début d’une révolution dans la prise en charge des patients. L’essor du traitement de la FA sera cependant freiné par le manque de ressources humaines et matérielles, qui se développent à un rythme plus lent (
Figure 2). Quelques analyses préliminaires montrent que la thermo-ablation de la FApermet une réduction des coûts de prise en charge des patients, qui pourrait s’avérer importante dans des analyses à plus long-terme. Il est probable que la thermo-ablation de la FAdiminue le risque thrombo-embolique et améliore le pronostic des patients à long terme, mais les études de suivi à long-terme manquent encore. De nouvelles technologies, combinant imagerie et navigation à distance sont très intéressantes, et il est possible que la robotisation prenne une place grandissante dans l’ablation de la FA [
15]. L’efficacité et la sécurité de ces techniques restent cependant à démontrer de façon objective et dans des collectifs significatifs de patients. L’efficacité, de même que le rapport coût – bénéfice, devra être comparée aux méthodes classiques.
La première étape du traitement des symptômes est de ralentir la conduction du nœud atrio-ventriculaire. Ce traitement rend asymptomatique une grande proportion des patients, et les soustrait aux stratégies de maintien en rythme sinusal. L’étude AFFIRM a montré que cette approche était adéquate, du moins chez les patients relativement âgés. Pour freiner le nœud AV, l’usage des béta-bloquants devrait continuer de se généraliser, et restera certainement le traitement de choix de la FA chez le grand collectifs de patients qui ne présentent pas de symptômes importants. Les anti-calciques non dihydropyridines et la digoxine resteront certainement de médicaments d’appoint lorsque le freinage par les béta-bloquant n’est pas suffisant, ou en cas d’intolérance ou de contre-indication aux béta-bloquants. Il est probable que l’ablation de la jonction atrioventriculaire avec l’implantation d’un pacemaker unicaméral ou un pacemaker de resynchronisation reste une alternative pour une minorité de patients chez qui le traitement médicamenteux est inefficace ou mal toléré.
Va t’on vraiment trouver une alternative aux anti-vitamines K, dont la fin de règne est annoncée depuis plusieurs années [
16]? L’anticoagulation par anti-vitamine K est à ce jour le seul traitement efficace et sûr chez les patients présentant des risques thrombo-emboliques [
17]. L étude ACTIVE W a montré que le clopidogrel associé à l’aspirine n’était pas une alternative valable à l’anticoagulation [
18]. La FDA a récemment refusé l’enregistrement du ximélagatran, un inhibiteur direct de la thrombine, principalement en raison des risques d’effets secondaires importants. Le ximélagatran provoque une augmentation des transaminases chez 4–6% des patients et cause de façon très rare une hépatite fulminante. Les études SPORTIF III et SPORTIF V avaient montré que ce médicament avait un effet préventif des complications thrombo-emboliques systémiques pratiquement similaire à celui des anti-vitamine K, alors que les taux annuels de saignements sévères tendaient à être légèrement inférieur avec le ximélagatran (1,9% versus 2,5%, risque relatif 0,76, intervalle de confiance de 95%: 0,56–1,03, p <0,07) [
19,
20]. Un autre inhibiteur direct de la thrombine, le dabigatran, va être évalué dans l’étude RELY (Randomization Evaluation of the Long-Term Anticoagulant Therapy), où il sera comparé aux anti-vitamines K chez 15000 patients. Des inhibiteurs du facteur Xa, le rivaroxaban et l’apixaban vont être évalués chacun chez près de 15000 patients. Tous ces agents sont comparés aux anti-vitamines K dans de très grandes études, qui ont pour but de démontrer leur non-infériorité par rapport aux anti-vitamine K. Un certain scepticisme quant au réel développement de ces agents est inévitable, en partie à cause des précédents avec le ximélagatran, et également en relation avec le design des études, qui ont pour
endpoint la non-infériorité d’un nouveau médicament. En effet, si chaque nouveau traitement accepté parce qu’il n’est pas inférieur au traitement classique est ensuite utilisé comme élément de référence pour le développement d’un nouveau produit, l’on ne peut pas exclure que l’on glisse lentement vers l’acceptation de traitement réellement inférieur.
Comment les recommandations vont-elles évoluer? Certains spécialistes estiment que le risque annuel de complication thrombo-embolique accepté comme seuil pour la nécessité d’introduire une anti-coagulation – actuellement de 3–4%, est trop haut [
11]. A l’heure actuel, une patiente hypertendue de 65 ans ne doit pas forcément être anti-coagulée, selon les recommandations internationales, alors que beaucoup de spécialistes sont soucieux de laisser la patiente sans anticoagulation dans cette situation. Il est possible que ce seuil évolue vers le bas, au niveau d’un risque annuel d’embolie systémique de 2–3%, car il semble bien que le risque d’hémorragie cérébrale a diminué depuis les données des études qui datent de près de 15 ans, et toujours citées. Cette diminution du risque d’hémorragie cérébrale est probablement en relation avec l’utilisation de l’INR, et en relation avec le niveau cible entre 2–3, qui représente une anti-coagulation modérée. L’arrivée sur le marché d’une alternative efficace aux anti-vitamines K contribuerait certainement à faire baisser le seuil mentionné ci-dessus. La population des patients coronariens doit être à l’avenir mieux étudiée. D’une part, ces patients ont un facteur de risque thrombo-embolique surajouté. D’autre part, de nouvelles études sont souhaitables pour résoudre le problème épineux de la triple anticoagulation des patients traités par stent actif. En attendant le résultat d’études complémentaires, la meilleure option est de n’implanter que des stents nus chez les patients nécessitant une anticoagulation au long cours pour une FA, et de suspendre le traitement anticoagulant pendant le cours traitement de clopidogrel. En effet, une re-sténose est moins grave qu’une thrombose de stent, une hémorragie, ou une embolie systémique, autres complications possibles chez ces patients si d’autres options sont choisies.
Resynchronisation cardiaque: efficacité confirmée
Malgré les remarquables progrès du traitement médical, l’insuffisance cardiaque réfractaire touche des patients de plus en plus nombreux. La resynchronisation cardiaque par pacing biventriculaire peut corriger les désordres électromécaniques induits par des troubles de conduction intra-ventriculaire, qui existent chez un quart à un tiers de ces patients. Depuis 10 ans, la resynchronisation cardiaque a connu un développement considérable tant sur le plan technologique qu’au niveau de sa validation scientifique [
21,
22,
23]. Les résultats spectaculaires de l’étude CARE-HF sont venus s’ajouter aux données de différentes études comprenant COMPANION, MUSTIC, MIRACLE, CONTAK-CD. Non seulement ce traitement améliore la qualité de vie et la capacité à l’effort, mais il diminue les hospitalisations pour insuffisance cardiaque, et surtout il diminue la mortalité globale de façon importante [
22]. Dans CARE-HF, la diminution absolue de la mortalité globale atteignait 13,4%, soit une diminution relative de la mortalité globale considérable de 40% (intervalle de confiance de 95%: 23–53%) 36 mois après l’implantation d’un pacemaker de resynchronisation [
24]. La
Table 3 décrit les indications actuelles à la resynchronisation, de même que quelques nouveaux collectifs de patients qui font l’objet d’études [
25].
En effet, l’évaluation de ce nouveau traitement se poursuit. Les futures études devront en particulier répondre aux questions suivantes: Comment peut on reconnaître les non-répondeurs, qui constituent encore environ un quart des patients, ou comment améliorer la sélection des patients? Comment peut-on optimiser la programmation du pacemaker de resynchronisation, ne faut-il pas systématiquement évaluer la fonction du pacemaker à l’effort? La resynchronisation ne doit pas être elle envisagée avant que les symptômes aient développé des symptômes sévères? Son efficacité est-elle la même chez les patients avec bloc de branche droit? et en cas de fibrillation auriculaire permanente?
L’industrie investit beaucoup pour élargir les indications du traitement, et il faudra rester objectif quant à l’interprétation des résultats des études incluant de nouveaux groupes de patients. Au vu des effets très bénéfiques du traitement, il est cependant légitime de spéculer que ce traitement devrait être introduit plus tôt, avant que les patients n’aient développé des symptômes sévères. C’est à cette question que répondront les études MADITCRT (The Multicentric Automatic Defibrillator Implantation Trial-Cardiac Resynchronization Therapy) et REVERSE (Resynchronizationn Reverses Remodeling in Systolic Left Ventricular Dysfunction). Ces deux études évaluent le rôle de la resynchronisation chez des insuffisants cardiaques avec une classe fonctionnelle NYHAI et II. Par ailleurs, l’étude RETHINK (Resynchronization Therapy in Normal QRS) inclut des patients avec un QRS fin avec des signes échocardiographiques d’asynchronisme. Pour l’instant, il est frappant de constater que pour diverses raisons, beaucoup des candidats à la resynchronisation n’ont pas accès à ce traitement, alors qu’il a une action combinée sur les symptômes et le pronostic.
Les coûts initiaux de ce traitement sont certes importants, et il n’est pas certain que la diminution des hospitalisation dans les premières années qui suivent l’implantation permettent une économie en terme de coût par patient. En effet, il s’agit d’un traitement palliatif et la réapparition d’une insuffisance cardiaque après un laps de temps plus ou moins important est presque inéluctable. Par ailleurs, comme les patients traités vivent plus longtemps, ils sont exposés plus longtemps à d’autres maladies, qui génèrent également des coûts. Cependant, les effets bénéfiques de ce traitement devraient être comparés à ceux d’autres traitements, qui ont moins de répercussions favorables sur le bien être des patients. Il est possible que ce type d’analyse se développe ces prochaines années.