Abklärung der Koronaren Herzkrankheit Mittels Herz-MR Oder Mehrzeilen-CT
Abstract
Zusammenfassung
Generelle Überlegungen zur Datenlage
Worauf basiert ein optimales Patienten-Management bei Verdacht auf koronare Herzkrankheit?
Was wir heute mit Herz-MR erreichen können
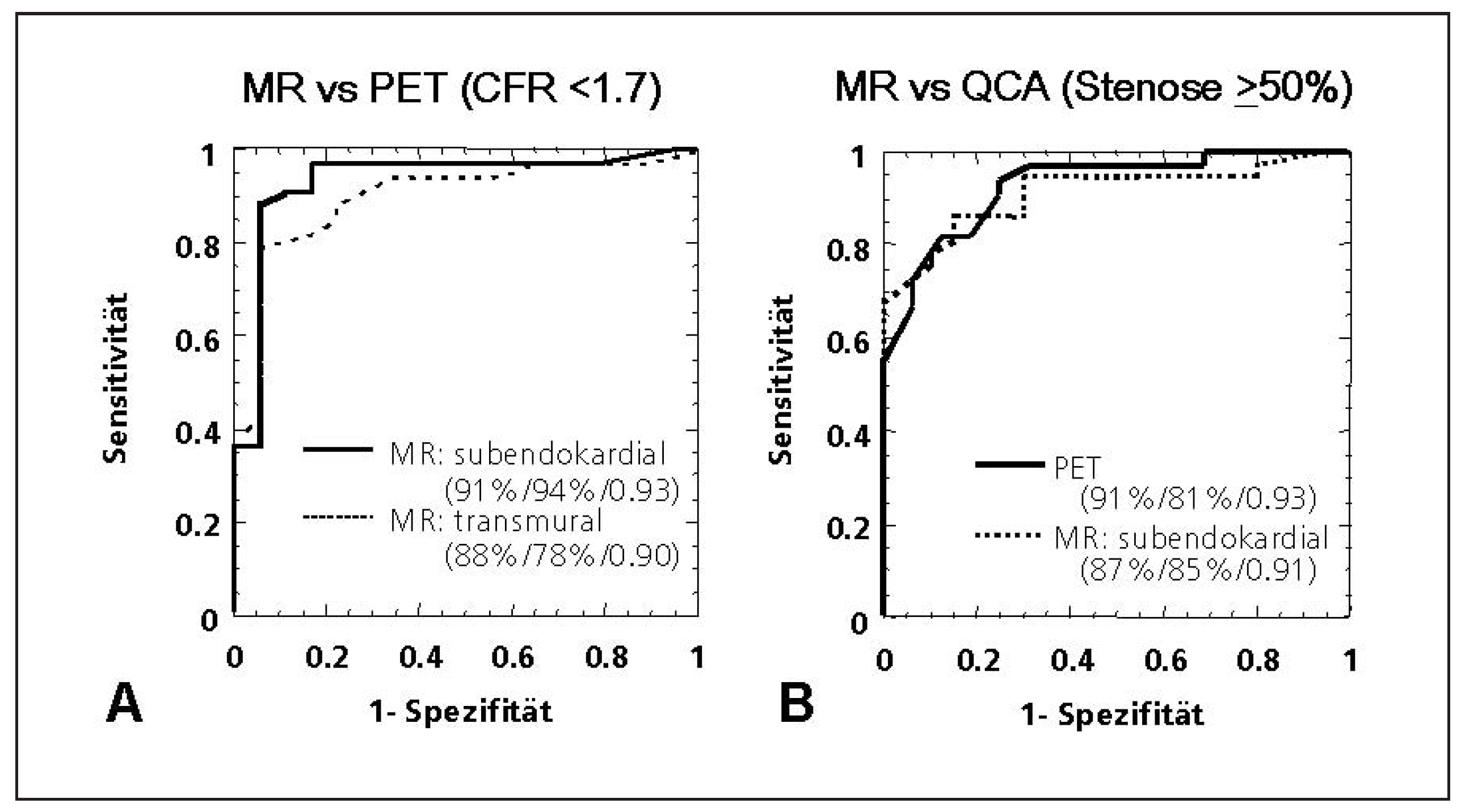
Multizenter-MR-Perfusionsstudien: Vergleich mit der quantitativen Koronarangiographie
Multizenter-MR-Perfusionsstudien: Vergleich mit der SPECT in «MR-IMPACT»
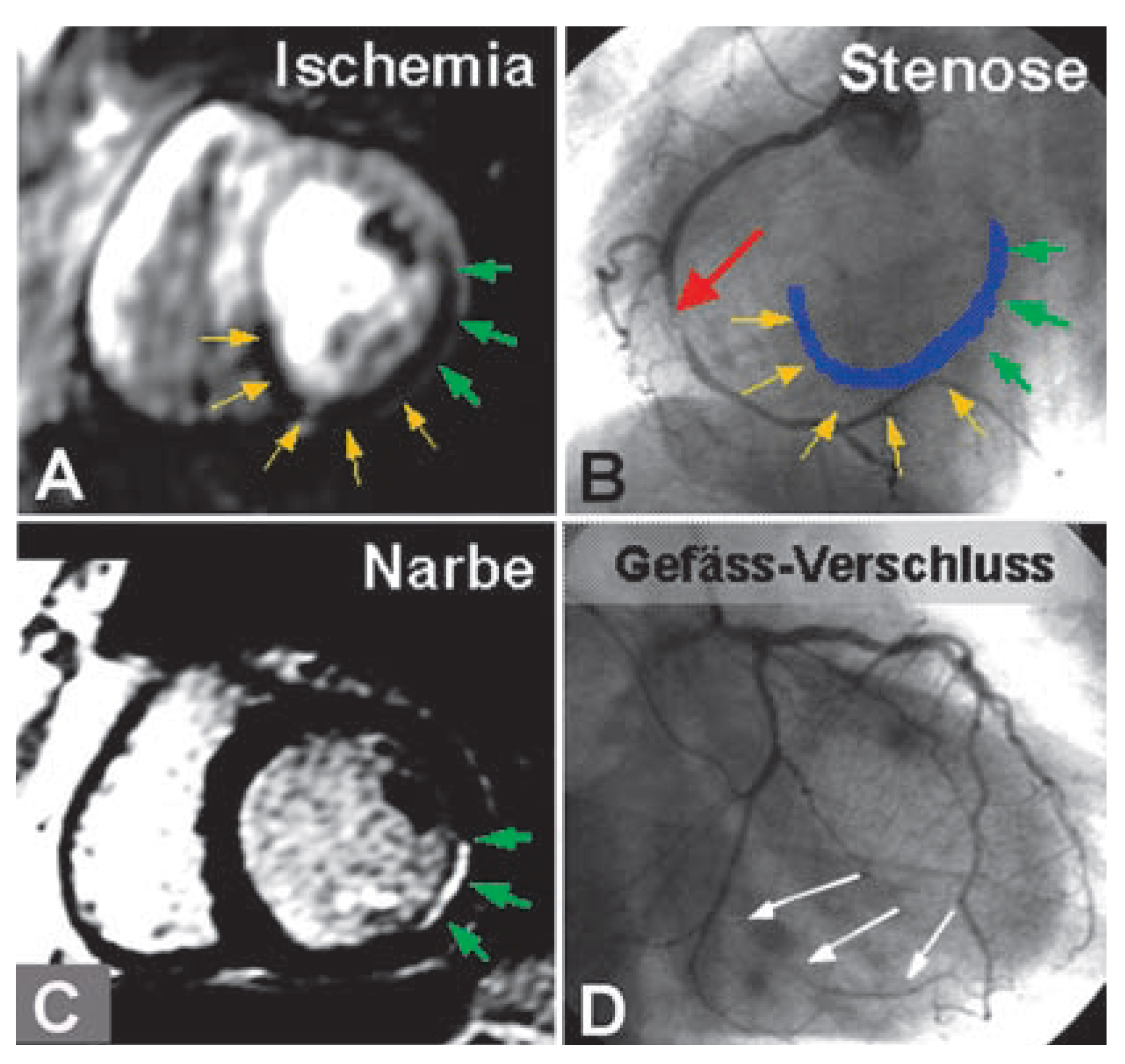
Beurteilung von Ischämie und Vitalität mittels Herz-MR
Vorteile und Nachteile der Herz-MR-MR-Untersuchung
MR-Koronarangiographie
Was wir heute mit dem Mehrzeilen-CT erreichen können
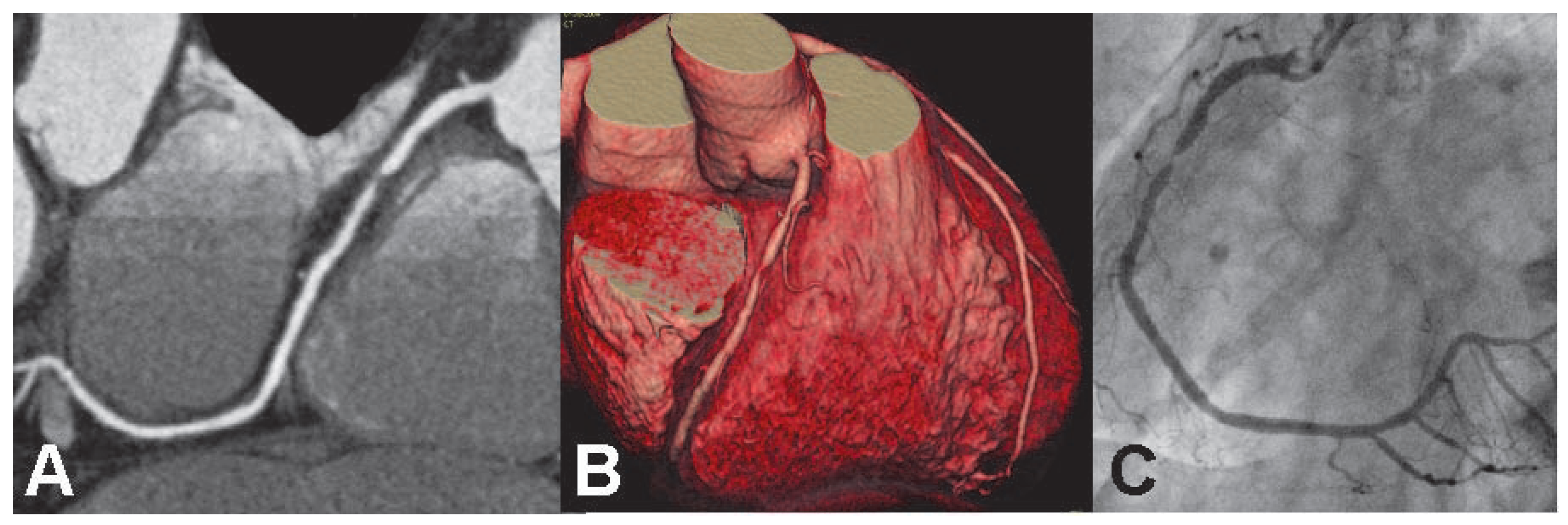
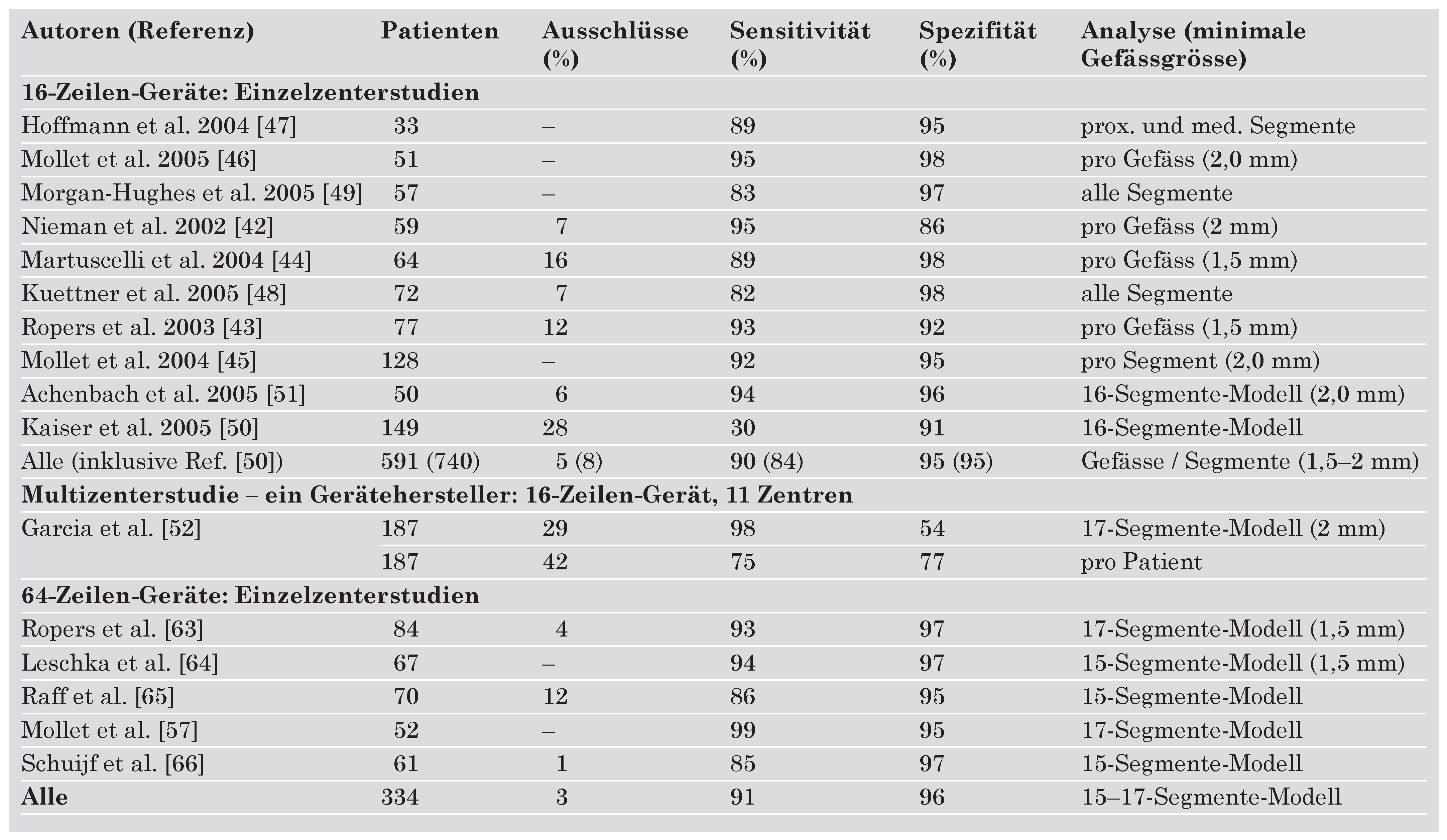
Mehrzeilen-CT-Koronarangiographie: Einzelzenterstudien
Mehrzeilen-CT-Koronarangiographie: Multizenterstudie
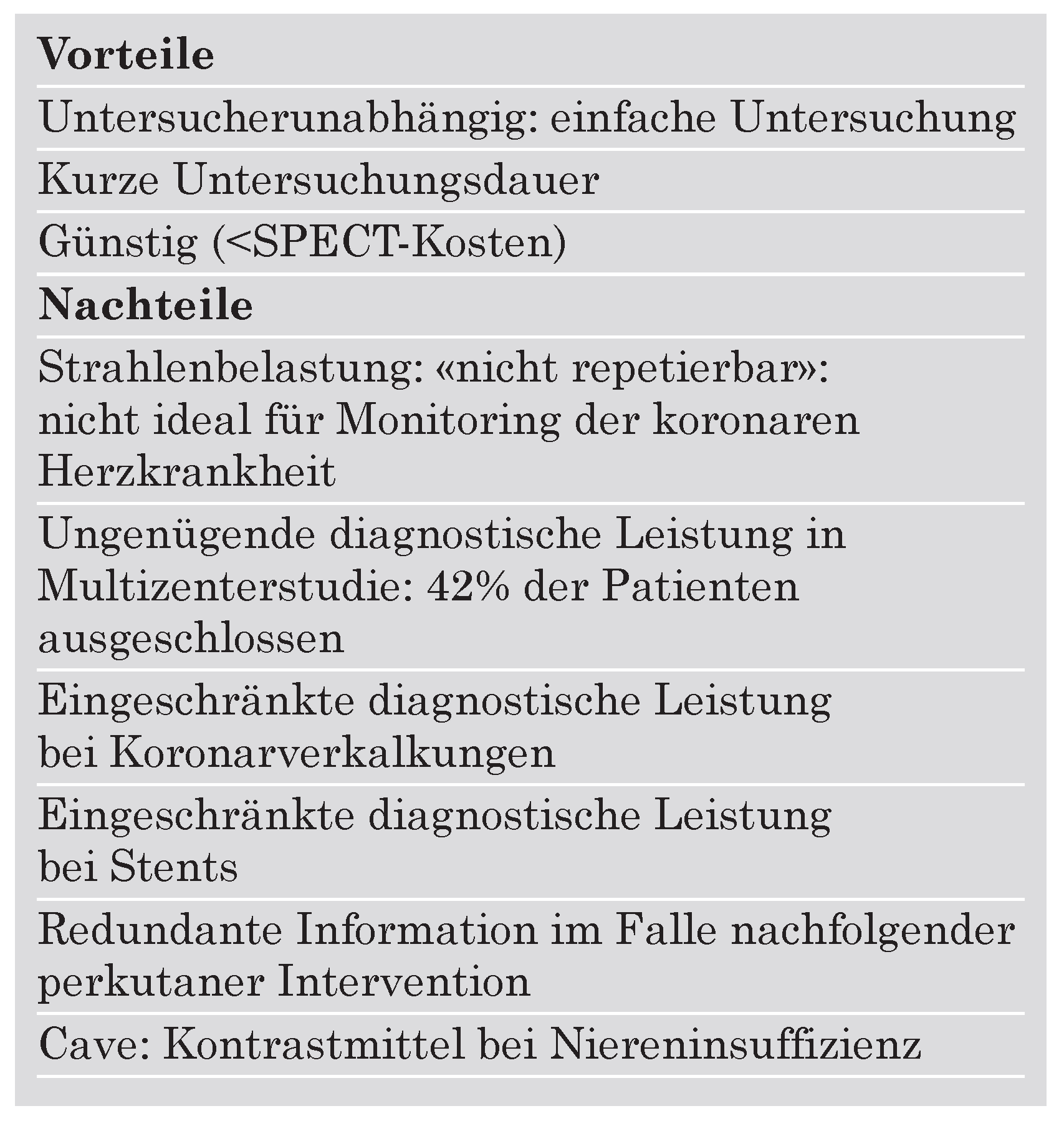
Vorteile und Nachteile der MZCT-MR-Untersuchung
Wie werden wir in Zukunft die koronare Herzkrankheit abklären: die re-aktive oder aktive Strategie?
Conflicts of Interest
References
- Yusuf, S.; Hawken, S.; Ounpuu, S.; Dans, T.; Avezum, A.; Lanas, F.; et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): Case-control study [see comment]. Lancet. 2004, 364, 937–952. [Google Scholar] [CrossRef] [PubMed]
- Prevention of coronary heart disease in clinical practice Recommendations of the second joint task force of European other societies on coronary prevention. Eur Heart J. 1998, 19, 1434–1503. [CrossRef]
- Smith SCJr Dove, J.T.; Jacobs, A.K.; Kennedy, J.W.; Kereiakes, D.; Kern, M.J.; et al. ACC/AHA guidelines for percutaneous coronary intervention (revision of the 1993 PTCA guidelines)executive summary: A report of the American College of Cardiology/American Heart Association task force on practice guidelines (Committee to revise the 1993 guidelines for percutaneous transluminal coronary angioplasty) endorsed by the Society for Cardiac Angiography and Interventions. Circulation. 2001, 103, 3019–3041. [Google Scholar]
- Davies, M.J. A macro and micro view of coronary vascular insult in ischemic heart disease. Circulation. 1990, 82, Ii38–46. [Google Scholar]
- Bruschke, A.V.; Kramer JRJr Bal, E.T.; Haque, I.U.; Detrano, R.C.; Goormastic, M. The dynamics of progression of coronary atherosclerosis studied in 168 medically treated patients who underwent coronary arteriography three times. Am Heart J. 1989, 117, 296–305. [Google Scholar] [CrossRef]
- Burke, A.P.; Kolodgie, F.D.; Farb, A.; Weber, D.K.; Malcom, G.T.; Smialek, J.; et al. Healed plaque ruptures and sudden coronary death: Evidence that subclinical rupture has a role in plaque progression. Circulation. 2001, 103, 934–940. [Google Scholar] [CrossRef]
- Ellis, S.; Alderman, E.L.; Cain, K.; Wright, A.; Bourassa, M.; Fisher, L. Morphology of left anterior descending coronary territory lesions as a predictor of anterior myocardial infarction: A CASS Registry Study. J Am Coll Cardiol. 1989, 13, 1481–1491. [Google Scholar] [CrossRef]
- Ojio, S.; Takatsu, H.; Tanaka, T.; Ueno, K.; Yokoya, K.; Matsubara, T.; et al. Considerable time from the onset of plaque rupture and/or thrombi until the onset of acute myocardial infarction in humans: Coronary angiographic findings within 1 week before the onset of infarction. Circulation. 2000, 102, 2063–2069. [Google Scholar] [CrossRef]
- Waters, D.; Lesperance, J.; Francetich, M.; Causey, D.; Theroux, P.; Chiang, Y.K.; et al. A controlled clinical trial to assess the effect of a calcium channel blocker on the progression of coronary atherosclerosis. Circulation. 1990, 82, 1940–1953. [Google Scholar] [CrossRef] [PubMed]
- Yokoya, K.; Takatsu, H.; Suzuki, T.; Hosokawa, H.; Ojio, S.; Matsubara, T.; et al. Process of progression of coronary artery lesions from mild or moderate stenosis to moderate or severe stenosis: A study based on four serial coronary arteriograms per year. Circulation. 1999, 100, 903–909. [Google Scholar] [CrossRef] [PubMed]
- Taeymans, Y.; Theroux, P.; Lesperance, J.; Waters, D. Quantitative angiographic morphology of the coronary artery lesions at risk of thrombotic occlusion. Circulation. 1992, 85, 78–85. [Google Scholar] [CrossRef]
- Schwitter, J. Future strategies in the management of coronary artery disease. Future Cardiology. 2006, 2, 555–566. [Google Scholar] [CrossRef]
- Kemp, H.; Kronmal, R.; Vlietstra, R.; Frye, R. Seven year survival of patients with normal or near normal coronary arteriograms: A CASS registry study. J Amer Coll Cardiol. 1986, 7, 479–483. [Google Scholar] [CrossRef]
- Ambrose, J.A.; Tannenbaum, M.A.; Alexopoulos, D.; Hjemdahl Monsen, C.E.; Leavy, J.; Weiss, M.; et al. Angiographic progression of coronary artery disease and the development of myocardial infarction. J Am Coll Cardiol. 1988, 12, 56–62. [Google Scholar] [CrossRef]
- Little, W.C.; Constantinescu, M.; Applegate, R.J.; Kutcher, M.A.; Burrows, M.T.; Kahl, F.R.; et al. Can coronary angiography predict the site of a subsequent myocardial infarction in patients with mild-to-moderate coronary artery disease? Circulation. 1988, 78, 1157–1166. [Google Scholar] [CrossRef] [PubMed]
- Nobuyoshi, M.; Tanaka, M.; Nosaka, H.; Kimura, T.; Yokoi, H.; Hamasaki, N.; et al. Progression of coronary atherosclerosis: Is coronary spasm related to progression? J Amer Coll Cardiol. 1991, 18, 904–910. [Google Scholar] [CrossRef] [PubMed]
- Giroud, D.; Li, J.; Urban, P.; Meier, B.; Rutishauser, W. Relation of the site of acute myocardial infarction to the most severe coronary arterial stenosis at prior angiography. Am. J. Cardiol. 1992, 69, 729–732. [Google Scholar] [CrossRef] [PubMed]
- Naghavi, M.; Libby, P.; Falk, E.; Casscells, S.W.; Litovsky, S.; Rumberger, J.; et al. From vulnerable plaque to vulnerable patient: A call for new definitions and risk assessment strategies: Part II. Circulation. 2003, 108, 1772–1778. [Google Scholar] [CrossRef]
- Iskander, S.; Iskandrian, A.E. Risk assessment using singlephoton emission computed tomographic technetium-99m sestamibi imaging. J Am Coll Cardiol. 1998, 32, 57–62. [Google Scholar] [CrossRef]
- Schwitter, J.; Nanz, D.; Kneifel, S.; Bertschinger, K.; Buchi, M.; Knusel, P.R.; et al. Assessment of myocardial perfusion in coronary artery disease by magnetic resonance: A comparison with positron emission tomography and coronary angiography. Circulation. 2001, 103, 2230–2235. [Google Scholar] [CrossRef]
- Al-Saadi, N.; Nagel, E.; Gross, M.; Bornstedt, A.; Schnackenburg, B.; Klein, C.; et al. Noninvasive detection of myocardial ischemia from perfusion reserve based on cardiovascular magnetic resonance. Circulation. 2000, 101, 1379–1383. [Google Scholar] [CrossRef]
- Cullen, J.H.; Horsfield, M.A.; Reek, C.R.; Cherryman, G.R.; Barnett, D.B.; Samani, N.J. A myocardial perfusion reserve index in humans using first-pass contrast-enhanced magnetic resonance imaging. J Am Coll Cardiol. 1999, 33, 1386–1394. [Google Scholar] [CrossRef] [PubMed]
- Schwitter, J.; DeMarco, T.; Kneifel, S.; von Schulthess, G.K.; Jorg, M.C.; Arheden, H.; et al. Magnetic resonance-based assessment of global coronary flow and flow reserve and its relation to left ventricular functional parameters: A comparison with positron emission tomography. Circulation. 2000, 101, 2696–2702. [Google Scholar] [CrossRef] [PubMed]
- Giang, T.; Nanz, D.; Coulden, R.; Friedrich, M.; Graves, M.; Al-Saadi, N.; et al. Detection of coronary artery disease by Magnetic Resonance myocardial perfusion imaging with various contrast medium doses: First European multicenter experienc. Eur Hear J. 2004, 25, 1657–1665. [Google Scholar] [CrossRef]
- Wolff, S.; Schwitter, J.; Coulden, R.; Friedrich, M.; Bluemke, D.; Biedermann, R.; et al. Myocardial first-pass perfusion magnetic resonance imaging: A multicentre dose-ranging study. Circulation. 2004, 110, 732–737. [Google Scholar] [CrossRef]
- Schwitter, J.; Bauer, W.; van Rossum, A.; Lombardi, M.; Al-Saadi, N.; Ahlstrom, H.; et al. MR-IMPACT: Comparison of myocardial perfusion imaging with single photon emission computed tomography in known or suspected coronary artery disease: A multicentre, multivendor dose finding study. Abstract: Clinical trial update. Eur Heart J. 2005, 26, 329. [Google Scholar]
- Hendel, R.C.; Berman, D.S.; Cullom, S.J.; Follansbee, W.; Heller, G.V.; Kiat, H.; et al. Multicentre clinical trial to evaluate the efficacy of correction for photon attenuation and scatter in SPECT myocardial perfusion imaging. Circulation. 1999, 99, 2742–2749. [Google Scholar] [CrossRef] [PubMed]
- Taillefer, R.; DeDuey, E.G.; Udelson, J.E.; Beller, G.A.; Latour, Y.; Reeves, F. Comparative diagnostic accuracy of Tl-201 and Tc-99m sestamibi SPECT imaging (perfusion and ECGgated SPECT) in detecting coronary artery disease in women. J Am Coll Cardiol. 1997, 29, 69–77. [Google Scholar] [CrossRef] [PubMed]
- Wackers, F.J.T.; Bodenheimer, M.; Fleiss, J.L.; Brown, M.; Multicenter Study on Silent Myocardial Ischemia Investigators. Factors affecting uniformity in interpretation of planar thallium-201 imaging in a multicenter trial. J Am Coll Cardiol. 1993, 21, 1064–1074. [Google Scholar] [CrossRef]
- Pasquet, A.; Robert, A.; D’Hondt, A.M.; Dion, R.; Melin, J.A.; Vanoverschelde, J.L. Prognostic value of myocardial ischemia and viability in patients with chronic left ventricular ischemic dysfunction. Circulation. 1999, 100, 141–148. [Google Scholar] [CrossRef]
- Schwitter, J.; Saeed, M.; Wendland, M.F.; Derugin, N.; Canet, E.; Brasch, R.C.; et al. Influence of the severity of myocardial injury on the distribution of macromolecules: Extraversus intravascular gadolinium-based MR contrast media. J Am Coll Cardiol. 1997, 30, 1086–1094. [Google Scholar] [CrossRef]
- Kim, R.J.; Wu, E.; Rafael, A.; Chen, E.L.; Parker, M.A.; Simonetti, O.; et al. The use of contrast-enhanced magnetic resonance imaging to identify reversible myocardial dysfunction. N Engl J Med. 2000, 343, 1445–1453. [Google Scholar] [CrossRef] [PubMed]
- Knuesel, P.R.; Nanz, D.; Wyss, C.; Buechi, M.; Kaufmann, P.A.; von Schulthess, G.K.; et al. Characterization of dysfunctional myocardium by positron emission tomography and magnetic resonance: Relation to functional outcome after revascularization. Circulation. 2003, 108, 1095–1100. [Google Scholar] [CrossRef]
- Choi, K.M.; Kim, R.J.; Gubernikoff, G.; Vargas, J.D.; Parker, M.; Judd, R.M. Transmural extent of acute myocardial infarction predicts long-term improvement in contractile function. Circulation. 2001, 104, 1101–1107. [Google Scholar] [CrossRef]
- Wu, E.; Judd, R.M.; Vargas, J.D.; Klocke, F.J.; Bonow, R.O.; Kim, R.J. Visualisation of presence, location, and transmural extent of healed Q-wave and non-Q-wave myocardial infarction. Lancet. 2001, 357, 21–28. [Google Scholar] [CrossRef]
- Schwitter, J.; Bauer, W.; van Rossum, A.C.; Lombardi, M.; AlSaadi, N.; Schwaiger, M.; et al. MR perfusion imaging for detection coronary artery disease: A multicenter dose finding study in comparison with X-ray coronary angiography and single photon emission computed tomography. Circulation. 2004, 110, III–643. [Google Scholar]
- Post, J.; van Rossum, A.; Bronzwaer, J.; de Cock, C.; Hofman, M.; Valk, J.; et al. Magnetic Resonance angiography of anomalous coronary arteries: A new gold standard for delineating the proximal course? Circulation. 1995, 92, 3163–3171. [Google Scholar] [CrossRef] [PubMed]
- Manning, W.J.; Li, W.; Edelman, R.R. A preliminary report comparing magnetic resonance coronary angiography with conventional angiography. [see comment]. N Engl J Med. [Erratum appears in N Engl J Med. 1993, 330, 152.]. 1993, 328, 828–832. [Google Scholar] [CrossRef] [PubMed]
- Müller, M.; Fleisch, M.; Kroeker, R.; Chatterjee, T.; Meier, B.; Vock, P. Proximal coronary stenosis: Three-dimensional MRI with fat saturation and navigator echo. J Magn Reson Imaging. 1997, 7, 644–651. [Google Scholar] [CrossRef]
- Sandstede, J.; Pabst, T.; Beer, M.; Geis, N.; Kenn, W.; Neubauer, S.; et al. Three-dimensional MR coronary angiography using the navigator technique compared with conventional coronary angiography. Am J Roentgenology. 1999, 172, 135–139. [Google Scholar] [CrossRef]
- Kim, W.Y.; Danias, P.G.; Stuber, M.; Flamm, S.D.; Plein, S.; Nagel, E.; et al. Coronary magnetic resonance angiography for the detection of coronary stenoses [see comment]. N Engl J Med. 2001, 345, 1863–1869. [Google Scholar] [CrossRef] [PubMed]
- Nieman, K.; Cademartiri, F.; Lemos, P.A.; Raaijmakers, R.; Pattynama, P.M.; de Feyter, P.J. Reliable noninvasive coronary angiography with fast submillimeter multislice spiral computed tomography. [see comment]. Circulation. 2002, 106, 2051–2054. [Google Scholar] [CrossRef]
- Ropers, D.; Baum, U.; Pohle, K.; Anders, K.; Ulzheimer, S.; Ohnesorge, B.; et al. Detection of coronary artery stenoses with thin-slice multi-detector row spiral computed tomography and multiplanar reconstruction. Circulation. 2003, 107, 664–666. [Google Scholar] [CrossRef]
- Martuscelli, E.; Romagnoli, A.; D’Eliseo, A.; Razzini, C.; Tomassini, M.; Sperandio, M.; et al. Accuracy of thin-slice computed tomography in the detection of coronary stenoses. Eur Heart J. 2004, 25, 1043–1048. [Google Scholar] [CrossRef]
- Mollet, N.R.; Cademartiri, F.; Nieman, K.; Saia, F.; Lemos, P.A.; McFadden, E.P.; et al. Multislice spiral computed tomography coronary angiography in patients with stable angina pectoris. J Am Coll Cardiol. 2004, 43, 2265–2270. [Google Scholar] [CrossRef]
- Mollet, N.R.; Cademartiri, F.; Krestin, G.P.; McFadden, E.P.; Arampatzis, C.A.; Serruys, P.W.; et al. Improved diagnostic accuracy with 16-row multi-slice computed tomography coronary angiography. J Am Coll Cardiol. 2005, 45, 128–132. [Google Scholar] [CrossRef]
- Hoffmann, U.; Moselewski, F.; Cury, R.C.; Ferencik, M.; Jang, I.K.; Diaz, L.J.; et al. Predictive value of 16-slice multidetector spiral computed tomography to detect significant obstructive coronary artery disease in patients at high risk for coronary artery disease: Patient-versus segment-based analysis. Circulation. 2004, 110, 2638–2643. [Google Scholar] [CrossRef]
- Kuettner, A.; Beck, T.; Drosch, T.; Kettering, K.; Heuschmid, M.; Burgstahler, C.; et al. Diagnostic accuracy of noninvasive coronary imaging using 16-detector slice spiral computed tomography with 188 ms temporal resolution. J Am Coll Cardiol. 2005, 45, 123–127. [Google Scholar] [CrossRef] [PubMed][Green Version]
- Morgan-Hughes, G.J.; Roobottom, C.A.; Owens, P.E.; Marshall, A.J. Highly accurate coronary angiography with submillimetre, 16-slice computed tomography. Heart. 2005, 91, 308–313. [Google Scholar] [CrossRef] [PubMed]
- Kaiser, C.; Bremerich, J.; Haller, S.; Brunner-La Rocca, H.; Bongartz, G.; Pfisterer, M.; et al. Limited diagnostic yield of noninvasive coronary angiography by 16-slice multi-detector spiral computed tomography in routine patients referred for evaluation of coronary artery disease. Eur Heart J. 2005, 26, 1987–1992. [Google Scholar] [CrossRef]
- Achenbach, S.; Ropers, D.; Pohle, F.K.; Raaz, D.; von Erffa, J.; Yilmaz, A.; et al. Detection of coronary artery stenoses using multi-detector CT with 16x0.75 collimation and 375 ms rotation. Eur Heart J. 2005, 26, 1978–1986. [Google Scholar] [CrossRef]
- Garcia, M.J.; Lessick, J.; Hoffmann, M.H.; Investigators, C.S. Accuracy of 16-row multidetector computed tomography for the assessment of coronary artery stenosis. JAMA. 2006, 296, 403–411. [Google Scholar] [CrossRef]
- Haberl, R.; Becker, A.; Leber, A.; Knez, A.; Becker, C.; Lang, C.; et al. Correlation of coronary calcification and angiographically documented stenoses in patients with suspected coronary artery disease: Results of 1,764 patients. J Am Coll Cardiol. 2001, 37, 451–457. [Google Scholar] [CrossRef]
- Walsh, L.; Rühm, W.; Kellerer, A. Cancer risk estimates for gamma-rays with regard to organ-specific doses (Part 1: All solid cancers combined). Radiat Environ Biophys. 2004, 43, 145–151. [Google Scholar] [CrossRef]
- ICRP. (1991) Publication 60. The 1990 Recommendations of the International Commission on Radiological Protection, Ann. ICRP 21 (1–3). Intenational Commission on Radiological Protection; Pergamon Press: Oxford, 1990. [Google Scholar]
- Coles, D.R.; Smail, M.A.; Negus, I.S.; Wilde, P.; Oberhoff, M.; Karsch, K.R.; et al. Comparison of radiation doses from multislice computed tomography coronary angiography and conventional diagnostic angiography. [see comment]. J Am Coll Cardiol. 2006, 47, 1840–1845. [Google Scholar] [CrossRef] [PubMed]
- Mollet, N.R.; Cademartiri, F.; van Mieghem, C.A.; Runza, G.; McFadden, E.P.; Baks, T.; et al. High-resolution spiral computed tomography coronary angiography in patients referred for diagnostic conventional coronary angiography. [see comment]. Circulation. 2005, 112, 2318–2323. [Google Scholar] [CrossRef]
- Cardis, E.; Vrijheid, M.; Blettner, M.; Gilbert, E.; Hakama, M.; Hill, C.; et al. Risk of cancer after low doses of ionising radiation: Retrospective cohort study in 15 countries. BMJ. 2005, 331, 77–82. [Google Scholar] [CrossRef]
- Ammann, P.; Brunner-La Rocca, H.; Angehrn, W.; Roelli, H.; Sagmeister, M.; Rickli, H. Procedural complications following diagnostic coronary angiography are related to the operator’s experience and the catheter size. Cath Cardiovasc Intervent. 2003, 59, 13–18. [Google Scholar] [CrossRef] [PubMed]
- Heart disease and stroke statistics: Update 2005. American Heart Association 2005.
- Fraser, A.; Buser, P.; Bax, J.; Dassen, W.; Nihoyannopoulos, P.; Schwitter, J.; et al. The future of cardiovascular imaging and non-invasive diagnosis. Eur Heart J 2006, 27, 1750–1753. [Google Scholar] [CrossRef]
- Naghavi, M.; Libby, P.; Falk, E.; Casscells, S.W.; Litovsky, S.; Rumberger, J.; et al. From vulnerable plaque to vulnerable patient: A call for new definitions and risk assessment strategies: Part I. Circulation. 2003, 108, 1664–1672. [Google Scholar] [CrossRef] [PubMed]
- Ropers, D.; Rixe, J.; Anders, K.; Kuttner, A.; Baum, U.; Bautz, W.; et al. Usefulness of multidetector row spiral computed tomography with 64? 0.6-mm collimation and 330-ms rotation for the noninvasive detection of significant coronary artery stenoses. Am J Cardiol. 2006, 97, 343–348. [Google Scholar] [CrossRef] [PubMed]
- Leschka, S.; Alkadhi, H.; Plass, A.; Desbiolles, L.; Grunenfelder, J.; Marincek, B.; et al. Accuracy of MSCT coronary angiography with 64-slice technology: First experience. [see comment]. Eur Heart J. 2005, 26, 1482–1487. [Google Scholar] [CrossRef]
- Raff, G.L.; Gallagher, M.J.; O’Neill, W.W.; Goldstein, J.A. Diagnostic accuracy of noninvasive coronary angiography using 64-slice spiral computed tomography. J Am Coll Cardiol. 2005, 46, 552–557. [Google Scholar] [CrossRef] [PubMed]
- Schuijf, J.D.; Pundziute, G.; Jukema, J.W.; Lamb, H.J.; van der Hoeven, B.L.; de Roos, A.; et al. Diagnostic accuracy of 64-slice multislice computed tomography in the noninvasive evaluation of significant coronary artery disease. Am J Cardiol. 2006, 98, 145–148. [Google Scholar] [CrossRef]
- Morin, R.; Gerber, T.; McCollough, C. Radiation dose in computed tomography of the heart. Circulation. 2003, 107, 917–922. [Google Scholar] [CrossRef]
- Committee to Assess Health Risks from Exposure to Low Levels of Ionizing Radiation NRCNAoS. Health risks from exposure to low levels of ionizing radiation: BEIR VII—Phase 2. Executive Summary. Available online: http://www.nap.edu/catalog/11340.html 20061–424.
 |
 |
 |
 |
 |
© 2007 by the author. Attribution—Non-Commercial—NoDerivatives 4.0.
Share and Cite
Schwitter, J. Abklärung der Koronaren Herzkrankheit Mittels Herz-MR Oder Mehrzeilen-CT. Cardiovasc. Med. 2007, 10, 126. https://doi.org/10.4414/cvm.2007.01241
Schwitter J. Abklärung der Koronaren Herzkrankheit Mittels Herz-MR Oder Mehrzeilen-CT. Cardiovascular Medicine. 2007; 10(4):126. https://doi.org/10.4414/cvm.2007.01241
Chicago/Turabian StyleSchwitter, Jürg. 2007. "Abklärung der Koronaren Herzkrankheit Mittels Herz-MR Oder Mehrzeilen-CT" Cardiovascular Medicine 10, no. 4: 126. https://doi.org/10.4414/cvm.2007.01241
APA StyleSchwitter, J. (2007). Abklärung der Koronaren Herzkrankheit Mittels Herz-MR Oder Mehrzeilen-CT. Cardiovascular Medicine, 10(4), 126. https://doi.org/10.4414/cvm.2007.01241




