Summary
On December 3rd, 1967, Christiaan Barnard transplanted for the first time a human heart. The patient died 18 days after the procedure due to a pneumonia that had been misinterpreted as a rejection with concomitant heart failure. Due to severe rejections many transplant programs were subsequently closed. After the discovery of cyclosporine, a substance that provided sustained immunosuppression, cardiac transplant programmes were restarted, in Switzerland at first in Zurich in 1985. After a remarkable growth up to 4438 heart transplants worldwide in 1994, the number of procedures declined thereafter, due to decreasing availability of organs and improved medical options. Today, biventricular pacers, left ventricular assist devices and stem cells play an increasing role. In Switzerland, heart transplants were first performed in Zurich, then in Lausanne and Geneva and much later in Bern and Basle. The increasing number of transplant programmes in Switzerland led decreasing procedures per centre and year. Whether this problem should be solved by an even distribution of organ transplantations in all five Swiss centres or by the creation of few comprehensive transplant centres in the country is in the theme of the ongoing political debate.
Zusammenfassung
Am 3. Dezember 1967 transplantierte Christiaan Barnard am Groote-Schuur-Krankenhaus in Kapstadt erstmals ein fremdes Herz. Der Patient verstarb 18 Tage nach der Transplantation an einer Pneumonie, die als Herzinsuffizienz im Rahmen einer Abstossung fehlinterpretiert wurde. Aufgrund unbeherrschbarer Abstossungsprobleme wurden viele Transplantationsprogramme sistiert. Erst durch die Entdeckung des Cyclosporins, welches das Immunsystem in Schach zu halten vermag, wurden Herztransplantationen (HTPL) wieder aufgenommen. Das Universitätsspital Zürich nahm als erstes Zentrum in der Schweiz 1985 HTPL wieder auf. Nach einer Zunahme der HTPLmit weltweit 4438 im Jahr 1994 kam es danach zu einem stetigen Rückgang, zum einen aufgrund abnehmender Spendewilligkeit und zum anderen wegen besseren medikamentösen Möglichkeiten. Heute spielen biventrikuläre Schrittmacher, «Left Ventricular Assist Devices» wie auch Stammzellen eine zunehmende Rolle. In der Schweiz wurden zunächst in Zürich, dann in Lausanne, Genf und deutlich später Bern und Basel HTPL durchgeführt. Die Zunahme der HTPL-Zentren hat zu einer Verdünnung der Erfahrung der erfahrendsten Zentren geführt. Ob die Lösung des Problems in einer gleichmässigen Verteilung aller Organtransplantationen auf 5 Universi tätszentren oder in der Schaffung weniger übergreifender Transplantationszentren in der deutschen und französischen Schweiz liegt, ist im Moment im Zentrum der politischen Debatte.
Die heroische Tat
Als Christiaan Barnard am 3. Dezember 1967 am Groote-Schuur-Krankenhaus in Kapstadt erstmals einem Patienten, dem Lebensmittelhändler Louis Washkansky, ein fremdes Herz in seinen Brustraum einsetzte, war dies eine medizinische Sensation, die Welt war begeistert und beeindruckt [
1,
2,
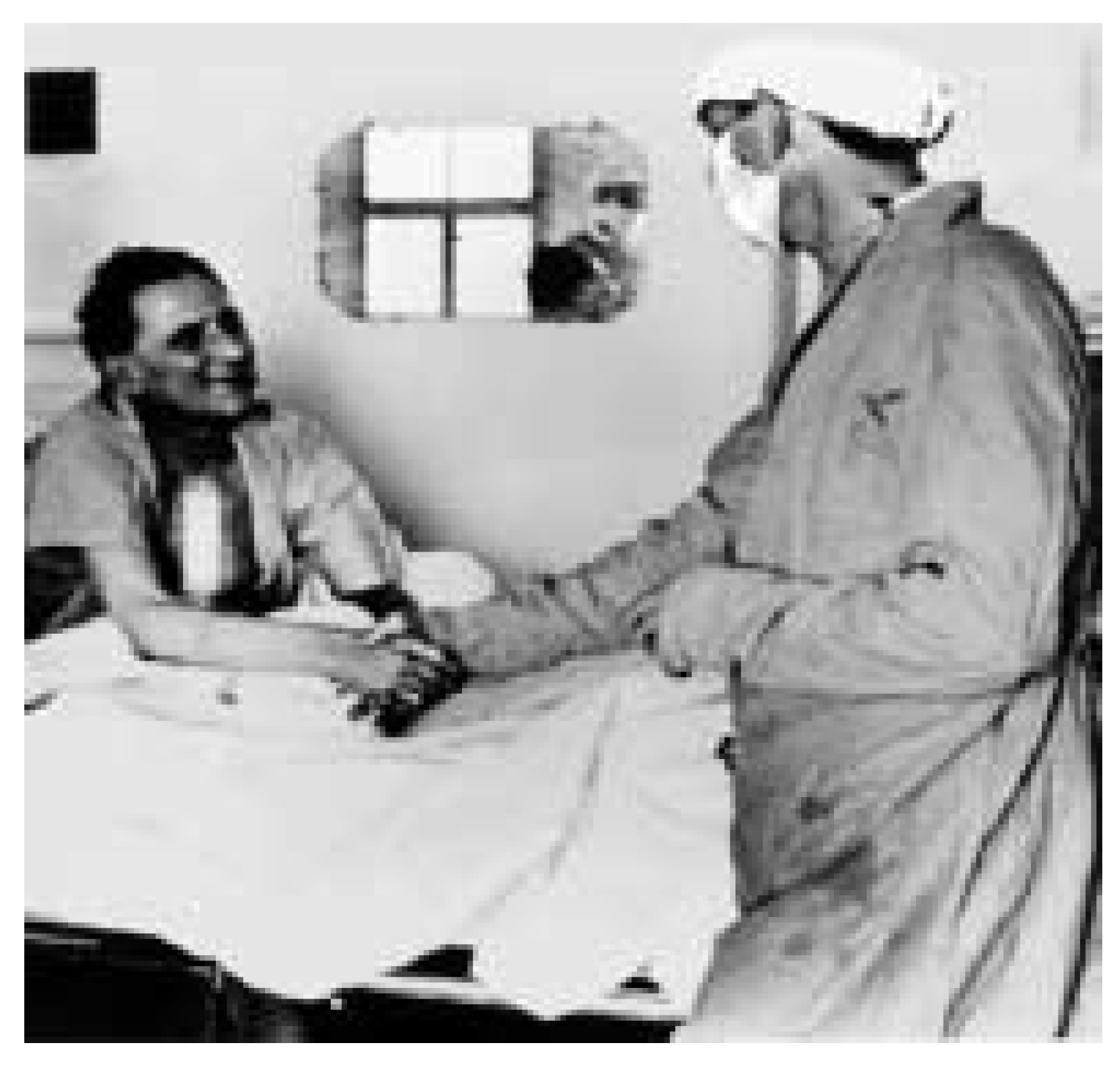
3]. Die Ungeheuerlichkeit, dass ein Mann mit dem Herzen einer Frau, Denise Derwall, 25jähriges Opfer eines Verkehrsunfalls, weiterlebte, war eine Sache; die historische Wende aber war, dass ein fremdes Herz in seinem Brustraum schlug und der Patient dennoch derselbe blieb. Auch dadurch wurde Neuland beschritten: Das Herz als Hort der Seele war Geschichte geworden, das Organ, nun eine ersetzbare Pumpe, hatte sich gegen das Symbol durchgesetzt (
Figure 1 und
Figure 2A).
Die Sache erwies sich bald als schwieriger denn erwartet. Es war weniger die chirurgische Tat, die alle bewunderten, die das eigentliche Problem darstellte; nein, die von Norman Shumway (
Figure 2B) experimentell entwickelte chirurgische Technik war einfacher als viele vergleichbare Herzoperationen [
4]. Bei Barnards erstem Patienten, dem 55jährigen Lebensmittelhändler Louis Washkansky, kam es in den ersten Wochen nach dem Eingriff zu Komplikationen. Der Patient starb schliesslich 18 Tage nach der Transplantation an einer Pneumonie, die als Herzinsuffizienz im Rahmen einer Abstossung fehlinterpretiert wurde [
5]. Norman Shumway, der eigentliche Pionier der Herztransplantation, nahm kurz nach Christiaan Barnard im Januar 1968 in Stanford die erste Herztransplantation in den USA vor. Obschon das eigentliche, die Transplantation, technisch machbar geworden war, erwiesen sich die Folgekrankheiten als schlecht beherrschbar. Das Fremde und Eigene erwies sich als das Zentrale. Viele Transplantationsprogramme wurden aufgrund der unbeherrschbaren Abstossungsprobleme sowie anderer Komplikationen sistiert, so auch in Zürich. Ake Senning (
Figure 2C) führte zwei Jahre später in Zürich eine der ersten Herztransplantationen in Europa durch und wiederholte diesen Eingriff zweimal, bevor auch in Zürich das mit grossen Erwartungen gestartete Herztransplantationsprogramm aufgrund der unbewältigten immunologischen Probleme 1971 zum Stillstand kam [
6,
7,
8].
Das Eigene und das Fremde
Erst die Fortschritte in der Immunologie, der Lehre vom Eigenen und Fremden im Körper, brachten den Durchbruch – oder vielmehr ein Zufall, ein Mitbringsel eines Mitarbeiters der Firma Hoffmann-La Roche aus seinen Ferien im hohen Norden, nach Basel: Cyclosporin, auch dies ein Produkt eines Pilzes, ein komplexes Molekül, das das Immunsystems in Schach zu halten vermochte und damit die Organtransplantation zur Routine machte [
9,
10,
11,
12]. Cyclosporin wurde von Sandoz im November 1983 in den USA eingeführt und bald darauf auch in Europa verfügbar. Die Erfolge bei der Nierentransplantation führten dazu, dass auch die Herztransplantationsprogramme zunehmend wieder reaktiviert wurden. 1985 wurde das Herztransplantationsprogramm am UniversitätsSpital Zürich als Erstes in der Schweiz durch Marko Turina wieder gestartet, danach folgten einige Jahre später Lausanne und Genf und schliesslich, 10 Jahre später, Bern und 1999 auch Basel (
Table 1).
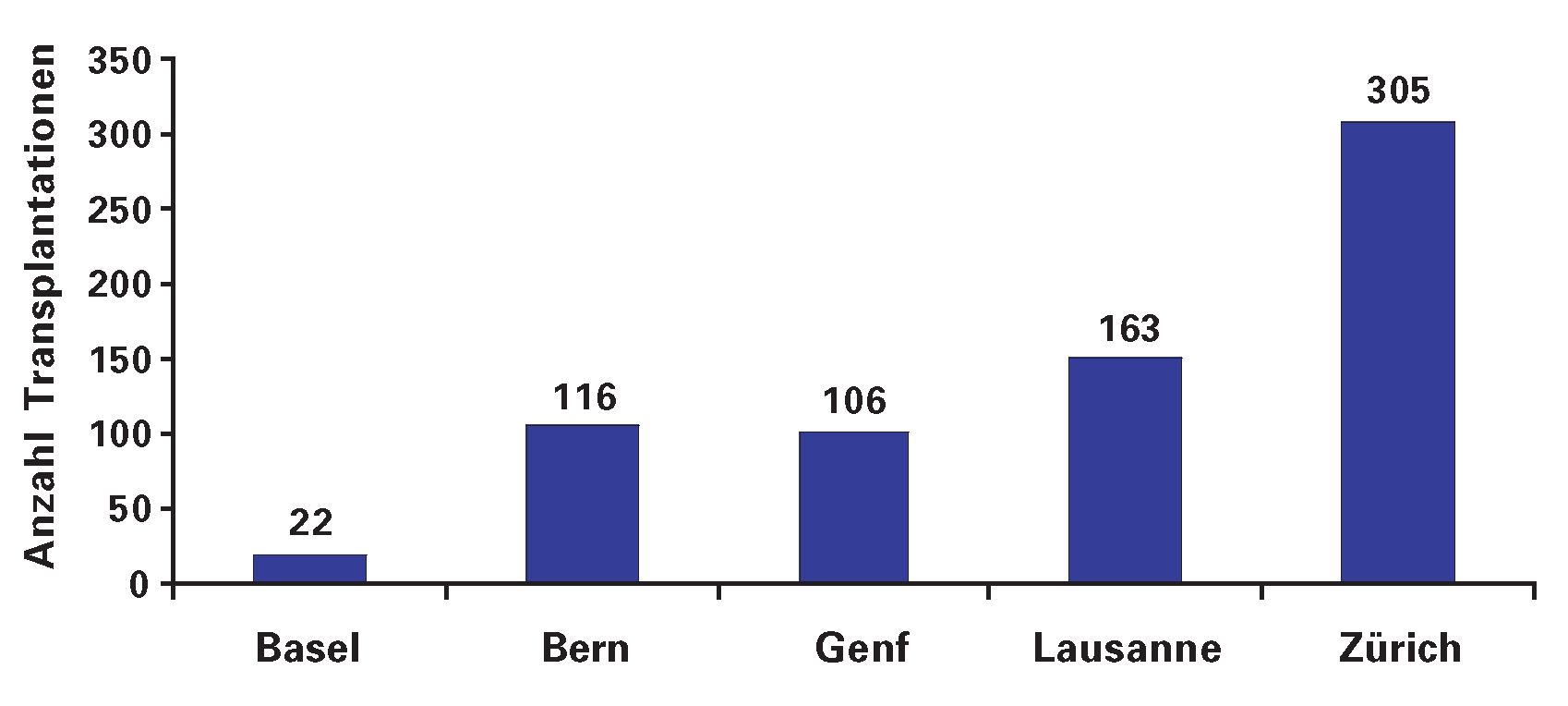
In der Schweiz wurden zwischen 1985 und 2004 insgesamt 690 Herzen transplantiert. Die Anzahl Herztransplantationen in den verschiedenen Universitätskliniken der Schweiz sind in Abbildung 3 dargestellt. Aufgrund der 2002 erhobenen Angaben, lebten damals 390 Patienten mit einem fremden Herz; diese werden in den verschiedenen Universitätskliniken der Schweiz regelmässig nachbetreut.
Figure 3.
Herztransplantationen in der Schweiz. Dargestellt sind die Anzahl durchgeführter Operationen in den verschiedenen Universitätskliniken der Schweiz von 1985–2004 (Quelle: Swiss Transplant; Website:
www.swisstransplant.org).
Figure 3.
Herztransplantationen in der Schweiz. Dargestellt sind die Anzahl durchgeführter Operationen in den verschiedenen Universitätskliniken der Schweiz von 1985–2004 (Quelle: Swiss Transplant; Website:
www.swisstransplant.org).
Indikationen und Abklärungen zur Herztransplantation
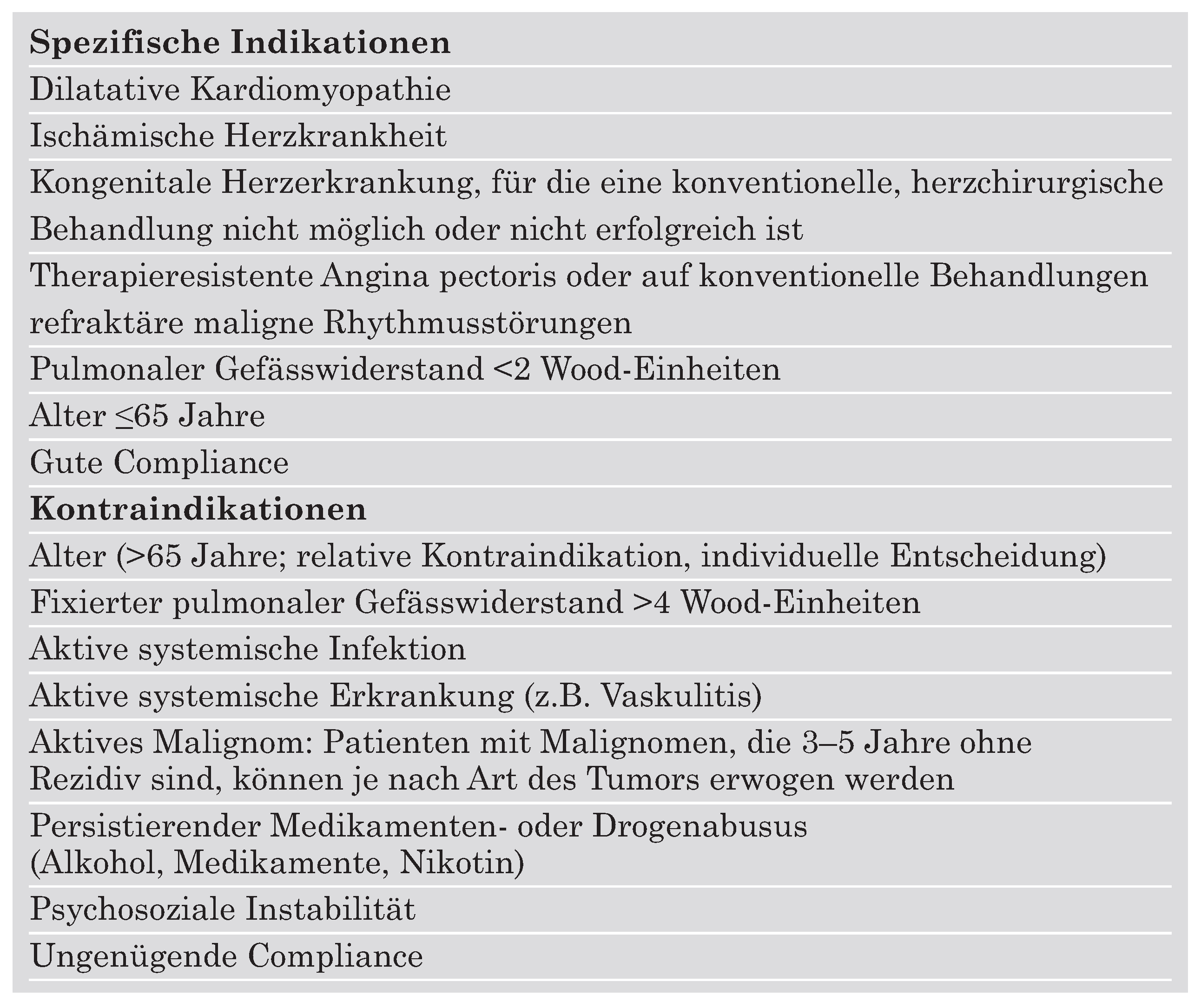
Die Indikation zur Herztransplantation ist eine schwere symptomatische Herzinsuffizienz, am häufigsten aufgrund einer terminalen koronaren Herzkrankheit mit multiplen Infarkten, Remodeling und schwer eingeschränkter linksventrikulärer Funktion (
Table 2). Weitere Indikationen sind eine schwere Kardiomyopathie, terminale Klappenvitien sowie Patienten mit kongenitalen Herzerkrankungen und einer Herzinsuffizienz.
Die kardialen Abklärungen umfassen neben der Bestimmung der linksventrikulären Auswurffraktion mittels Echokardiographie eine Koronarangiographie zur Bestimmung der Ätiologie der Erkrankung sowie eine Spiroergometrie zur Quantifizierung der Schwere der Herzinsuffizienz. Aufgrund verschiedener grösserer Studien wird heute eine maximale Sauerstoffaufnahme von ≤14 ml/min/kg Körpergewicht als Grenzwert angesehen. Die Bestimmung der natriuretischen Peptide spielt nur eine geringe Rolle [13, 14].
Zusätzlich zur kardialen Untersuchung wird vor der Transplantation eine intensive internistische Abklärung durchgeführt. Damit soll das Vorhandensein von malignen Tumoren oder anderen schweren Erkrankungen mit grösstmöglicher Sicherheit ausgeschlossen werden (
Table 2).
Verlauf nach Herztransplantation
Die akute Abstossung im Rahmen einer Herztransplantation ist heute selten geworden; entsprechend beträgt die perioperative Mortalität heute nur noch ca. 16%. Das Langzeitüberleben der Patienten wird in erster Linie durch akute und chronische Abstossungen, Infektionen sowie Begleiterkrankungen wie Lymphome und Karzinome bestimmt [
15,
16,
17,
18,
19,
20,
21,
22].
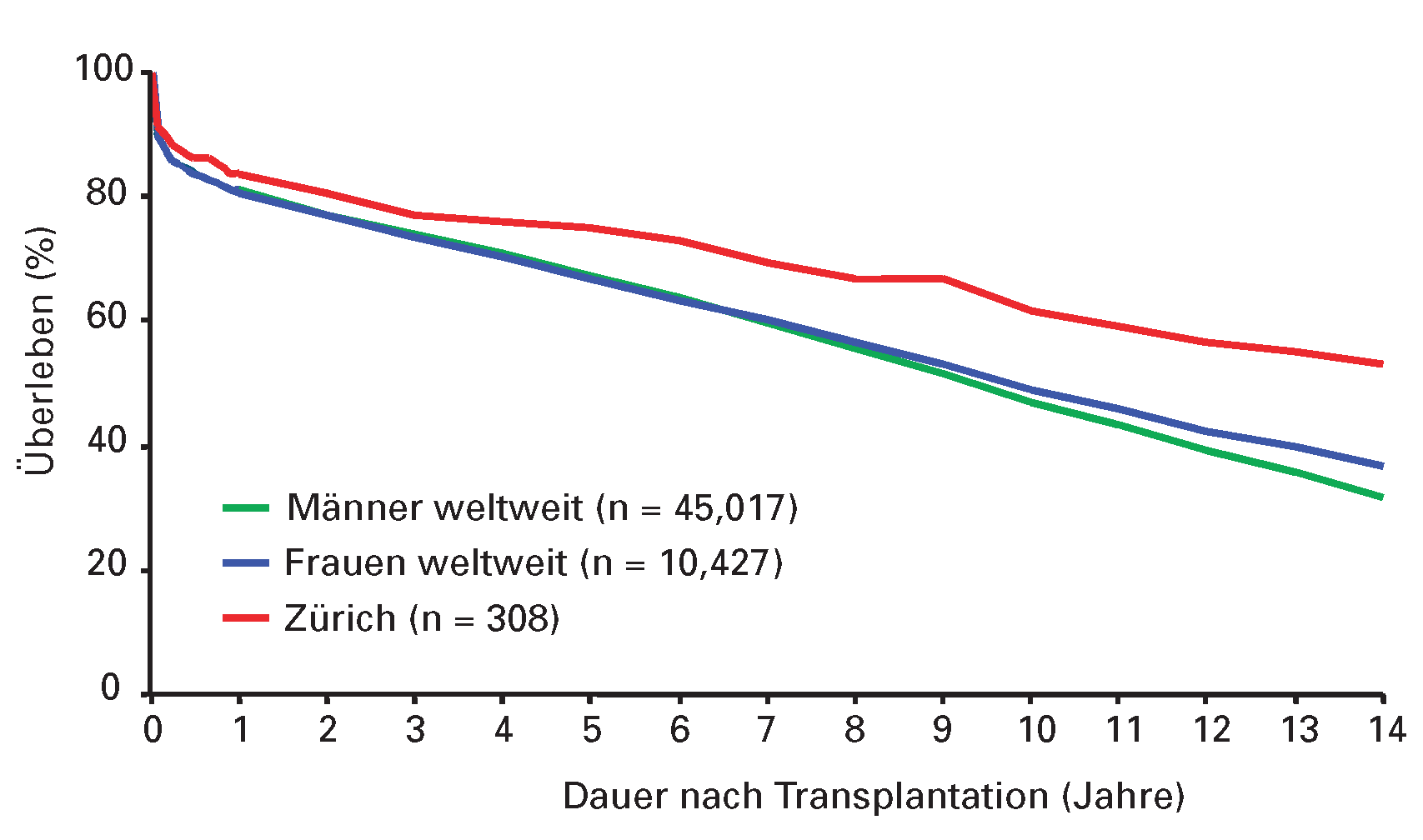
Das Langzeitüberleben der am Universitäts-Spital Zürich transplantierten Patienten ist in Abbildung 4 dargestellt. Der Vergleich zur weltweiten Überlebenskurve aller Patienten unterstreicht die Qualität der Versorgung an schweizerischen Zentren wie beispielsweise Zürich. Die Langzeitergebnisse der Herztransplantation sind heute deutlich besser als diejenigen der Lungen- bzw. Herz-Lungen-Transplantation und vergleichbar mit denjenigen der Nierentransplantation.
Transplantationsforschung
Patientenaspekte
Bei den allermeisten Patienten führt die Herztransplantation zu einer dramatischen Verbesserung der Lebensqualität. So nimmt die körperliche Belastbarkeit stark zu und erreicht bei vielen normale Werte. Es werden sogar sportliche Wettkämpfe für Herztransplantierte durchgeführt. Rund 40% der Patienten können die Arbeit wieder aufnehmen, zwei Drittel davon zu 100%. Obschon psychologische Probleme mit dem Fremdorgan entstehen können, bedürfen sie selten fachärztlicher Betreuung. Patienten nach Herztransplantation haben sich in verschiedenen Organisationen zusammengefunden, so in der Schweiz in «Ass-de-Cœur».
Medizinische Aspekte
Während in den 1960er Jahren vor allem die durch Norman Shumway initiierte Entwicklung der chirurgischen Techniken im Vordergrund stand, hat sich die Operation heute derart standardisiert, dass in diesem Bereich keine weiteren Neuentwicklungen zu erwarten sind. Im chirurgischen Bereich sind es vor allem implantierbare Pumpen, sogenannte «left ventricular assist devices» [
23], welche heute im Zentrum der Forschungsanstrengungen stehen, während das Total implantierbarer künstlicher Herzen sich wegen verschiedenster Probleme nach der Implantation, so insbesondere Blutungen, Thrombosen und Infektionen, nicht durchsetzen konnte.
Der Langzeitverlauf der Patienten (
Figure 4) wurde allerdings durch die Abstossungsprobleme bestimmt, weshalb vor allem immunologische Probleme sowie die typische diffuse koronare Herzkrankheit in transplantierten Herzen im Zentrum des Forschungsinteresses standen [24, 25]. In der Schweiz war die Forschung im Bereich Herztransplantation in den letzten 20 Jahren recht aktiv (
Figure 5). Thematisch standen klinische Fragestellungen im Vordergrund. Kriterien für die Transplantation, die immunsuppressive Behandlung und Abstossungsreaktionen sowie Fragestellungen der Graft-Arteriosklerose wurden intensiv beforscht.
Entwicklung der Herztransplantation in den letzten 10 Jahren
In den letzten 10 Jahren kam es weltweit nach einer deutlichen raschen Zunahme mit maximal 4438 Transplantationen im Jahr 1994 in den meisten Ländern zu einem Rückgang der Eingriffe während der letzten Jahre (
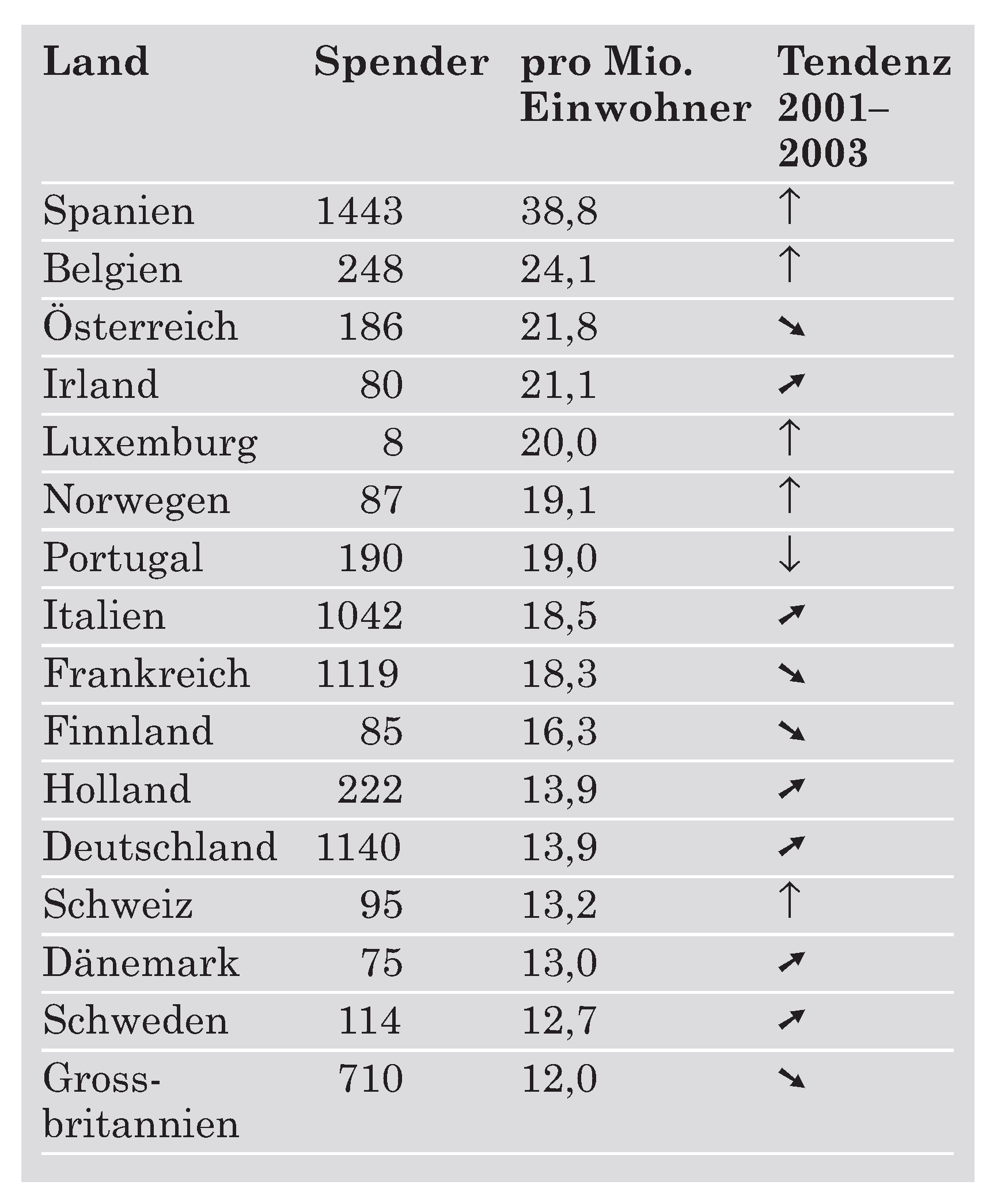
Figure 6). Diese Entwicklung ist auf verschiedene Faktoren zurückzuführen. Zum einen kam es zu einem Rückgang der Bereitschaft zur Organspende durch betroffene Familien bzw. die Spender selber. Dabei lassen sich enorme Unterschiede zwischen verschiedenen Ländern beobachten; so weist Spanien beispielsweise eine sehr hohe Spenderate pro Million Einwohner auf, während in Deutschland und der Schweiz eher wenig Organe gespendet werden (
Table 3). In Japan hat sich die Organtransplantation sogar aus kulturellen Gründen praktisch nie durchgesetzt. Verschiedene Bemühungen durch öffentliche Aktionen, die Spen dewilligkeit zu erhöhen, haben wenig Wirkung gezeigt. Als besonders schädlich erwiesen sich verschiedene Berichte über den kriminellen Organhandel.
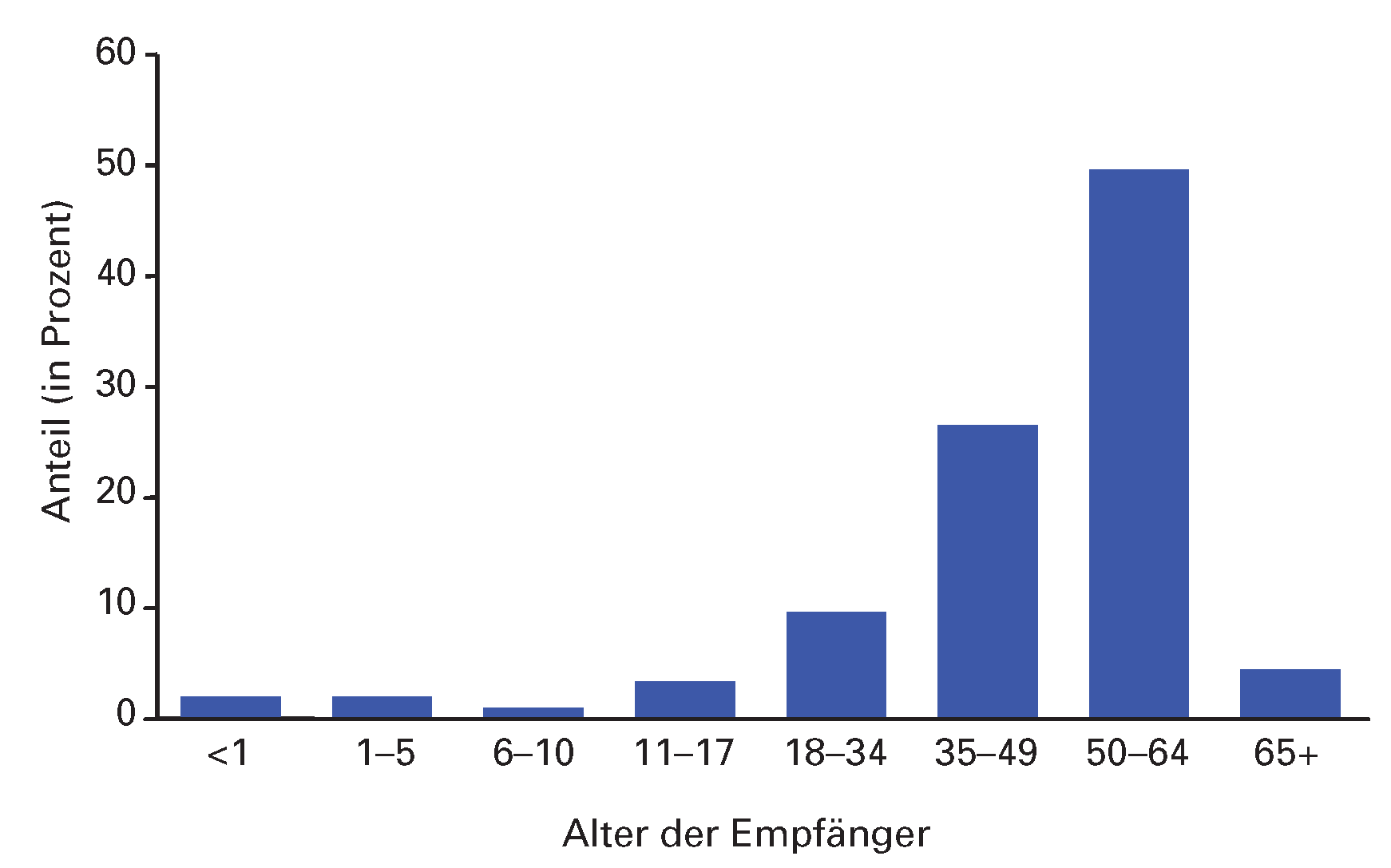
Dies erklärt teilweise, warum trotz der steigenden Inzidenz und Prävalenz von Patienten mit Herzinsuffizienz aufgrund einer koronaren Herzkrankheit, einer Hypertonie oder einer Kardiomyopathie oder seltener Erkrankungen, die Transplantationszahlen weiter abnehmen. Dieser Trend hat neben den obengenannten Aspekten auch damit zu tun, dass das Alter bei Auftreten einer schweren Herzinsuffizienz sich zunehmend von der Altersgruppe der 50–60jährigen auf die Altersgruppe der 60–70jährigen verschoben hat. Damit kommen viele Patienten mit Herzinsuffizienz aufgrund der heute gültigen Indikationen für eine Organtransplantation nicht mehr in Frage. Die Altersgrenze für eine Herztransplantation wurde ursprünglich auf 60 Jahre festgelegt, und wird heute aber individuell gehandhabt. Dennoch sind Herztransplantationen bei über 65jährigen Patienten weltweit selten (
Figure 7).
Ausblick
Was sind die Herausforderungen für die Zukunft? Die Herztransplantation bringt Patienten mit terminaler Herzinsuffizienz bei optimalem Verlauf zwar eine praktisch normale Herz- und Kreislauffunktion zurück und damit eine normale körperliche Leistungsfähigkeit. Dennoch weist die Methode neben den Kosten für den Eingriff selbst Nachteile auf, so z.B.:
- -
eine lebenslange Immunsuppression mit ihren Folgen (siehe oben)
- -
aufwendige Nachkontrollen inkl. regelmässige Myokardbiopsien und Koronarangiographien und
- -
ist mit der Abhängigkeit von der Spendefreudigkeit für Organe, als Methode in ihrer Anwendung generell beschränkt.
Diese Nachteile der Methode haben zu vielen Forschungsanstrengungen im Bereich der Immunsuppression, Xenotransplantation und Stammzellentherapie geführt, mit welchen versucht wird, fremdes Gewebe möglichst nebenwirkungsfrei und immunologisch verträglich zu machen bzw. die eigenen Zellen zur Bildung neuen Gewebes zu verwenden. Neuere Immunsuppressiva wie z.B. Rapamycin u.a.m. weisen nur marginale Vorteile gegenüber Cyclosporin auf, können aber für einzelne Patienten durchaus einen Fortschritt bedeuten. Die Xenotransplantation wird in den nächsten Jahren keine klinische Bedeutung erlangen, da neben infektiologischen Problemen Schwierigkeiten aufgrund der immunologischen Unverträglichkeit fremder Organe über Speziesgrenzen hinweg ungelöst sind. Die Stammzellen bieten neue Möglichkeiten, untergegangenes Myokardgewebe und/oder Gefässe zu regenerieren. Unkontrollierte Studien zeigten nach einer solchen Behandlung bei Patienten nach Herzinfarkt einen Anstieg der Auswurffaktoren um 5%. Im Rahmen von Forschungsprotokollen wurden am Universitäts-Spital Zürich bereits 10 Patienten mit dieser neuen Methode nach einem Herzinfarkt behandelt.
Embryonale Stammzellen bieten die theoretische Möglichkeit (vor allem in Kombination mit rekombinantem Klonieren), immunologisch verträgliche Organe für die Transplantation herzustellen. Ethische und rechtliche Einschränkungen machen solche Lösungsansätze aber schwierig.
Die Herztransplantation, wie sie heute Verwendung findet, hat aber gezeigt, dass die wirksamste Behandlung der Herzinsuffizienz der Ersatz des kranken Herzmuskels darstellt. Pumpen und künstliche Herzen wurden seit über 20 Jahren entwickelt und auch klinisch verwendet. Wenn sich die künstlichen Herzen auch als wenig praxistauglich herausstellten (vor allem Thromben und Blutungen erwiesen sich als grosse Probleme), so gehören die sogenannten «Left-Ventricular Assist Devices (LVAD)» zum Arsenal eines jeden Zentrums, welches sich mit Patienten mit schwerer Herzinsuffizienz beschäftigt. Diese Pumpen, welche das insuffiziente Herz unterstützen, können heute auf der Intensivstation für Tage bis Wochen verwendet werden, ja, neuere Modelle können sogar implantiert werden und wurden am UniversitätsSpital Zürich in den letzten Jahren bis zu 12 Monaten eingesetzt. Pumpen für den Langzeitgebrauch sind vor allem als «bridging» bis zur Transplantation ein grosser Fortschritt [
22].
Ausblick für die Schweiz
Der weltweite Rückgang der Herztransplantationen hatte auch Auswirkungen auf die Schweiz: Während 1994 Zürich mit 31 Herztransplantationen das mit Abstand grösste Herztransplantationszentrum der Schweiz war, sind die jährlichen Zahlen durch die Aufnahme von Herztransplantationen in Bern und Basel zurückgegangen (
Table 1). Das hat dazu geführt, dass an allen 5 Schweizer Universitätsspitälern relativ wenige Herztransplantationen durchgeführt werden und dies auch an Zentren mit zeitlich nur sehr limitierter Erfahrung (
Table 1 und
Figure 3). Die «Groupe des Quinze», der Rat der Weisen (d.h. die Dekane, Spital- und Gesundheitsdirektoren der Universitätskantone) hat sich dieses Problems angenommen und die Transplantationsmedizin als Gesamtes zu regeln versucht. Dabei kam in schweizerischer Manier zunächst die helvetische Gieskanne zum Einsatz; so wurde versucht, Organtransplantationen gleichmässig zu verteilen, um alle Kantone zufrieden zu stellen. Diesem Konzept der allgemeinen Verteilung hat der Regierungsrat des Kantons Zürich in seiner Motion vom 12. 01. 2005 das Konzept von zwei übergreifenden Transplantationszentren in der Schweiz entgegengesetzt. Dieses Konzept sähe eine Konzentration auf zwei Zentren vor, welche das gesamte Spektrum der Transplantationsmedizin anbieten würden. Alternativ liessen sich auch drei Zentren denken. Dies hätte den Vorteil, dass zentrale Dienstleistungen wie die Transplantationskoordination, Immunologie, Infektiologie und Pathologie, welche für die Nieren-, Lungen-, Herz- und andere Organtransplantationen gleich wichtig sind (
Table 4), auf hohem Niveau betrieben werden könnten und man die kritische Masse an Transplantationen insgesamt und damit Qualität und Patientenbetreuung verbessern könnte.
Das Modell der gleichmässigen Verteilung von Transplantationen an verschiedenen Zentren hat sicher den Vorteil höherer politischer Akzeptanz. Darüber hinaus würden dadurch aber weder Kosten gespart, noch Kompetenzzentren generiert; vor allem würde in der jetzigen vorgeschlagenen Form die bisherige Erfahrung und akademische Bedeutung der in Frage kommenden Zentren nicht berücksichtigt. Ebenso wenig käme bei diesem Vorgehen die Bedeutung der Kinderherzchirurgie zum Zuge. Gegenwärtig werden in Zürich pro Jahr etwa 300 Kinder mit kongenitalen Herzfehlern operiert, während andere Schweizer Zentren gar nicht (Basel) oder über bedeutend kleinere kinderherzchirurgische Zentren verfügen. Herztransplantationen bei Kindern sind zwar selten, sollten aber auch nach europäischen Richtlinien zu einem kinderchirurgischen Zentrum gehören.
Folgerungen
Zusammenfassend hat die Schweiz sehr erfolgreiche Herztransplantationszentren entwickelt. Zukünftig scheint sich dieses Gebiet zu komprehensiven Transplantations-Zentren zu entwickeln, welche alle Arten der Organverpflanzung anbieten. Zur Behandlung der Herzinsuffizienz wird ein solches Zentrum nicht nur neben der medikamentösen Therapie die Herztransplantation anbieten müssen, sondern auch verwandte Verfahren wie LVAD, biventrikuläre Schrittmacher und vielleicht bald die Stammzellentherapie. In der Schweiz sollten bei politischen Entscheiden mehr als bisher diese Aspekte, die gesamte Erfahrung und die akademische Leistung der 5 Zentren in Betracht gezogen werden.