Einführung
Die Mitralinsuffizienz (MI) ist die häufigste Herzklappenerkrankung allgemein und, nach der Aortenstenose, die zweithäufigste bei hospitalisierten Patienten [
1]. Die Prävalenz einer mittelschweren Mitralinsuffizienz beträgt etwa 1,9%, die einer schweren Mitralinsuffizienz 0,2%. Sie ist im Alter zunehmend [
2]. Der Verlauf der Erkrankung ist häufig schleichend und Symptome treten meist erst in fortgeschrittenen Stadien auf.
Die Behandlung einer schweren Mitralinsuffizienz war bisher eine herzchirurgische Domäne. Die operative Mitralklappenrekonstruktion ist heute Therapie der Wahl für die Korrektur der Mitralinsuffizienz verschiedener Ätiologien, da sie hinsichtlich der perioperativen Morbidität und Mortalität sowie im Bezug auf die Langzeitergebnisse dem Mitralklappenersatz überlegen ist. Der beste Zeitpunkt der chirurgischen Klappensanierung wird zurzeit kontrovers diskutiert [
3,
4]. Viele Patienten werden jedoch ohnehin erst spät diagnostiziert, zu einem Zeitpunkt also, in welchem das Operationsrisiko für eine Mitralklappenrekonstruktion oder einen Mitralklappenersatz hoch ist. In den letzten Jahren wurden verschiedene neue perkutane Behandlungsmethoden entwickelt, welche in erster Linie für diese Patientengruppe eine echte Alternative zur operativen Behandlung der Erkrankung werden könnten. Ein detaillierter Überblick über die verschiedenen klassischen und neueren Behandlungsmethoden und deren Indikationen wurde kürzlich publiziert [
5].
In Anlehnung an die chirurgische «Alfieri-Stich»-Technik [
6], bei der mittels einer «edge-to-edge»-Naht der beiden gegenüberliegenden Mitralsegel eine Reduktion des Mitralinsuffizienzjets erreicht werden kann, wurde von der kalifornischen Firma Evalve eine perkutane Technik entwickelt (Abb. 1), bei der die beiden Mitralsegel nicht genäht, sondern «edge-to-edge» aneinander «geclipt» werden. Der Clip besteht aus einer (MRI-kompatiblen) metallischen Legierung, überzogen mit Polyester, um den Heilungsprozess zu beschleunigen. Bis heute wurde diese Technik in zwei klinischen Studien evaluiert. Die EVEREST-I-Studie [
7] war eine reine Machbarkeits- und Sicherheitsstudie; in der noch nicht abgeschlossenen, prospektiv randomisierten EVEREST-II-Studie wurden hochselektionierte Patienten mit MitraClip
® behandelt und mit Patienten verglichen, welche einer operativen Mitralklappenrekonstruktion unterzogen wurden. Die Einschlusskriterien waren in beiden Studien äusserst streng, so dass nicht von einer «real-world»-Population ausgegangen werden kann.
Abbildung 1.
Das Gerät zur Implantation des Clips besteht aus einem steuerbaren Führungskatheter und einem steuerbaren Clip-Delivery-System. Ein Bild des Clips ist im Kästchen unten rechts dargestellt.
Abbildung 1.
Das Gerät zur Implantation des Clips besteht aus einem steuerbaren Führungskatheter und einem steuerbaren Clip-Delivery-System. Ein Bild des Clips ist im Kästchen unten rechts dargestellt.
Wir stellen in dieser Arbeit die Erfahrungen der beiden ersten schweizerischen Zentren vor, welche seit dem Februar 2009 25 ausgewählte Hochrisikopatienten mittels dieser neuen Technik behandelt haben.
Methoden
Studiendesign
Retrospektive Analyse der Daten der ersten 25 Patienten, die seit Februar 2009 mittels perkutaner Mitralklappenrekonstruktion (MitraClip®) in zwei schweizerischen Zentren (Cardiocentro Ticino, Lugano, und Universitätsspital, Zürich) behandelt wurden.
Patientenselektion
Bei sämtlichen Patienten wurde, nach ausführlicher invasiver und echokardiographischer Abklärung, eine Klasse-IIndikation zur chirurgischen Sanierung der Mitralklappe gestellt. Der Entscheid zur transvenösen Intervention wurde multidisziplinär getroffen. Die Patienten wiesen entweder ein durch Berechnung des logistischen EuroScores bzw. STSScores (für Mortalität) definiertes hohes Operationsrisiko auf oder waren wegen anderer, nicht durch Risikoberechnungen erfasster Kriterien für eine chirurgische Mitralklappensanierung ungeeignet.
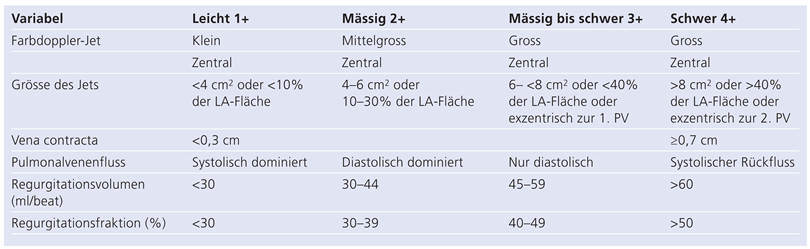
Als echokardiographisches Haupteinschlusskriterium wurde eine schwere Mitralinsuffizienz (3+ bis 4+) basierend auf den Empfehlungen der ACC (Tab. 1) [
8] definiert. Ätiologisch wurde zwischen einer funktionell-ischämischen, einer funktionell nicht-ischämischen und einer degenerativen Ursache des Mitralvitiums unterschieden.
Tabelle 1.
Definition des Schweregrades der Mitralinsuffizienz.
Tabelle 1.
Definition des Schweregrades der Mitralinsuffizienz.
Ausschlusskriterium für den Einsatz des Clips waren ein schwer verkalkter Mitralanulus, eine Klappenöffnungsfläche <4,0 cm2, ein «flail leaflet» von >15 mm mit Koadaptations-abstand von >12 mm, ein tethering von >11 mm, eine floride Endokarditis, ein Thrombus in den Vorhöfen oder allfällige sonstige anatomische Begebenheiten, die eine solche Behandlung ausschliessen.
Technik
Die Behandlung erfolgt im Herzkatheterlabor in Rückenlage. Um eine kontinuierliche Überwachung des Eingriffs mittels transösophagealer Echokardiographie (TEE) zu ermöglichen, werden die Patienten endotracheal intubiert, der Einsatz einer Herz-Lungen-Maschine ist jedoch nicht notwendig. Nach Punktion der Vena femoralis und Gabe von 5000 IU Heparin wird ein Mullins-Katheter (8F) in den rechten Vorhof vorgeschoben. Unter TEE-Kontrolle in der bikavalen Schnittebene wird der optimale Ort der Vorhofseptumpunktion bestimmt. Diese sollte idealerweise mit 3,5 bis 4 cm Abstand zur Mitralklappenebene und relativ posterior erfolgen. Dieser Abstand ist notwendig um den Führungskatheter und das Trägerkathetersystem (clip delivery system) im linken Vorhof steuern zu können.
Nach erfolgreicher Punktion des Vorhofseptums wird ein steifer Draht im linken Vorhof platziert. Nach Vordilatation in der Leiste wird danach der an der Spitze steuerbare Führungskatheter (24F) unter 2D- und 3D-TEE-Kontrolle im linken Vorhof positioniert (Abb. 2). Über den Führungskatheter wird das ebenfalls steuerbare Trägerkathetersystem bis in den linken Vorhof vorgeschoben und unter TEE-3DKontrolle erst senkrecht in Richtung auf die Mitralkommissuren und dann genau mitten in den Insuffizienzjet ausgerichtet. Auf der Spitze des Systems ist ein Clip montiert. Die Ausrichtung des Clips wird in unterschiedlichen Projektionen (2-, 3-, 4-Kammerschnitt, mittels X-plane und 3D) kontrolliert und nach Eröffnung des Clips im linken Vorhof seine Position im Verhältnis zu den Segelsegmenten und Kommissuren geprüft. Das Trägerkathetersystem wird dann in den linken Ventrikel durch die Mitralklappe vorgeschoben. Beim langsamen Zurückziehen des Systems werden die Klappensegel von den Clip-Flügeln und den sogenannten «Grippern» erfasst; schliesslich wird beim Schliessen der Flügel versucht, genau die beiden gegenüberliegenden Mitralsegelanteile zu ergreifen, welche als ursächlich für die Insuffizienz angesehen werden und diese dann mittels vollständigem Schluss des Clips aneinander zu fixieren.
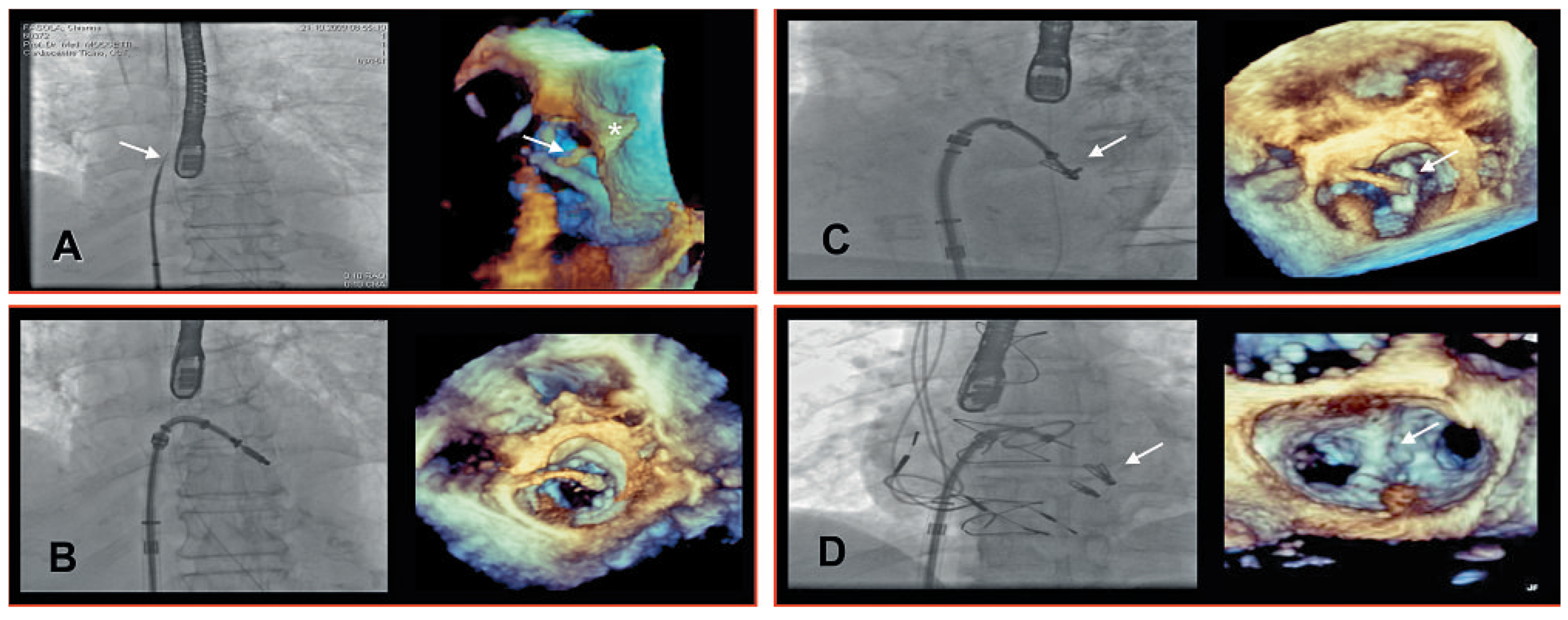
Abbildung 2.
Durchleuchtung und transösophageale 3-dimensionale echokardiographische (TEE-3-D-) Bilder von: A Transseptale Punktion, der Pfeil zeigt die transeptale Nadel. TEE-3-D-Bild mit Rekonstruktion des Vorhofseptums zeigt die Vorwölbung bei der Punktion (Stern). B Ausrichtung des Trägerkatheters auf die Mitralklappe; TEE-3-D mit Sicht vom linken Vorhof in Richtung Mitralklappe. C Platzierung des geöffneten MitraClips® in die Mitralklappe (TEE-3-D-Sicht vom linken Vorhof in Richtung Mitralklappe). D Clip ist vom Trägerkatheter freigesetzt (Pfeil, in diesem Fall wurden 2 Clips implantiert); TEE-3-D-Blick vom LA auf das entstandene «double orifice» der Mitralklappe. LA = linker Vorhof. TEE = transösophageale Echokardiographie.
Abbildung 2.
Durchleuchtung und transösophageale 3-dimensionale echokardiographische (TEE-3-D-) Bilder von: A Transseptale Punktion, der Pfeil zeigt die transeptale Nadel. TEE-3-D-Bild mit Rekonstruktion des Vorhofseptums zeigt die Vorwölbung bei der Punktion (Stern). B Ausrichtung des Trägerkatheters auf die Mitralklappe; TEE-3-D mit Sicht vom linken Vorhof in Richtung Mitralklappe. C Platzierung des geöffneten MitraClips® in die Mitralklappe (TEE-3-D-Sicht vom linken Vorhof in Richtung Mitralklappe). D Clip ist vom Trägerkatheter freigesetzt (Pfeil, in diesem Fall wurden 2 Clips implantiert); TEE-3-D-Blick vom LA auf das entstandene «double orifice» der Mitralklappe. LA = linker Vorhof. TEE = transösophageale Echokardiographie.
Nun erfolgt eine kritische Evaluation des primären Resultats bezüglich Abnahme des Insuffizienzjets sowie Stabilität der aneinander fixierten Anteile der Mitralsegel in diversen 2DTEE-Projektionen sowie in 3D. Bei unzureichendem Ergebnis kann der Clip wieder geöffnet, zurückgezogen und falls nötig entfernt werden. Bei zufriedenstellendem Ergebnis, d.h. nachweisbar deutlicher Abnahme der Mitralinsuffizienz, sicher am Clip fixierte Mitralsegelanteile, kein signifikanter transvalvulärer Gradient, wird der Clip vom Katheter gelöst und an der Mitralklappe im Herzen belassen. Gegebenenfalls kann ein zweiter Clip eingesetzt werden (sowohl in gleicher Sitzung, als auch im Rahmen einer zweiten Intervention). Als Endergebnis entsteht, analog zum Alfieri-Stich, ein zweigeteiltes Mitralorifizium (doppelter Mitraleinstrom) mit meist deutlicher Reduktion des Insuffizienzjets. Vor Implantation beim ersten Patienten im jeweiligen Zentrum wurden die Operateure in einem zweitägigen praktischen Kurs durch einen erfahrenen Proktor und Techniker der Firma geschult. Bei bislang sämtlichen Eingriffen war zudem eine von der Firma Evalve bestellte Person während der Intervention im Kathetersaal anwesend, um bei technischen Fragen Unterstützung zu leisten.
Resultate
Am 18. 2. 2009 wurde die erste MitraClip®-Implantation der Schweiz in Lugano vorgenommen, Zürich folgte am 5.5.2009. Seitdem wurden in der Schweiz bis Ende 2009 insgesamt 25 Patienten mittels perkutaner Mitralklappenrekonstruktion behandelt, 13 am Cardiocentro Ticino und 12 am Universitätsspital Zürich.
Die klinischen Parameter vor dem Eingriff sind in Tabelle 2 verzeichnet. Das mittlere Alter der Patienten betrug 69 ± 9,8 Jahre, wobei 60% männlich waren. Die Ursache der Mitralinsuffizienz war bei 11 Patienten (44%) funktionell-ischämischer Genese. Bei 3 Patienten (12%) war die Ursache funktionell nicht ischämischer und bei 7 Patienten (28%) degenerativer Natur. Bei 4 Patienten führten zwei oder mehrere Faktoren zum Entstehen der Mitralinsuffizienz. Es handelte sich um funktionell stark beeinträchtigte Patienten; 92% befanden sich in einer NYHA-Klasse III oder IV und wiesen eine schwer eingeschränkte linksventrikuläre Funktion auf (Median der LVEF: 36% ± 16%). Entsprechend war das Operationsrisiko stark erhöht (Median EuroScore: 15% ± 20%; STS Score: 7% ± 9%;). Bei 14 Patienten (56%) lag das Risikoprofil in einem Bereich, der vergleichbar ist mit der Patientenpopulation des «EVEREST high risk»-Registers [
9], definiert durch eine LVEF <25%, einen LVESD >55 mm, eine schwere pulmonal-arterielle Hypertonie oder eine vom Herzchirurgen attestierte absolute Kontraindikation zur operativen Behandlung.
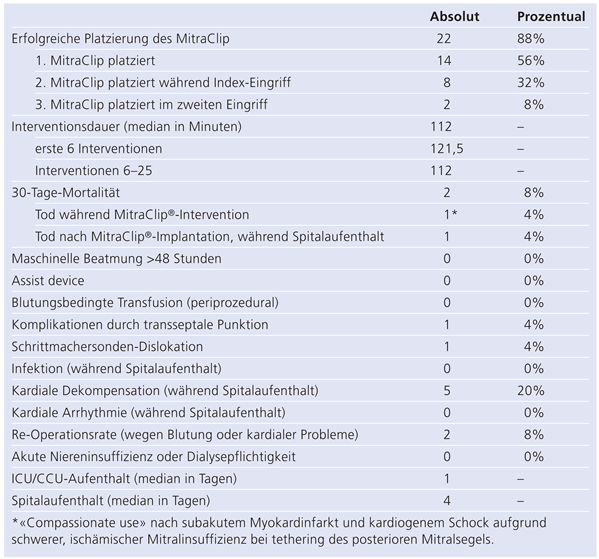
Die periprozeduralen Ergebnisse sind in Tabelle 3 zusammengefasst. Die erfolgreiche Implantation von einem oder zwei Clips gelang bei 22 der 25 Patienten (88%). Bei 32% der Patienten erfolgte die Implantation eines zweiten Clips während der Index-Intervention, in 2 Fällen (8%) wurde ein zweiter Clip in einer Folgeintervention erfolgreich implantiert. Die Implantationsdauer («device time») betrug im Median 112 Minuten (Bereich 48–251). Dabei zeigte sich tendenziell eine Lernkurve. Die Implantationsdauer der ersten 6 Patienten (erste 3 Patienten je Zentrum) dauerte mit einem Median von 122 Minuten noch etwas länger (Bereich 72– 200), bei den letzten 5 Eingriffen dauerte die Clip-Implantation im Median noch 75 Minuten (54–112).
Tabelle 2.
Klinische Parameter vor MitraClip®.
Tabelle 2.
Klinische Parameter vor MitraClip®.
Tabelle 3.
Periprozedurale Daten (n = 25).
Tabelle 3.
Periprozedurale Daten (n = 25).
Verbesserung der Mitralinsuffizienz
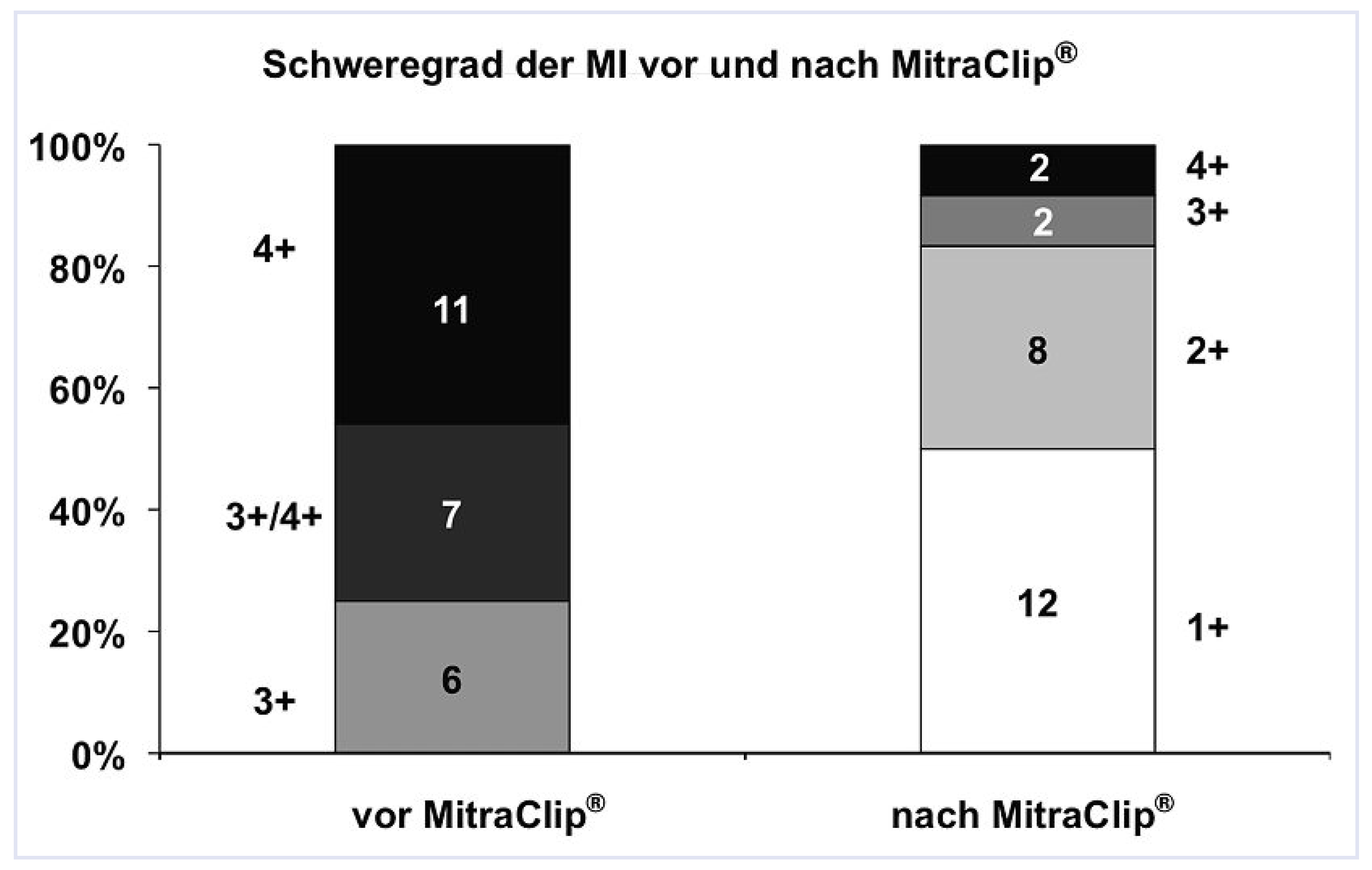
Sämtliche Patienten (n = 25) hatten vor der Intervention einen Schweregrad der Mitralinsuffizienz von mindestens 3+ (Abb. 4). Nur bei 3 Patienten konnte der Schweregrad durch den Eingriff nicht verbessert werden.
Bei sämtlichen, erfolgreich implantierten Patienten (n = 22) kam es zu einer Verbesserung der Mitralinsuffizienz, bei 15 (68%) um mehr als zwei Schweregrade, bei 7 Patienten (32%) um mehr als einen Schweregrad. Bei 20 der 22 erfolgreich implantierten Patienten (91%) lag der Schweregrad der MI nach Intervention zwischen 1+ und 2+.
Abbildung 3.
Verlauf des Schweregrades der echokardiographisch definierten Mitralinsuffizienz nach Implantation des Clips.
Abbildung 3.
Verlauf des Schweregrades der echokardiographisch definierten Mitralinsuffizienz nach Implantation des Clips.
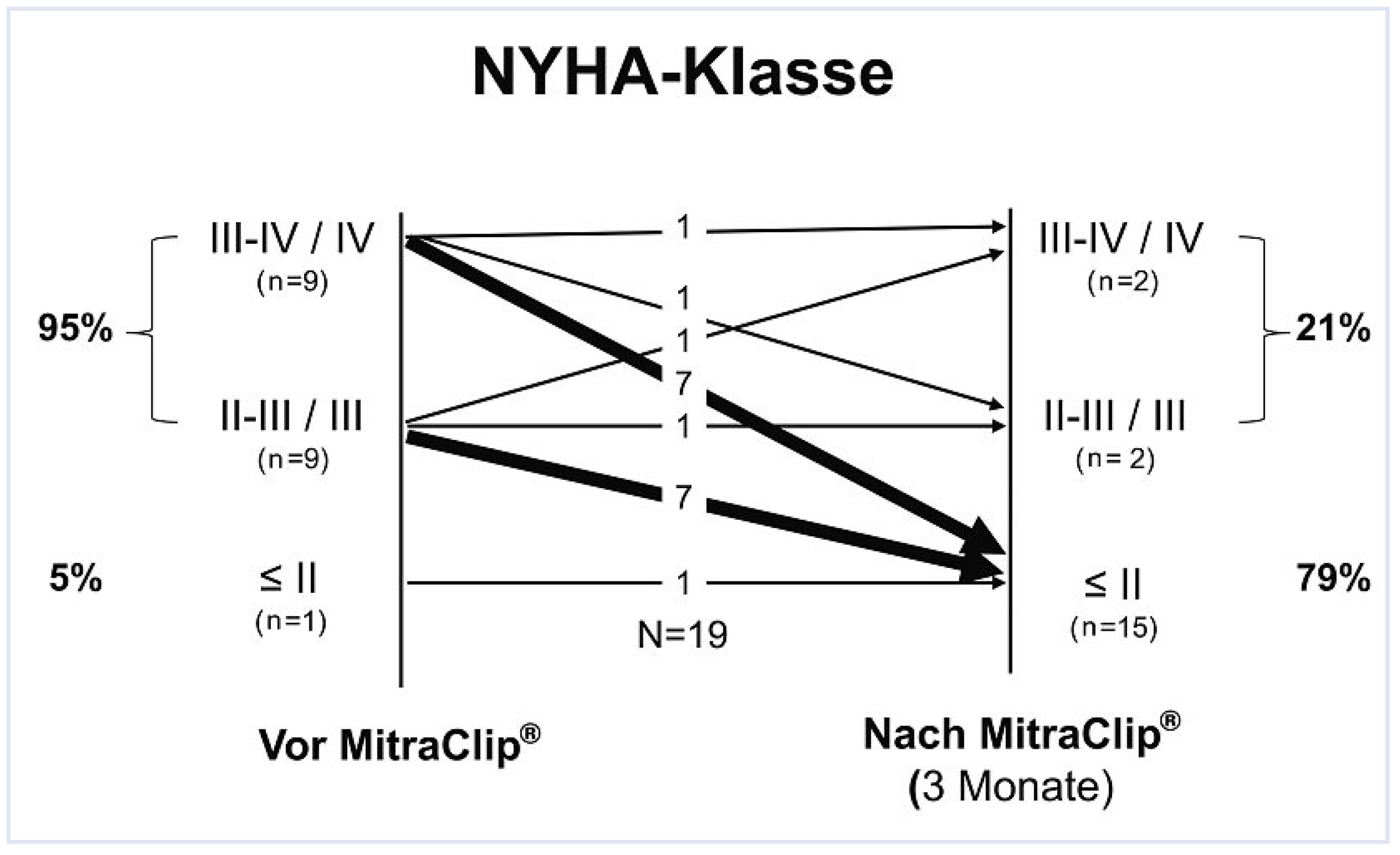
Abbildung 4.
Verlauf der Dyspnoe (gemäss NYHA-Klassifizierung) nach Implantation des Clips bei 19 Patienten, welche einen Verlauf von mindestens 3 Monaten aufweisen. Die dünnen Pfeile zeigen den Verlauf der einzelnen Patienten an, die dicken Pfeile entsprechen dem Verlauf von je 7 Patienten.
Abbildung 4.
Verlauf der Dyspnoe (gemäss NYHA-Klassifizierung) nach Implantation des Clips bei 19 Patienten, welche einen Verlauf von mindestens 3 Monaten aufweisen. Die dünnen Pfeile zeigen den Verlauf der einzelnen Patienten an, die dicken Pfeile entsprechen dem Verlauf von je 7 Patienten.
Funktionelle Verbesserung
Klinisch ging die Abnahme des Schweregrads der Mitralinsuffizienz mit einer Verbesserung der NYHA-Klasse von im Mittel 3,2 ± 0,5 auf 2,1 ± 0,7 nach einem Monat einher (n = 19, p < 0,001). Bei 15 (79%) kam diese klinische Verbesserung effektiv zum Tragen, bei 4 Patienten (21%) blieben die Beschwerden unverändert bzw. kam es zu einer Verschlechterung der Symptomatik (Abb. 4).
Spitalverweildauer
Der Median der Verweildauer auf einer Überwachungs- oder Intensivstation betrug einen Tag (Bereich: 1–23 Tage), die mediane gesamte Hospitalisationsdauer lag bei 4 Tagen (Bereich: 2–60 Tage). 3 Patienten blieben wegen Herzinsuffizienz verhältnismässig lange hospitalisiert.
Komplikationen
Als primär nicht erfolgreich implantiert wurden solche Patienten klassifiziert, bei denen der Clip entweder effektiv nicht implantiert werden konnte, oder es aufgrund der Clip-Implantation zu einer Verschlechterung der Mitralinsuffizienz, z.B. durch Zerstörung von Strukturen des Klappenapparats gekommen ist (n = 3).
Zwei dieser Patienten mussten nach primär nicht erfolgreicher Clip-Implantation operiert werden. In einem Fall konnte bei einem chronisch herzinsuffizienten Patienten aus technischen Gründen keine optimale Position für einen zweiten Clip gefunden werden, nachdem schon die Implantation des ersten Clips nicht zur Abnahme der Mitralinsuffizienz geführt hatte. Einige Tage danach wurde er trotz eines sehr hohen operativen Risikos (log EuroScore 53%, STSScore 9%) einer chirurgischen Mitralklappensanierung zugeführt. Der Patient verstarb nach 40 Tagen an einer Pneumonie.
Bei einem zweiten Patienten (log EuroScore 29%, STS-Score 10%) kam es zu einer durch den Clip bedingten Ruptur eines Sehnenfadens, was einerseits die Mitralinsuffizienz weiter verschlimmerte und andererseits den Fortgang der Intervention aus technischen Gründen unmöglich machte. Der Patient verstarb am zweiten postoperativen Tag nach notfallmässigem chirurgischem Mitralklappenersatz.
Bei einer dritten, 83-jährigen Patientin (log EuroScore 31%, STS-Score 19%) wurde die Implantation eines MitraClip® acht Tage nach postero-lateralem Myokardinfarkt zur Behebung einer akuten, ischä-misch bedingten, schweren Mitralinsuffizienz als «compassionate therapy» auf Wunsch der Angehörigen eingesetzt, nachdem von herzchirurgischer Seite eine Operation ausgeschlossen wurde. Nach primär erfolgreicher Platzierung des Clips kam es jedoch infolge der massiven Zunahme des intraventrikulären Druckes zu einem Abriss des infarzierten Papillarmuskels und die Patientin verstarb kurz nach der Intervention.
Als «MACE» wurden die 30-Tage-Gesamtmortalität definiert, ein kardial oder blutungsbedingter herzchirurgischer Eingriff, eine prolongierte (>48 Stunden) mechanische Ventilation, die Notwendigkeit eines «Assist device» sowie lebensbedrohliche periprozedurale Komplikationen wie Blutung, Perikardtamponade sowie iatrogene Mitralstenose. Die «MACE»-Rate bei unserer Klientel lag bei 20% (n = 5).
Neben den drei oben beschriebenen Patienten kam es bei einem Patienten im Rahmen der transseptalen Punktion zu einer Perikardtamponade, welche jedoch erfolgreich therapiert werden konnte und daher ohne Konsequenzen blieb, und bei einer weiteren Patientin (log EuroScore 8%, STS-Score 1,5%) kam es nach Implantation zweier Clips zu einem signifikanten Anstieg des transmitralen Gradienten, so dass die Patientin nach 6 Monaten schliesslich doch einem operativen Mitralklappenersatz unterzogen werden musste.
Diskussion
Bei der vorgestellten Technik handelt es sich um eine neuartige perkutan-transvenöse Rekonstruktion der insuffizienten Mitralklappe mittels Implantation von «Clips», die das anteriore und das posteriore Mitralsegel, ähnlich wie bei der chirurgischen «edge-to-edge»-Technik nach Alfieri [
6], aneinander fixieren. Es ist eine anspruchsvolle Technik, die einen sicheren Umgang mit transseptaler Punktion und gute Kenntnisse der Anatomie der Mitralklappe erfordert. Die genaue Bestimmung des Ortes der transseptalen Punktion und die Ausrichtung des Trägerkathetersystems auf die Mitralkommissuren erfolgt grösstenteils unter echokardiographischer Führung, was die Wichtigkeit einer optimalen Kommunikation zwischen Operateur und Echokardiographeur bei dieser Intervention deutlich macht. Letzterer sollte ebenfalls über ausgezeichnete Kenntnisse der Mitralklappenanatomie sowohl in 2-D- als auch in 3-D-Technik verfügen.
Wie bei allen technisch anspruchsvollen Eingriffen wurde auch bei den vorgestellten Fällen eine nicht zu unterschätzende Lernkurve beobachtet, was sich sowohl in der Untersuchungsdauer als auch im primären Resultat widerspiegelte. Entscheidend für den Erfolg des Eingriffs ist die korrekte Positionierung des/der Clips, was in einigen Fällen, abhängig vom Entstehungsort des Insuffizienzjets, schwierig sein kann und die Prozedur daher viel Zeit und Geduld beanspruchen kann, was für das Endergebnis aber wenig Einfluss hat. Dem Operateur steht genügend Zeit für die optimale Platzierung des Clips zur Verfügung, da es in der Regel nicht zu hämodynamischen Problemen kommt.
Sollte es nicht zur Reduktion der Mitralinsuffizienz nach Implantation kommen, kann der MitraClip® operativ im Rahmen einer chirurgischen Mitralklappenrekonstruktion entfernt werden, ohne dass von einem Schaden am Klappenapparat auszugehen ist. Insgesamt kann man nach den ersten 25 in der Schweiz behandelten Patienten folgendes Fazit ziehen:
Die Patienten wiesen ein deutlich höheres Risikoprofil auf als in der Patientenpopulation der zwei bisher publizierten EVEREST-I- und -II-Studien und ist am ehesten vergleichbar mit dem Patientengut aus dem «EVEREST high risk»-Register [
9]. Der EuroScore lag im Median bei 15,7% und die EF mit 35% leicht über der des Registers. Das Risiko vieler Patienten wurde jedoch nur ungenügend von den üblichen Berechnungsmethoden erfasst, in einigen Fällen wurden die Patienten von herzchirurgischer Seite als inoperabel angesehen. 48% der Patienten hatten bereits einen Myokardinfarkt, bei insgesamt 32% der Fälle waren in der Vergangenheit bereits ein oder mehrere herz- bzw. thoraxchirurgische Eingriffe erfolgt, in 16% der Fälle waren die Patienten bereits resynchronisiert und in 64% der Fällen bestand eine schwere chronische Niereninsuffizienz, charakterisiert durch einen Serumkreatininwert von über 200 µmol/l.
Insgesamt kann von einer positiven Erfahrung mit dieser neuen perkutan-transvenösen Intervention gesprochen werden. So konnten trotz des beschriebenen Hochrisikoprofils bei 88% der Fälle ein oder zwei Clips erfolgreich platziert werden, und die Rate der schweren Komplikationen («MACE») in den ersten 30 Tagen lag mit 20% (5 Patienten) in einem zu erwartenden Rahmen—nicht höher als im vergleichbaren Klientel des «EVEREST high risk»-Registers [
9]. Erwähnenswert ist, dass es lediglich bei zwei Patienten gänzlich unmöglich war, den Clip zu platzieren, bei beiden Fällen handelte es sich um eine Mitralinsuffizienz der lateralen Kommissur, deren Behandlung mittels MitraClip
® allseits als schwierig angesehen wird.
Konnte(n) ein/die Clip(s) erfolgreich platziert werden, kam es bereits während des Eingriffs zu einer deutlichen Reduktion der Mitralinsuffizienz und anschliessend zu einer anhaltend verbesserten Leistungsfähigkeit. Bezogen auf das gesamte Patientengut wurde bei 20 von 25 Fällen (80%) ein Grad der residuellen Mitralinsuffizienz von ≤2+ erreicht. Die Ergebnisse sind mindestens vergleichbar mit denen der EVEREST-Studie [
7] (74% der behandelten Patienten mit residueller MI ≤2+). Langzeitergebnisse liegen aktuell noch nicht vor.
Die initiale Abnahme der Mitralinsuffizienz, zusammen mit der Verbesserung der Beschwerdesymptomatik kurz- und mittelfristig, lassen berechtigte Hoffnungen bezüglich eines Einsatzes dieser neuen, weniger invasiven Behandlung bei Hochrisikopatienten aufkommen.
In den bisher publizierten Studien [
7] wurde die Technik grösstenteils bei Patienten mit degenerativ bedingter Mitralinsuffizienz angewandt, welche in unserem Patientenklientel nur eine Minderheit ausmachen (n = 7; 28%). Bei 56% unserer Patienten (n = 14) war die Ursache der Mitralinsuffizienz funktionell bedingt (ischämisch bzw. nicht ischämisch im Rahmen einer schweren LV-Funktionsstörung). Es handelt sich hierbei um eine neue Patientengruppe, die der MitraClip
®-Behandlung zugeführt wurden, bei denen eine operative Sanierung der Mitralinsuffizienz aufgrund enttäuschender Langzeitergebnisse äusserst umstritten ist [
10,
11]. Die kurzfristigen Ergebnisse nach MitraClip
®-Implantation auch bei dieser Patientengruppe sind sicherlich vielversprechend, auch wenn der Langzeitverlauf wahrscheinlich eher von der Entwicklung der Herzinsuffizienz als von der Behebung der Mitralinsuffizienz abhängt. Unklar ist auch der langfristige Einfluss der MitraClip
®-Implantation auf das LV-Remodeling sowie auf eine allfällige Dilatation des Mitralanulus mit erneuter Verschlimmerung der Insuffizienz, wie es nach der chirurgischen «edge-to-edge»Technik [
6] beobachtet wurde, und welcher bisher nur durch chirurgische Implantation eines Mitralklappenrings [
12] effektiv behandelt werden konnte.
Der MitraClip®-Technik zugute kommen könnte möglicherweise die Tatsache, das in den meisten Fällen die Mitralinsuffizienz nicht völlig aufgehoben, sondern lediglich vermindert wird, was mit einer weniger grossen Belastung für die meist schon vorgeschädigten linken Ventrikel einhergehen könnte. Zudem wird durch das Clippen der gegenüberliegenden Mitralsegel eine gewisse Spannung auf die Mitralkommissur ausgeübt, welche theoretisch einer Anulusdilatation entgegenwirken könnte.
Geplant ist, sämtliche in der Schweiz mit dieser Technik behandelten Patienten in Zukunft prospektiv zu erfassen, um dieser und anderen Fragen nachzugehen.