Einleitung
Zur Behandlung von Vorhofflimmern und zur Indikationsstellung für implantierbare Defibrillatoren (ICD) existieren aktuelle Behandlungsrichtlinien [
1,
2,
3]. Trotzdem gibt es in der klinischen Praxis Situationen, in welchen diese Richtlinien nicht weiterhelfen oder ihre Umsetzung im Einzelfall schwierig ist. An zwei Beispielen sollen deshalb neue, im Jahre 2008 publizierte Daten besprochen werden.
Bedeutung von durch PM- oder ICD-detektiertem paroxysmalem Vorhofflimmern Resultate der TRENDS-Studie
Vorhofflimmern ist mit einem erhöhten Risiko für thromboembolische Komplikationen wie z.B. Hirnschlagbehaftet. Das Ausmass des Risikos und damit die Indikationsstellung zur medikamentösen Thromboembolie-Prophylaxe (Azetylsalicylsäure vs. orale Antikoagulation) beruht auf zusätzlichen klinischen Risikofaktoren, welche nach dem CHADS
2-Score beurteilt werden [
4]. Die diesbezügliche Bedeutung von lediglich paroxysmalem, oft auch asymptomatischem Vorhofflimmern ist weniger klar. Obwohl nicht mit verlässlichen Studien belegt, scheint paroxysmales Vorhofflimmern ein ähnliches Hirnschlagrisiko zu beinhalten wie permanentes Vorhofflimmern. Entsprechend sind gemäss den aktuellen Richtlinien die Empfehlungen zur Thromboembolie-Prophylaxe für paroxysmales und permanentes Vorhofflimmern identisch [
1]. Bisher bleibt unklar, ob es eine quantitative Beziehung zwischen Häufigkeit und Dauer von Episoden mit paroxysmalem Vorhofflimmern (so genannter «AF-burden») und dem Hirnschlag-Risiko gibt. Dies gilt insbesondere für nur kurze und oft asymptomatische Episoden.
In den letzten Jahren haben die Monitoring-Möglichkeiten und Speicherkapazitäten der implantierten Herzschrittmacher (PM) und Defibrillatoren (ICD) rasant zugenommen [
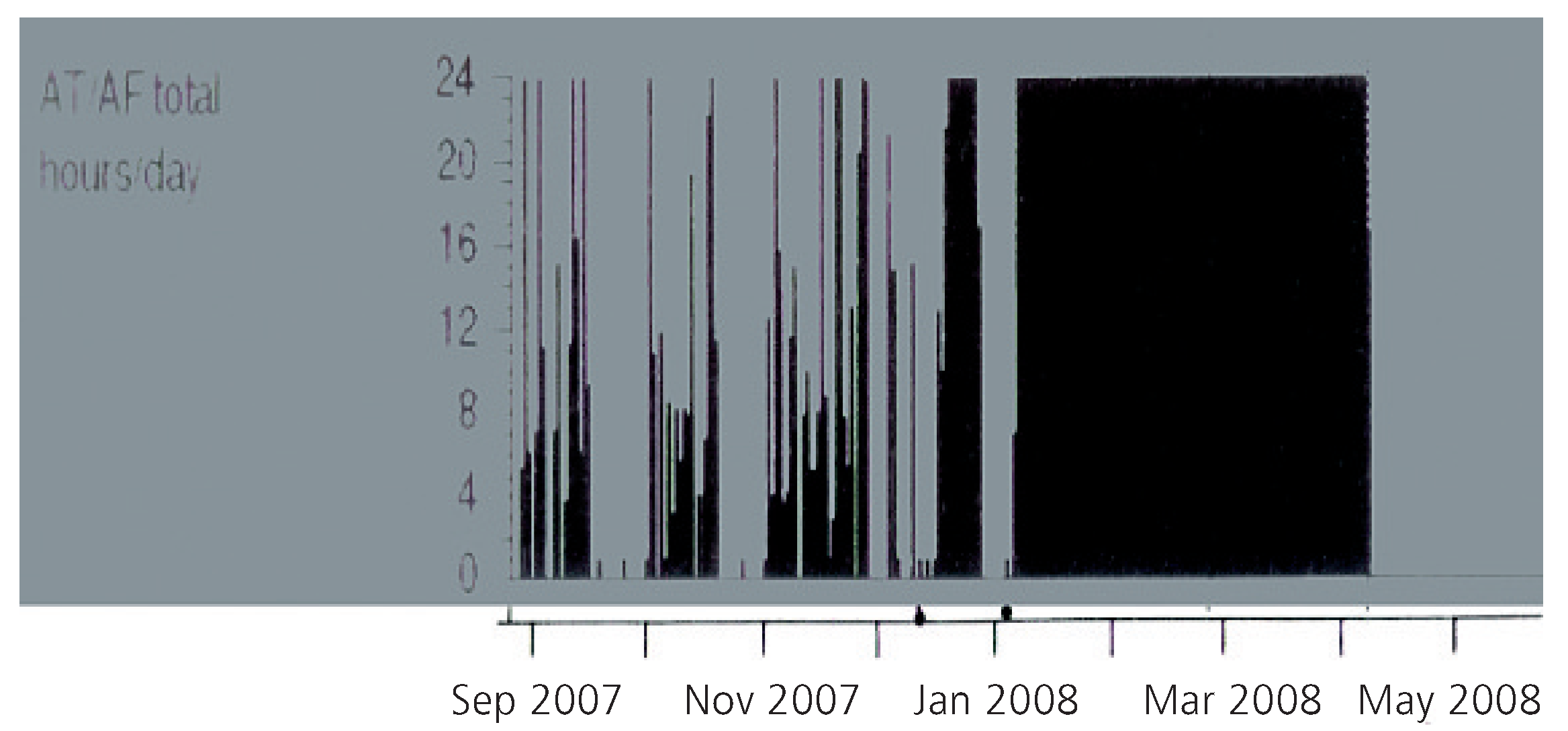
5]. Unter anderem können damit Episoden mit atrialen Tachyarrhythmien (Vorhofstachykardien, Vorhofflattern, Vorhofflimmern) dokumentiert und quantitativ erfasst werden. Dabei lassen sich Häufigkeit und Dauer der Episoden sowie deren chronologisches Auftreten darstellen (Abb. 1). Teilweise können auch die intrakardialen Elektrogramme dieser Arrhythmien aufgezeichnet werden. Diese Möglichkeiten öffnen ein weites Feld zur Symptom-Arrhythmie-Korrelation und zur Therapiesteuerung. Andererseits werden durch dieses kontinuierliche Monitoring zunehmend auch asymptomatische Arrhythmien dokumentiert und anlässlich der Routinenachsorge dieser Patienten entdeckt. Wie mit dieser «Datenflut» umzugehen ist und welche allfälligen therapeutischen Konsequenzen sich daraus ergeben, ist in vielen Fällen noch unklar. Wie in anderen Fällen hinkt hier die klinische Evidenz dem technischen Fortschritt hinterher.
Abbildung 1.
Beispiel für eine graphische Darstellung aus einem ICD-Speicher. Über die Zeitachse ist das Auftreten und die Dauer (Stunden/Tag) von Episoden mit atrialen Tachyarrhyhthmien resp. Vorhofflimmern (AT/AF) dargestellt. Das Beispiel zeigt zu Beginn noch paroxysmales Vorhofflimmern, mit häufiger und länger werdenden Episoden, zuletzt dann den Übergang in persistierendes Vorhofflimmern.
Abbildung 1.
Beispiel für eine graphische Darstellung aus einem ICD-Speicher. Über die Zeitachse ist das Auftreten und die Dauer (Stunden/Tag) von Episoden mit atrialen Tachyarrhyhthmien resp. Vorhofflimmern (AT/AF) dargestellt. Das Beispiel zeigt zu Beginn noch paroxysmales Vorhofflimmern, mit häufiger und länger werdenden Episoden, zuletzt dann den Übergang in persistierendes Vorhofflimmern.
In diesem Zusammenhang wurden am diesjährigen Kongress des «American College of Cardiology» die Resultate der TRENDS-Studie vorgestellt [6,7]. TRENDS ist eine prospektive, multizentrische Kohortenstudie (115 Zentren in USA, Kanada und Australien) über knapp 2500 Patienten mit implantierten Zweikammer-Herzschrittmachern (50%), Zweikammer-Defibrillatoren (31%) und CRT-Systemen (19%). Das primäre Studienziel war die Beantwortung der Frage, ob die von den Geräten gespeicherten Daten bezüglich Dauer allfälliger Episoden mit Vorhofstachykardien (AT) oder Vorhofflimmern (AF) einen unabhängigen Prädiktor für das Auftreten von thromboembolischen Ereignissen darstellen (kombinierter Endpunkt für ischämischen Hirnschlag, transiente ischämische Attacke (TIA) oder andere systemische Embolien). Es wurden Patienten mit und ohne anamnestisch bekanntes Vorhofflimmern eingeschlossen und die Patienten mussten zumindest einen der folgenden Risikofaktoren für Hirnschlag aufweisen: Alter >65 Jahre (Mittel war 71 Jahre), anamnestisch Hirnschlag oder TIA (bei 13%), Hypertonie (76%), Diabetes mellitus (32%) oder Herzinsuffizienz (60%). Daraus ergab sich ein mittlerer CHADS2-Score von 2,2. Patienten mit bekanntem chronischem Vorhofflimmern waren ausgeschlossen. Bei Studieneinschluss waren 21% der Patienten oral antikoaguliert und 62% unter Azetylsalizylsäure.
Bei den Nachsorgeuntersuchungen (alle 3–6 Monate) wurden die Schrittmacher- bzw. ICD-Geräte abgefragt und die dokumentierten AT/AF-Episoden sowie allfällige Endpunkte erfasst (mittlere Follow-up-Dauer 1,4 Jahre; total 3382 Patientenjahre). Als AT/AF-Episode galt eine Vorhofsfrequenz >175/min über eine Dauer von >20 Sekunden (gemäss gespeicherter Trenddaten; es wurden offenbar keine intrakardialen Elektrogramme analysiert). Mit diesen Daten aus den Gerätespeichern wurde der sogenannte «AT/AF-burden» ermittelt, d.h. die totale Anzahl Stunden mit Vorhofstachykardie bzw. -flimmern an einem einzelnen Tag. In jedem 30-Tage-Fenster vor einem thromboembolischen Ereignis wurde die maximale AT/AF-Dauer (h/Tag) erfasst. Der Medianwert des AT/AF-burden aller Fenster lag bei 5,5 h/Tag. Aufgrund dieses Wertes wurden folgende Risikogruppen definiert: Patienten ohne AT/AF-Episoden in den 30 Tagen vor einem thromboembolischen Ereignis (76%), solche mit tiefem «AT/AF-burden» von <5,5 h/Tag (12%) und solche mit hohem «AT/AF-burden» von >5,5 h/Tag (12%). Zwischen diesen drei Gruppen wurde die Häufigkeit von thromboembolischen Ereignissen verglichen und statistisch für andere Risikofaktoren bzw. für die die antithrombotische Therapie korrigiert. Während des gesamten Follow-up kam es zu insgesamt 40 Ereignissen (20 «strokes», 17 TIA und 3 andere systemische Embolien). Die jährliche Rate betrug 1,2%. Der Vergleich zwischen den drei Risikogruppen ist in Tabelle 1 dargestellt.
Tabelle 1.
Häufigkeit thromboembolischer Ereignisse in Abhängigkeit des «AT/AF-burden» in den 3 Gruppen ohne Vorhofflimmern bzw. bei tiefem oder hohem «AT/AF-burden» (modifiziert nach Glotzer TV, et al. ACC Scientific sessions 2008).
Tabelle 1.
Häufigkeit thromboembolischer Ereignisse in Abhängigkeit des «AT/AF-burden» in den 3 Gruppen ohne Vorhofflimmern bzw. bei tiefem oder hohem «AT/AF-burden» (modifiziert nach Glotzer TV, et al. ACC Scientific sessions 2008).
Aufgrund dieser Daten besteht bei einem «AT/AFburden» von >5,5 h/Tag eine Verdoppelung des Risikos für thromboembolische Ereignisse und zwar unabhängig von anderen Risikofaktoren. Ob dieser Grenzwert als alleiniges Kriterium genügt, um mit einer oralen Antikoagulation zu beginnen, kann wohl noch nicht mit Sicherheit gesagt werden. Dazu bräuchte es letztlich entsprechende Interventionsstudien, welche die Effektivität eines solchen Vorgehens belegen (Reduktion Hirnschlaghäufigkeit durch die Antikoagulation). Zumindest kann aber gefolgert werden, dass «nur» via Gerätespeicher detektierte (häufig asymptomatische) AT/AF-Episoden von mehrstündiger Dauer ein erhöhtes Risiko bedeuten. Damit müssen solche Speicherdaten ernst genommen werden und es sollte im Einzelfall und unter Beizug bisheriger Kriterien (CHADS2-Score) entschieden werden, ob und welche Thromboembolie-Prophylaxe nötig ist. Abschliessend bleibt festzuhalten, dass die Verwendung solcher Gerätespeicherdaten eine adäquate Programmierung der Speichereinstellungen und eine kritische Interpretation der Daten voraussetzt (z.B. Ausschluss von Artefakten, Over-/Under-Sensing usw.).
ICD-Therapie: «Neue Scores» und «Competing Risks»
Obwohl in der medikamentösen und interventionellen Therapie der ischämischen Herzkrankheit in den letzten Jahrzehnten grosse Fortschritte erzielt wurden, bleiben der plötzliche Herztod und die zuverlässige Erfassung der gefährdeten Patienten ein Problem. Die eingeschränkte linksventrikuläre Pumpfunktion (EF) nach Myokardinfarkt gilt weiterhin als der wichtigste, unabhängige Risikofaktor für die kardiale Mortalität. Daten mehrerer grosser Studien haben gezeigt, dass die primärprophylaktische ICD-Therapie bei Patienten mit einer EF von unter 30–35% eine bedeutsame Reduktion der Mortalität bewirkt [8, 9]. Die entsprechenden Behandlungsrichtlinien wurden kürzlich erneut überarbeitet [
2]. Trotzdem besteht eine anhaltende Kontroverse, ob eine schwer eingeschränkte EF als alleiniges Kriterium eine primärprophylaktische ICD-Implantation generell rechtfertig oder ob der Nutzen dieser Therapie abhängig von anderen Faktoren unterschiedlich sein kann [
10]. Anders ausgedrückt: innerhalb der Gruppe der Patienten mit einer tiefen EF kann das Risiko eines arrhythmiebedingten Todes heterogen sein, abhängig z.B. vom Ausmass der kardialen Funktionseinschränkung, der Symptomatik, des Zeitpunkts der ICD-Implantation nach Infarkt bzw. Revaskularisation oder der Komorbiditäten.
Abbildung 2.
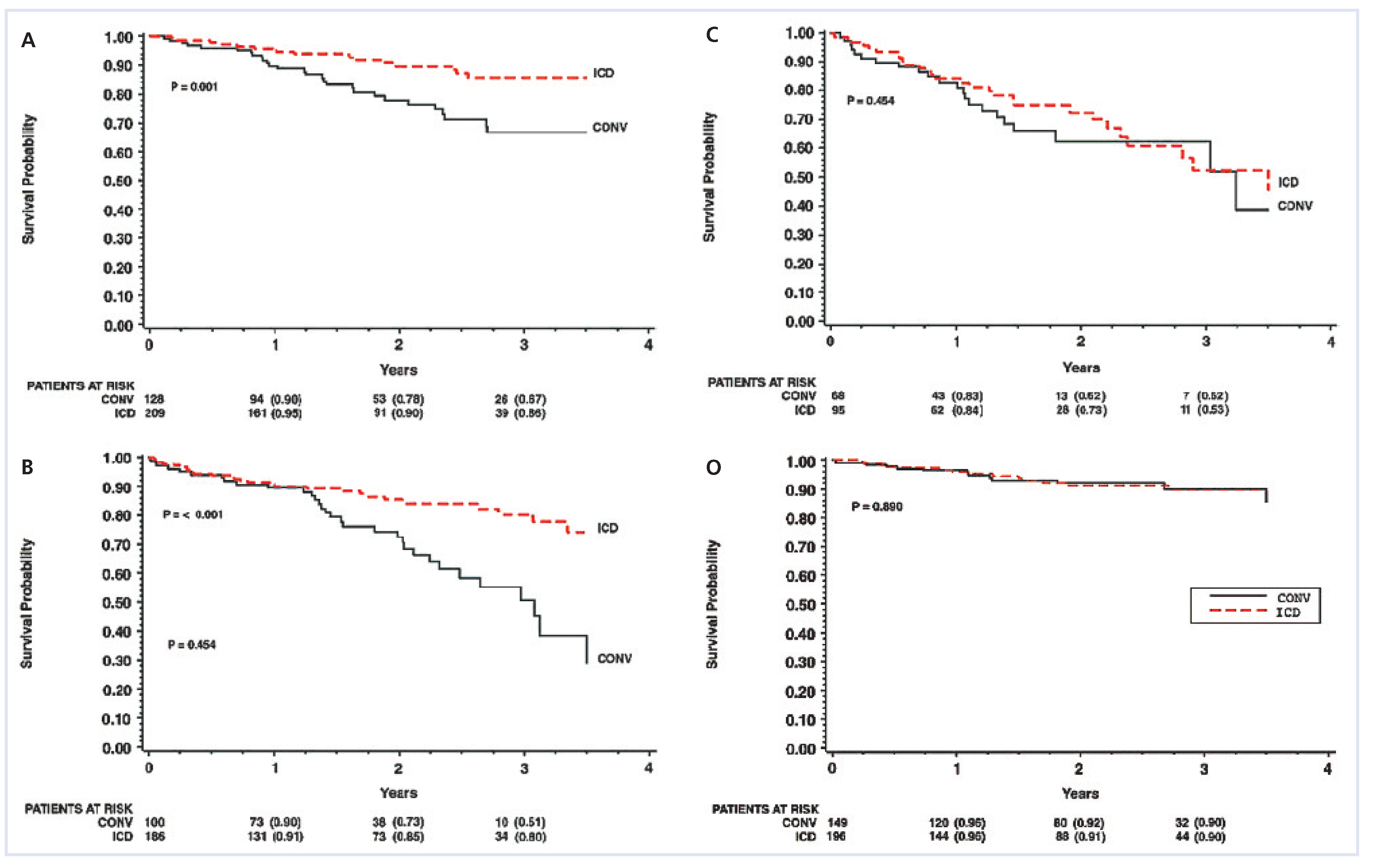
Kaplan-Meier-Überlebenskurven für konventionell (durchgehende Linien) bzw. mit ICD (gestrichelte Linien) behandelte Patienten in 4 Risikogruppen. O = Risikoscore = 0, A = Risikoscore = 1, B = Risikoscore = 2, C = Risikoscore ≥3. (Wiedergabe nach [
11]: Goldenberg I, Vyas AK, Hall WJ, Moss AJ, Wang H, He H, Zareba W, et al. for the MADIT-II Investigators. Risk stratification for primary implantation of a cardioverter-defibrillator in patients with ischemic left ventricular dysfunction. J Am Coll Cardiol. 2008;51:288–96. Copyright© 2009, mit freundlicher Genehmigung von Elsevier, Oxford, UK.).
Abbildung 2.
Kaplan-Meier-Überlebenskurven für konventionell (durchgehende Linien) bzw. mit ICD (gestrichelte Linien) behandelte Patienten in 4 Risikogruppen. O = Risikoscore = 0, A = Risikoscore = 1, B = Risikoscore = 2, C = Risikoscore ≥3. (Wiedergabe nach [
11]: Goldenberg I, Vyas AK, Hall WJ, Moss AJ, Wang H, He H, Zareba W, et al. for the MADIT-II Investigators. Risk stratification for primary implantation of a cardioverter-defibrillator in patients with ischemic left ventricular dysfunction. J Am Coll Cardiol. 2008;51:288–96. Copyright© 2009, mit freundlicher Genehmigung von Elsevier, Oxford, UK.).
In diesem Zusammenhang publizierten Goldenberg et al. kürzlich eine interessante Subanalyse der MADIT-II-Studienpopulation [
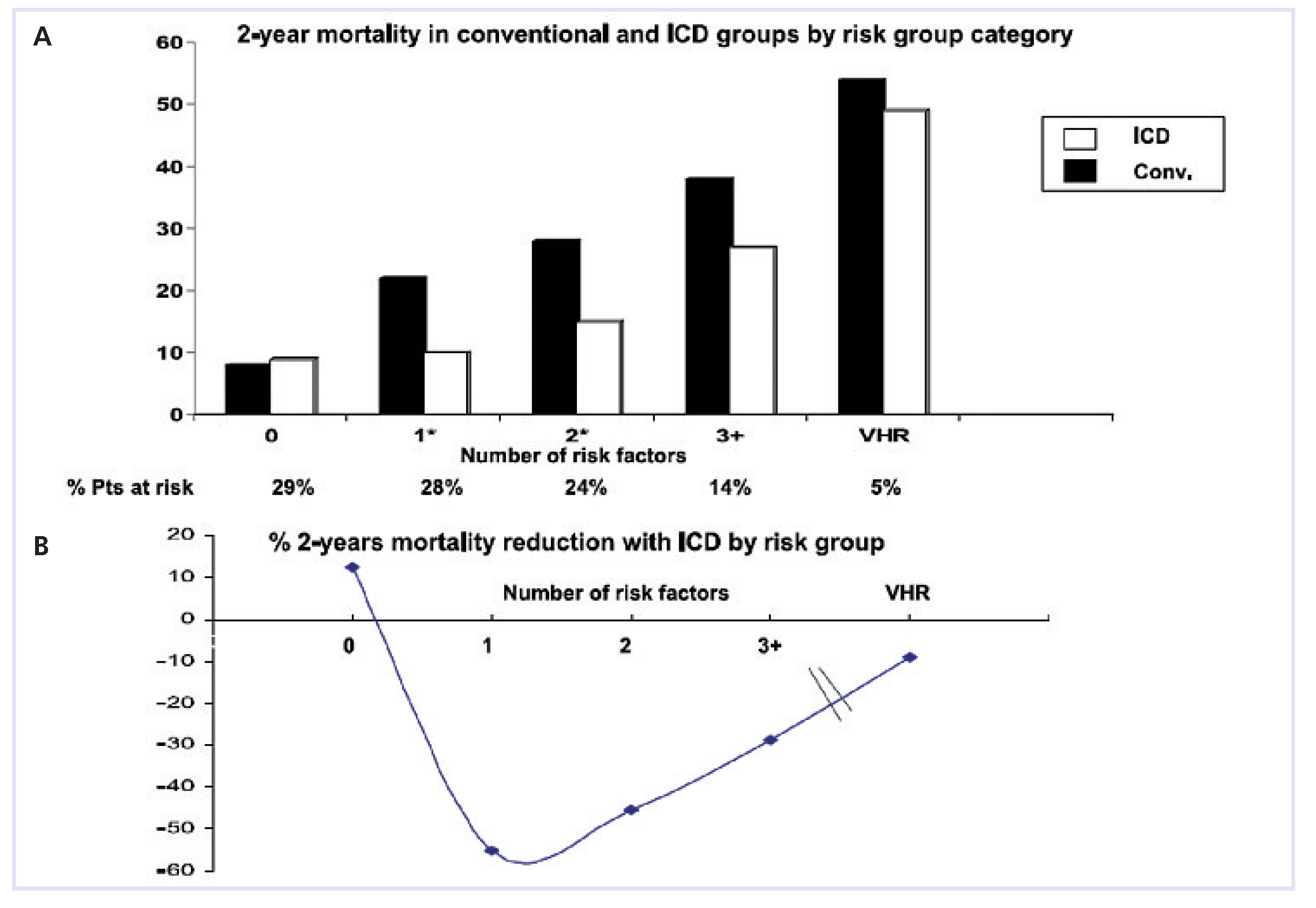
11]. Die Autoren haben einen einfachen klinischen Risikoscore entwickelt, um damit bei verschiedenen Risikogruppen den effektiven Überlebensvorteil durch die ICD-Therapie zu vergleichen. Primär wurden 17 mögliche Risikofaktoren evaluiert, 5 davon wurden nach komplexen statistischen Analysen als «signifikant» angesehen und in einen Score integriert. Der Risikoscore umfasst die folgenden Faktoren: NYHA-Funktionsklasse >II, Vorhofflimmern, QRS-Breite im EKG >120 ms, Alter >70 Jahre und Niereninsuffizienz (Harnstoff >9 mmol/l). Jeder Faktor ergab einen Score-Punkt. Anhand dieses Scores wurde das Überleben mit und ohne ICD-Implantation in den Risikogruppen mit einem Score von 0, 1, 2 oder ≥3 verglichen. Abbildung 2 zeigt die Überlebenskurven in den verschiedenen Risikogruppen bei Patienten mit vs. ohne ICD-Implantation. Die Autoren schlossen aus diesen Daten, dass der Nutzen einer ICD-Therapie in zwei Subgruppen des MADIT-II-Kollektivs limitiert sein kann: einerseits in der Gruppe ohne Risikofaktoren (Score 0) mit einem entsprechend tiefem Mortalitätsrisiko und andererseits in der Gruppe mit sehr hohem Risiko (Score ≥3) als Ausdruck einer fortgeschrittenen Herzkrankheit oder erheblicher Komorbidität. In den mittleren Risikogruppen mit Score 1 und 2 war jedoch der ICD sehr effektiv. Daraus ergibt sich bezüglich Risikoreduktion durch die ICD-Implantation ein «U-shaped pattern» mit hohem Nutzen bei Patienten mit mittlerem Risiko und abgeschwächter Effektivität bei sehr tiefem oder sehr hohem Risiko (Abb. 3).
Abbildung 3.
A. 2-Jahres-Mortalität bei konventionell (schwarze Säulen) vs. mit ICD (weisse Säulen) behandelten Patienten in den verschiedenen Risikogruppen mit 0, 1, 2 oder ≥3 Risikofaktoren, sowie einer zusätzlichen, separat analysierten Hochrisikogruppe mit schwerer Niereninsuffizienz. *. p <0,05. VHR = very high risk. B. Reduktion (%) der 2-Jahres-Mortalität durch die ICD-Therapie in den gleichen Risikogruppen (wie unter A). (Wiedergabe nach [
11]: Goldenberg I, Vyas AK, Hall WJ, Moss AJ, Wang H, He H, Zareba W, et al. for the MADIT-II Investigators. Risk stratification for primary implantation of a cardioverter-defibrillator in patients with ischemic left ventricular dysfunction. J Am Coll Cardiol. 2008;51:288–96. Copyright© 2009, mit freundlicher Genehmigung von Elsevier, Oxford, UK.).
Abbildung 3.
A. 2-Jahres-Mortalität bei konventionell (schwarze Säulen) vs. mit ICD (weisse Säulen) behandelten Patienten in den verschiedenen Risikogruppen mit 0, 1, 2 oder ≥3 Risikofaktoren, sowie einer zusätzlichen, separat analysierten Hochrisikogruppe mit schwerer Niereninsuffizienz. *. p <0,05. VHR = very high risk. B. Reduktion (%) der 2-Jahres-Mortalität durch die ICD-Therapie in den gleichen Risikogruppen (wie unter A). (Wiedergabe nach [
11]: Goldenberg I, Vyas AK, Hall WJ, Moss AJ, Wang H, He H, Zareba W, et al. for the MADIT-II Investigators. Risk stratification for primary implantation of a cardioverter-defibrillator in patients with ischemic left ventricular dysfunction. J Am Coll Cardiol. 2008;51:288–96. Copyright© 2009, mit freundlicher Genehmigung von Elsevier, Oxford, UK.).
Diese Daten zeigen, dass durch Einsatz eines einfachen klinischen Risikoscores Subgruppen identifiziert werden könnten, bei welchen der Nutzen der primärprophylaktischen ICD-Therapie bei ischämischer Herzkrankheit und schwer eingeschränkter Pumpfunktion limitiert sein kann. Ob eine solche zusätzliche Risikostratifizierung in diesem Kollektiv den effektiven Nutzen und die Kosteneffektivität der ICD-Therapie steigert, bleibt in weiteren Studien prospektiv zu validieren. Zu berücksichtigen ist zudem, dass sich die Risiken dynamisch verhalten und deshalb periodische Risikoanalysen notwendig sein dürften.
In einer interessanten Arbeit haben Koller et al. [
12] das «competing risk» von ICD-Patienten und dessen Einfluss auf ICD-Therapien analysiert. Sie gingen davon aus, dass zwei Patientengruppen nicht von einer ICD-Implantation, obwohl diese gemäss Guidelines indiziert wäre, profitieren können. Diejenigen, die vor einer ersten ICD-Intervention versterben und diejenigen, die nie eine ICD-Intervention benötigen. Es gibt somit zwei sich strikt ausschliessende «Risiken»: eine adäquate ICD-Intervention und der Tod ohne jegliche vorgängige ICD-Intervention.
Dieser Aspekt wurde in den bisherigen randomisierten Studien nicht berücksichtigt, unter anderem auch deshalb, weil dort Patienten mit einem «hohen» Mortalitätsrisiko jeweils ausgeschlossen wurden. In einem grösseren Register von 450 Patienten mit koronarer oder dilatativer Kardiopathie und einer mittleren Beobachtungszeit von 3,5 Jahren wurde einerseits das Ausmass dieses «competing risk» untersucht und andererseits nach Prädiktoren gesucht. Ungefähr 50% aller Patienten erhielten im Verlauf eine ICDTherapie (mehrheitlich Antitachykardie-Pacing). 11% der Patienten verstarben ohne jegliche ICD-Interventionen. Wenn effektives Kammerflimmern (nicht nur eine schnelle Kammertachykardie in der Flimmerzone) als Surrogatmarker für einen «sicheren» Tod angesehen wurde, zeigte es sich, dass nach etwa 3 Jahren kaum mehr erste Episoden mit Kammerflimmern auftraten (der eine Teilaspekt des «competing risks» also vernachlässigbar wurde), aber im Verlauf 15% der Patienten ohne jegliche ICD-Therapie verstarben.
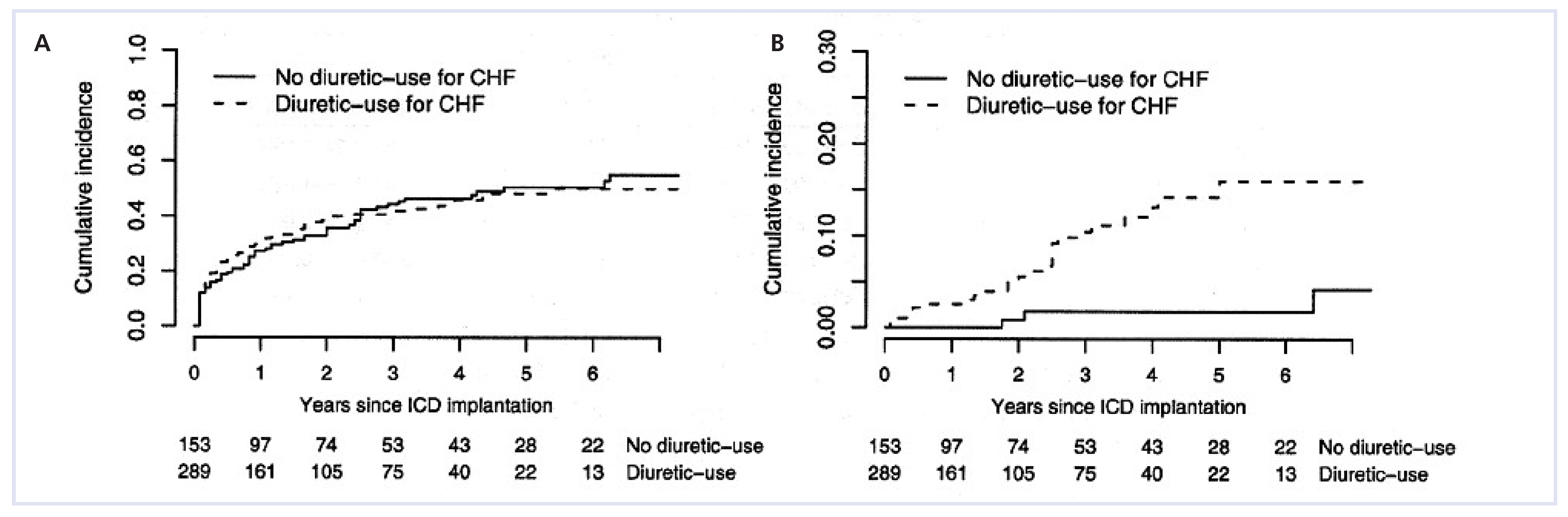
Ein relevanter Prädiktor für das «competing risk» war die Herzinsuffizienz, ausgedrückt im Bedarf an diuretischer Therapie. Währenddem es für alle Formen der ICD-Intervention keine Rolle spielte, ob Patienten Diuretika erhielten oder nicht (Abb. 4A), war dies für den Faktor «Tod vor erster ICD-Inter-vention» relevant und statistisch hoch sigifikant (Abb. 4B).
Abbildung 4.
Abbildung 4A zeigt mittels «cumulative incidence function», dass der Diuretikagebrauch als Surrogatmarker für eine Herzinsuffizienz (CHF) in Bezug auf die erste appropriate ICD-Therapie keinen Prädiktor darstellt, indem praktisch gleich viele Patienten in beiden Gruppen eine ICD-Therapie erhielten. Hingegen ist die Diuretikatherapie ein starker Prädiktor für Tod jeglicher Ursache (4B). (Wiedergabe nach [
12]: Koller MT, Schaer B, Wolbers M, Sticherling C, Bucher HC, Osswald S. Death without prior appropriate implantable cardioverter-defibrillator therapy: a competing risk study. Circulation. 2008;117:1918–26. Copyright© 2009, mit freundlicher Genehmigung von Wolters Kluwer Health, Baltimore, USA.).
Abbildung 4.
Abbildung 4A zeigt mittels «cumulative incidence function», dass der Diuretikagebrauch als Surrogatmarker für eine Herzinsuffizienz (CHF) in Bezug auf die erste appropriate ICD-Therapie keinen Prädiktor darstellt, indem praktisch gleich viele Patienten in beiden Gruppen eine ICD-Therapie erhielten. Hingegen ist die Diuretikatherapie ein starker Prädiktor für Tod jeglicher Ursache (4B). (Wiedergabe nach [
12]: Koller MT, Schaer B, Wolbers M, Sticherling C, Bucher HC, Osswald S. Death without prior appropriate implantable cardioverter-defibrillator therapy: a competing risk study. Circulation. 2008;117:1918–26. Copyright© 2009, mit freundlicher Genehmigung von Wolters Kluwer Health, Baltimore, USA.).
Die Autoren folgerten, dass diese «competing risks», also z.B. relevante Komorbiditäten, vermehrt in die Risikoüberlegungen Einzug finden müssten und diese Analyse auch zum Zeitpunkt eines Aggregatsaustauches erneut vorgenommen werden sollte.
Schlussfolgerung
Erste Studienresultate sprechen dafür, dass im Schrittmacherspeicher dokumentierte mehrstündige Episoden von Vorhofflimmern einer sorgfältigen Evaluation bezüglich Thromboembolieprophylaxe gemäss gängigen Richtlinien bedürfen. Das Risiko für Hirnschläge scheint dabei nämlich zweifach erhöht zu sein.
Bei der primärprophylaktischen ICD-Implantation ist trotz des anerkannten Markers der schwer eingeschränkten LV-Funktion die Risikoverteilung für Arrhythmien sehr heterogen und wahrscheinlich auch abhängig von weiteren Parametern, wie dies in einer Subanalyse der MADIT-II-Daten gezeigt werden konnte. Es wird sich zeigen, ob der darauf aufbauende Score Einzug in den klinischen Alltag finden wird, wozu eine prospektive Validierung notwendig sein wird. Im Weiteren wird man in Zukunft wohl auch mehr den «competing risks» der Patienten, die für eine ICD-Implantation qualifizieren, Rechnung tragen müssen, da ein nicht unerheblicher Anteil der Patienten ohne jegliche ICD-Intervention verstirbt.